Cukura diabēta ārstēšanā daudzi momenti ir saistīti ar slimnieka nieru funkciju – tajos ietilpst glikēmijas kontroles metodes, komplikācijas, ko izsauc hiperglikēmijas terapija, un nenoteiktais rezultāts insulīna terapijai pacientiem ar progresīvu nieru mazspēju. Jārūpējas arī par asinsspiediena un plazmas lipīdu līmeņa koriģēšanu, lai mazinātu kardiovaskulāro saslimstību un agrīnu nāvi. Tāpat jādomā par hroniskas nieru mazspējas komplikācijām: anēmiju, hiperfosfatēmiju un hiperparatireoīdismu, kas nosaka nieru funkciju samazināšanos.
Hroniska nieru mazspēja (HNM) ir bieži sastopams stāvoklis - aprēķināts, ka no tās cieš 11% no ASV iedzīvotājiem jeb 19 miljoni cilvēku, un vairāk nekā 50 miljoni cilvēku pasaulē. Kaut gan dati par HNM incidenci Latvijā nav pilnīgi, var domāt, ka tā ir līdzīga. Arī cukura diabēts ir sasniedzis epidēmisku incidenci - slimo ap 20 miljo-niem cilvēku ASV un 171 miljonu pasaulē. Latvijā 2007. gadā bija apzināti 57 000 cukura diabēta pacientu, un ir iespējams, ka šis skaitlis varētu būt divreiz lielāks (daudziem cilvēkiem ar 2. tipa cukura diabētu noteikti simptomi nav vērojami un viņi medicīnisku palīdzību nemeklē).
Cukura diabēts bieži ir saistīts ar HNM; 45% pacientu, kas saņem dialīzes terapiju, cukura diabēts ir primārais nieru mazspējas iemesls. Mērena līdz smaga HNM ir atrodama vēl 15-23% CD pacientu. Ir svarīgi atcerēties par abu slimību kombināciju, jo šajos gadījumos komplikāciju un arī nāves risks ir daudz lielāks nekā slimniekiem bez šāda papildu aspekta. Turklāt slimniekiem ar mikroalbuminūriju ir divreiz augstāks kardiovaskulārais risks nekā tiem, kam albuminūrijas nav.
Diagnoze
Tradicionāli termins diabētiskā nefropātija nozīmē hronisku nieru mazspēju cukura diabēta slimības gaitā. Šis nosaukums patiesībā būtu lietojams, ja nieru biopsija histopatoloģiski pierāda nieru bojājumu, kas atbilst diabētiskām pārmaiņām (difūza vai nodulāra diabētiskā glomeruloskleroze - 1. attēls). Bez biopsijas HNM, kam ticams cēlonis ir cukura diabēts, būtu saucama par diabētisku nieru slimību (NS).
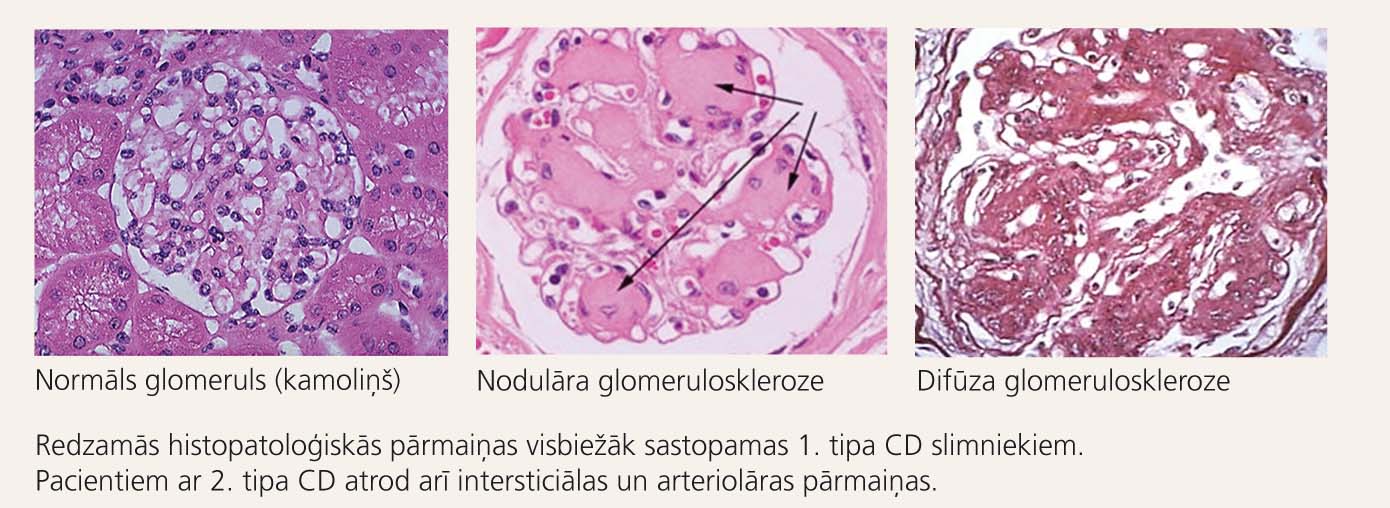

1. attēls
Histopatoloģiskās izmaiņas nierēs pacientam ar cukura diabētu
Neskatoties uz izcelsmi, HNM ir definēta kā nieru bojājums vai samazināta nieru funkcija, kas ieilgst trīs vai vairāk mēnešus. Nieru bojājumu var apstiprināt ar izmainītu rentgenoloģisko ainu, urīna sedimentu, vai visbiežāk - proteinūriju. HNM iedala piecās stadijās atkarībā no aprēķinātā GFĀ (salīdzinošās HNM stadijas ir parādītas 1. tabulā).
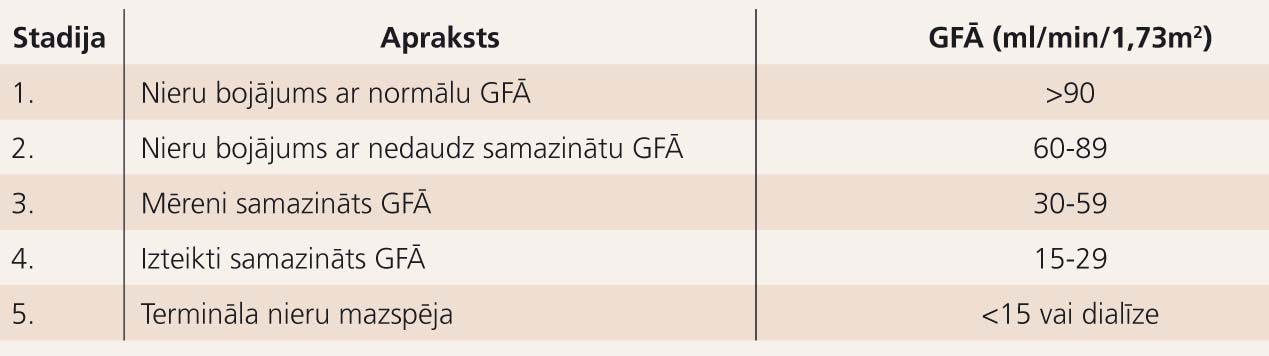

1. tabula
Hroniskas nieru mazspējas klasifikācija
Klīniskajā laboratorijā nieru funkciju šodien nosaka kā aprēķinātu GFĀ, pielietojot vienādojumus, kuros vērā ņemts slimnieka vecums, dzimums un seruma kreatinīna līmenis.
Diabētiskās NS klīniskā diagnoze visbiežāk tiek noteikta, atrodot albuminūriju.
- Mikroalbuminūrija ir definēta kā 30-300 mg albumīna urīnā 24 stundu laikā. Visvieglāk ir pielietot albumīna-kreatinīna proporciju (AKP) urīna paraugā, nevis 24 stundu kolekcijā, jo pierādījies, ka starp AKP un 24 stundu kolekcijas proteinūriju ir ļoti laba korelācija. Mikroalbuminūrija eksistē, ja albumīna/kreatinīna proporcija ir 30-300 mg/gm.
- Makroalbuminūrija ir definēta kā AKP > 300 mg/gm jeb > 300 mg albumīna 24 stundās.
Ja albumīns urīnā tiek atrasts, jāizslēdz infekcijas, sirds mazspēja, grūtniecība, smaga hipertensija un hematūrija kā proteinūrijas cēloņi un pirms galīgās proteinūrijas diagnozes apstiprināšanas atkārtoti jānosaka albuminūrija trīs reizes trīs līdz sešu mēnešu laikā.
Pacientiem ar CD, kuriem atrod makroalbuminūriju, diezgan droši var pieņemt, ka HNS iemesls ir diabēts, jo korelācija ir pierādīta ar nieru biopsijām (vismaz 1. tipa CD pacientiem). Lai gan 1. tipa CD izraisa vieglākas patoloģiskās pārmaiņas, tomēr rada HNM risku, sevišķi, ja slimniekam ir hipertensija. Asociācija starp mikroalbuminūriju un diabētisko NS nav tik saistoša 2. tipa CD slimniekiem - tikai 30% no šādiem pacientiem atrod tipiskas pārmaiņas nieres biopsijā. Ja 2. tipa CD slimniekam ir retinopātija, tad parasti būs arī diabētiskā NS.
Kopsavilkums
CD slimniekam ar makroalbuminūriju vai mikroalbuminūriju un retinopātiju nieru bojājumu var pieskaitīt cukura diabēta sekām bez biopsijas, un slimības smagumu jānovērtē, vadoties no GFĀ. Ja ir smagi bojāta nieru funkcija, albuminūrija > 500 mg/dienā un ātri progresējoša proteinūrija (krītošs GFĀ), slimnieks ir jānosūta pie speciālista.
Cukura līmeņa kontrole
HbA1c ir visierastākais rādītājs, ko pielieto glikēmijas kontroles novērtējumam. HbA1c var lietot arī nieru slimniekiem, un tiek rekomendēts parastais mērķis (nepareizs, jo slimniekiem bieži ir anēmija ar dzelzs trūkumu, hemolīzi un īsāku eritrocītu dzīvi.
Hiperglikēmijas terapija slimniekiem ar hronisku nieru mazspēju
Hiperglikēmijai ir centrālā loma HNS patoģenēzē, tāpēc optimāla cukura līmeņa kontrole ir ļoti svarīga, jo īpaši 1. tipa CD slimniekiem. Ir pierādīts, ka ar stingru glikēmijas kontroli var samazināt albuminūriju, kā arī retinopātijas tendenci un bremzēt HNM attīstību.
Insulīns
Terapijas mērķis - HbA1c
Perorālie hipoglikēmiskie līdzekļi
Nieru mazspēja samazina daudzu medikamentu klīrensu - rezultātā medikamentu un to metabolītu ietekme ir ilgāka un nelabvēlīgu blakusefektu risks ir augstāks. Visaugstākais tas ir slimniekiem ar mērenu un smagu HNM (3.-5. stadija). HNM diagnoze un mainīga nieru funkcija prasa, lai ārsts regulāri pārskata hipoglikēmiskos līdzekļus un to devas vai maina preparātus, lai sasniegtu labu cukura līmeņa kontroli bez blakus efektiem.
- Sulfonilurīnvielas grupas preparāti šodien ir visbiežāk pielietotās zāles CD terapijā. Lielākā daļa šo preparātu un to metabolītu tiek izdalīti urīnā, un HNM pacientiem ir aprakstīti smagi hipoglikēmijas gadījumi. Pirmās paaudzes sulfonilurīnvielas preparātus HNM slimniekiem nevajadzētu nozīmēt. No otrās pakāpes sulfonilurīnvielas grupas lietojami ir glipizīds (glipizidum), arī glikvidons (gliquidonum), jo to metabolīti nav aktīvi, tāpēc hipoglikēmijas risks ir zemāks.
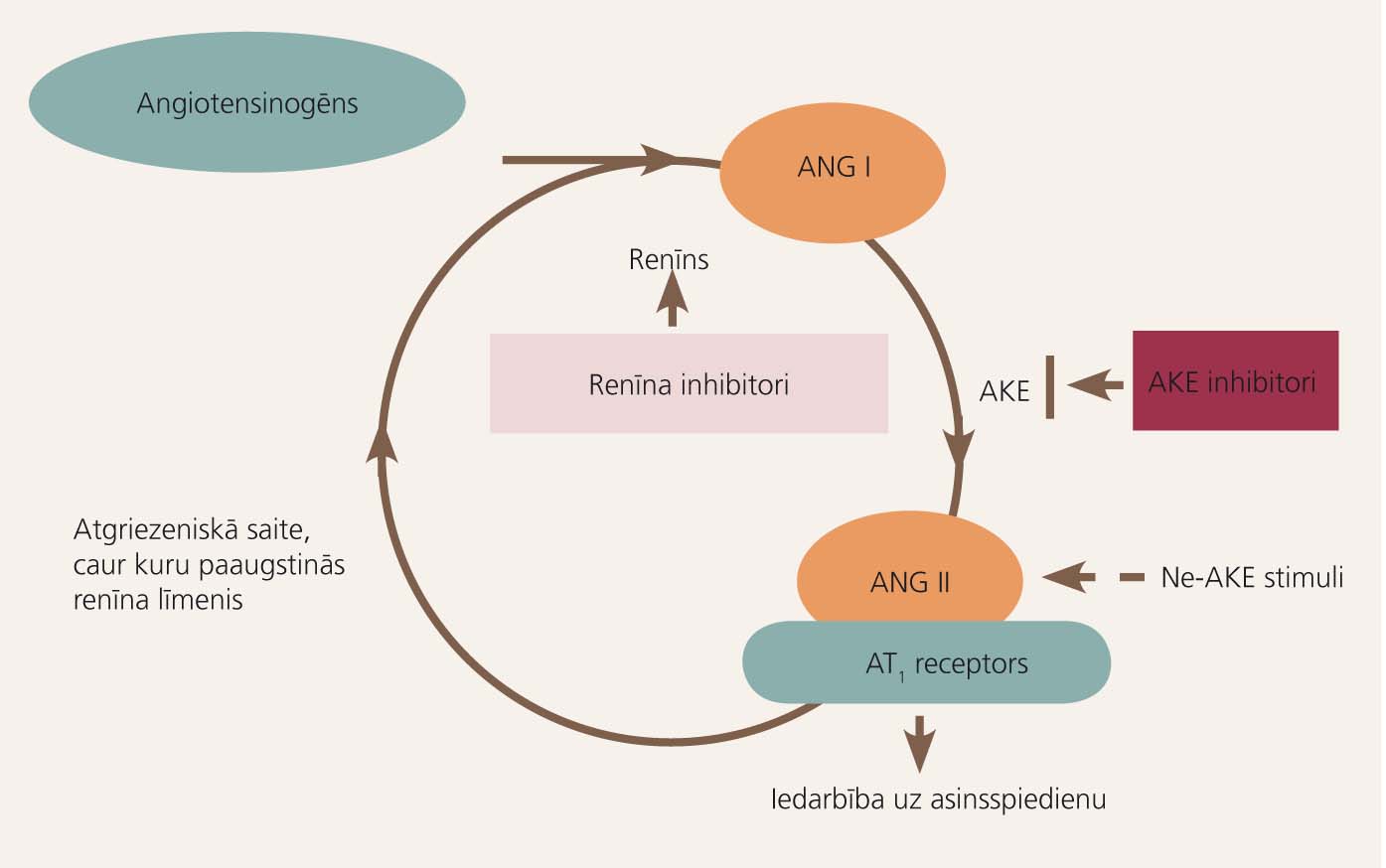

2. attēls
Aliskirēns: pirmais renīna inhibitors klīniskai praksei
- Neskaidru mehānismu rezultātā a- glikozidāzes inhibitori vai to metaboliskie produkti var bojāt aknas, tāpēc šīs grupas medikamentus nerekomendē, ja slimnieka seruma kreatinīna līmenis ir > 2mg/dl.
- Biguanīdu grupas preparāti (metformīns) nerada lielu hipoglikēmijas risku. Tomēr metformīns 100% tiek neizmainīts izdalīts urīnā un uzkrājoties var izsaukt lakt acidozi pat pacientiem ar mērenu nieru mazspēju. Šis preparāts ir kontrindicēts vīriešiem ar seruma kreatinīnu >1,5 mg/dl un sievietēm ar >1,4 mg/dl. Arī slimniekiem ar vieglāku HNM metformīna lietošanu jāpārtrauc pirms rentgena procedūras ar kontrastvielu, jo draud akūta nieru mazspēja.
- Tiazolidīndioni (TZD) ir PPARg ago nisti, kuriem piemīt šķietami labvēlīgs efekts uz nierēm, mazinot albuminūriju un mazinot vai varbūt pat novēršot HNM. Šīs grupas preparāti tiek metabolizēti aknās, tāpēc pacientiem ar HNM tiek pielietoti bez devas maiņas. Jāņem vērā, ka TZD blakusefekts ir nātrija un šķidruma retence, kas var manifestēties kā tūska un sirds mazspēja. Tūska slikti padodas parastajiem diurētiskajiem līdzekļiem, un ir jālieto amilorīds. Pastāv varbūtība, ka rosiglitazons ir saistīts ar paaugstinātu miokardiāla infarkta varbūtību.
- No meglitinīdu grupas preparātiem repaglinīdu (repaglinidum) var pielietot bez devas maiņas.
- No inkretīna mimētisko līdzekļu preparātiem eksenatīdu (exenatide) var lietot bez devas maiņas, bet sitagliptīns (sitagliptin) izdalās neizmainīts urīnā, un to nevajadzētu lietot, ja GFĀ ir
Kopsavilkums
Daudzi perorālie hipoglikēmiskie līdzekļi ir kontrindicēti, ja pacientam ir nieru mazspēja. Lai paaugstinātu insulīna sekrēciju 2. tipa CD slimniekam, var lietot glimepirīdu vai repaglinīdu. Tiazolidīndionus var lietot, taču jāuzmanās sirds mazspējas gadījumos. Skat. 2. tabulu.
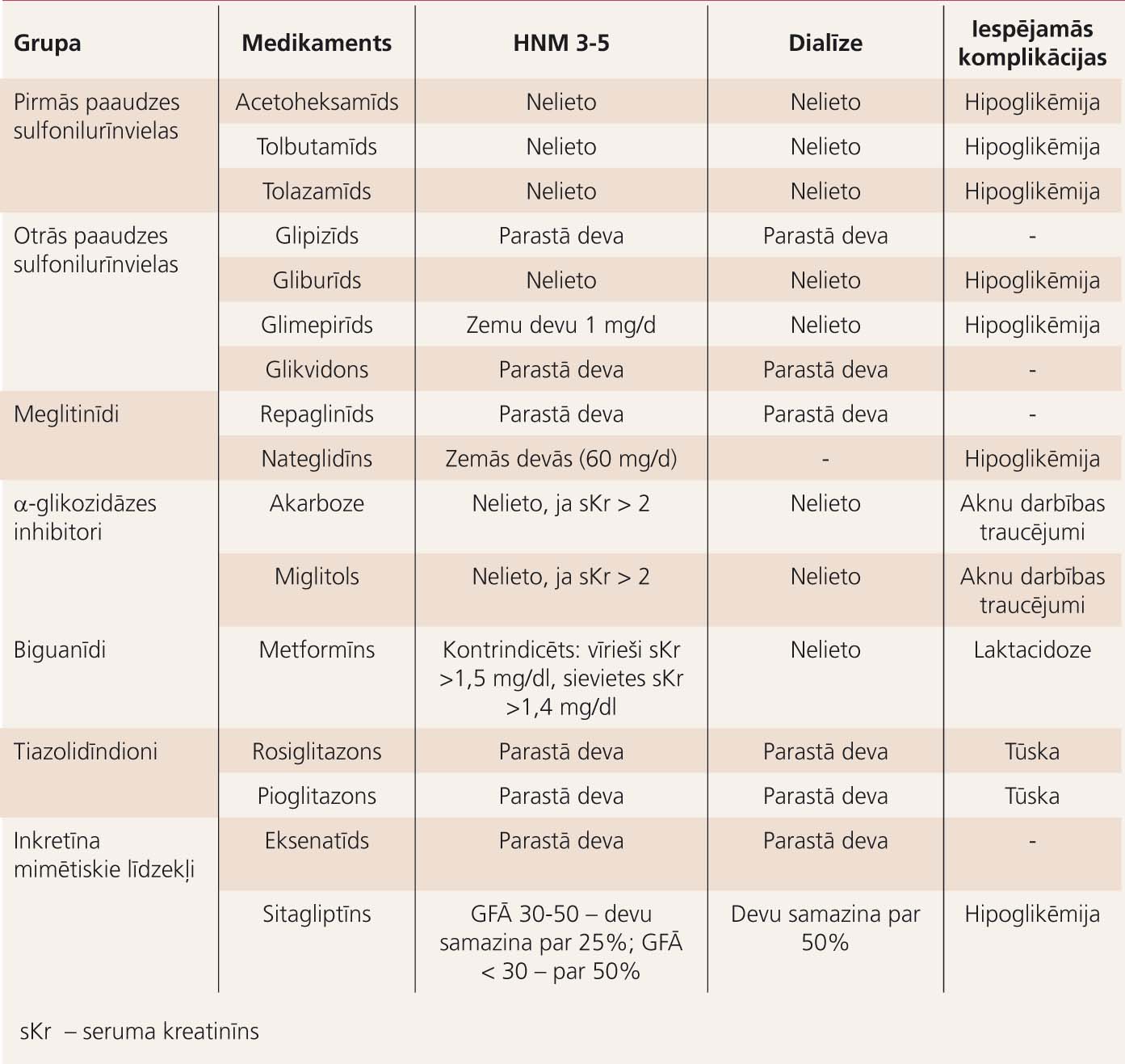

2. tabula
Hiperglikēmijas terapija slimniekiem ar hronisku nieru mazspēju
Kardiovaskulāro komorbiditātes faktoru ārstēšana
Arteriālā hipertensija
Augsts asinsspiediens ir drošs diabētiskās NS attīstības riska faktors un nepietiekamas kontroles gadījumā steidzina GFĀ un nieru funkcijas zušanas jaudu. Asinsspiedienu > 130/80 mmHg atrod 30-60% HNM slimnieku - augstāka prevalence ir saistīta ar smagāku proteinūriju. Hipertensija ir saistīta ar lielāku kardiovaskulāru komorbiditāti un mirstību.
Būtisks diabētiskās NS patoģenētiskais faktors ir pastiprināta renīna-angiotensīna-aldosterona sistēmas (RAAS) galaprodukts angiotensīns II, kas izsauc vazokonstrikciju un kā fibrinoģenēzi veicinoša viela un augšanas faktors nosaka ekstracelulārās matrices olbaltumu izmaiņas, šūnu hipertrofiju un proliferāciju. Tāpēc kā galvenos hipertensijas terapijā lieto angiotensīna konvertāzes (AKE) inhibitorus un angiotensīna II receptoru blokatorus (ARB). Pētījumi pierāda, ka terapija ar vienu vai abiem šiem līdzekļiem samazina vai aptur proteinūrijas progresiju slim niekiem ar 1. un arī 2. tipa CD. Tāpat RAAS blokāde aptur HNM progresu uz terminālu nieru mazspēju un stabilizē slimību (pat uz visu mūžu). Kaut gan visi AKE inhibitori un ARB ir efektīgi līdzekļi, pētījumos konstatēts, ka telmisartāns iedarbojas labāk par citiem sartāniem, piemēram, losartānu, pat neskatoties uz to, ka efekts uz asinsspiedienu var būt vienāds.
Lai arī AKE inhibitori un ARB bloķē RAAS, seruma aldosterona līmenis saglabājas augsts. Šis fakts var būt iemesls kardiovaskulāru problēmu tālākai attīstībai. Daži reti ziņojumi norāda, ka, AKEI/ARB terapijai pievienojot spironolaktonu, iegūst vēl labāku proteinūrijas samazināšanos un lēnāku nieru slimības progresiju. Tomēr spironolaktons un citi aldosterona antagonisti var izsaukt smagu hiperkaliēmiju, tāpēc nepieciešama bieža kālija līmeņa kontrole (personīgi es neiesaku spironolaktona lietošanu HNM slimniekam).
Nesen lietošanai ir apstprināts jauns antihipertensīvais līdzeklis, kas ir pirma is tiešais renīna inhibitors - aliskirēns (2. attēls). Aliskirēns paredzēts lietošanai monoterapijā vai kombinējot ar citiem antihipertensīviem līdzekļiem. Pētījumā pacientiem ar 2. tipa cukura diabētu un protei nūriju aliskirēns kombinācijā ar losartānu, salīdzinot ar placebo, par 20% efektīvāk samazināja albumīna/kreatinīna rādītāju. Pētījums demonstrēja aliskirēna renoprotektīvo efektu pacientiem ar hipertensiju, 2. tipa cukura diabētu un nefropātiju. Šī medikamenta lietošana hipertensijas slimniekiem ar smagu nieru mazspēju (GFĀ
Slimniekiem ar CD un HNM tiek rekomendēta terapija ar AKE inhibitoriem un ARB, bet daudzos gadījumos, lai sasniegtu vēlamo asinsspiediena līmeni, ir nepieciešami pat četri, pieci medikamenti. Parastajā kombinācijā ietilpst b-blokatori, kalcija kanālu blokatori un diurētiskie līdzekļi. Ar laiku, kad nieru funkcija pasliktinās, tiazīdu grupas diurētiskie līdzekļi vairs nav efektīgi, tāpēc, slimniekam, kam GFĀ ir
Hiperlipidēmija
Kardiovaskulāro riska faktoru - tai skaitā dislipidēmijas - modifikācijai ir liela loma, lai mazinātu sirds un asinsvadu bojājumus pacientiem ar CD un HNM. Holesterīna un citu lipīdu līmenis būtu jānosaka katru gadu, ar zema blīvuma lipoproteīnu holesterīna mērķi
Medikamentu deva ir jāpielāgo atkarībā no nieru mazspējas smaguma. Nav jāsamazina niacīna, ezetimiba, atorvastatīna un pravastatīna deva. Blakusefekti (galvenokārt rabdomialīze) ir novēroti ar lovastatīnu, rosuvastatīnu un fluvastatīnu, un to deva ir jāsamazina slimniekiem 4. vai 5. HNM stadijā (GFĀ
Anēmija
Anēmija HNM slimniekiem ir definēta, ja hemoglobīna līmenis ir 12 gm/dl, eritropoietīna terapija neuzlaboja dzīves kvalitāti un pat paaugstināja kardiovaskulāro risku (pirms ieteikt intensīvu eritropoetīna terapiju šajā pacientu grupā, jāgaida turpmāki pētījumi). Ja lieto eritropoetīnu, jānosaka dzelzs un feritīna līmenis, saglabājot feritīnu > 100 mg/l.
Kalcijs, fosfors un parathormons
Izmainīts kalcija un fosfora metabolisms HNM slimniekiem ir saistīts ar kalcitriola (aktīvā D vitamīna) trūkumu un sekundāru hiperparatireoīdismu. Rezultātā veidojas renāla osteodistrofija ar kaulu pārmaiņām un vaskulāru pārkaļķošanos. Nosakot kalcija, fosfātu un intaktā parathormona (iPTH) līmeni, var identificēt HNM radītās kaulu problēmas un novērst kaulu lūzuma risku. Šo rādītāju noteikšanas biežums parādīts 3. tabulā. Seruma fosfātu līmenis ir jātur
Diēta
HNM slimnieku diētas sastāvs var manāmi ietekmēt slimības gaitu, izsaucot hiperkaliēmiju, hiperfosfatēmiju un hipertensiju. Tādos gadījumos diēta ir jākoriģē, samazinot uzturā to produktu apjomu, kuros ir daudz kālija, fosfora un nātrija. Tā kā CD jau pats par sevi ierobežo ēdiena izvēli, rekomendācijas var būt sarežģītas un ir vēlams vērsties pēc padoma pie uztura speciālista. Proteīnu uzņemšana HNM 1.-4. stadijas slimniekiem ir jāsamazina līdz 0,8 g/kg ķermeņa svara dienā - rezultātā iegūst albuminūrijas samazināšanos un lēnāku nieru mazspējas attīstību. Kādreizējā rekomendācija līdzsvarot proteīnu zudumu urīnā ar liela proteīnu daudzuma iekļaušanu diētā smaga nefrotiskā sindroma gadījumos ir pilnīgi nepareiza, jo paātrina HNM gaitu.
Kopsavilkums
- Cukura diabēta izplatība ļoti strauji pieaug, bet bieži tā atklāšana ir novēlota.
- Diabētiskā nefropātija attīstās ap 30% CD slimnieku, bet bieži netiek savlaicīgi diagnosticēta.
- Agrīna diabētiskās nefropātijas konstatēšana ir viegli realizējama un ļoti būtiska iznākumu uzlabošanai.
- Mikroalbuminūrijas novēršanas pamatpostulāti: normoglikēmija, asinsspiediena kontrole, RAAS inhibīcija, nesmēķēšana.
- Insulīna metabolismu iespaido nieru funkcijas, un insulīna deva bieži ir jāsamazina.
- Atkarībā no HNM smaguma medikamentu devas un izvēle ir jāmaina un jāierobežo proteīna un kālija daudzums uzturā (4. tabula).
- Hipoglikēmija HNM slimniekiem attīstās bieži, sulfonilurīnvielas grupas preparāti ir lietojami piesardzīgi.
- Diabēta slimniekiem ar nieru mazspēju ir augsts citu mikro- un makrovaskulāru komplikāciju risks, ko gandrīz pilnīgi var novērst, pielietojot RAAS blokatorus un statīnu terapiju.
- AKE inhibitoru un ARB terapija jāuzsāk, līdzko diabētiskā NS ir atklāta. Savienojot AKE inhibitorus ar ARB, panākami labāki rezultāti. Aliskirēna loma vēl nav pilnīgi noskaidrota.
- Konstatējot HNM, jāsāk rūpēties par tās komplikācijām - anēmiju un kalcija/fosfora vielmaiņas izmaiņām.
- Pēdējās divās desmitgadēs prognoze pacientiem ar diabētisko nefropātiju ir uzlabojusies un nieru mazspējas attīstības tempu var samazināt. Taču, lai efektīgi samazinātu diabētiskās nefropātijas epidēmiju, ir svarīga zinoša ārsta un paklausīga slim-nieka sadarbība.