Hospitālī iegūtā pneimonija (HIP) skar astoņus no tūkstoša hospitalizēto slimnieku (0,8%). Hospitālī iegūtā pneimonija ir otrā biežākā hospitālī iegūtā infekcija pēc hospitālī iegūtās urīnceļu infekcijas. Īpaši bieži (15-20%) HIP skar intensīvās terapijas nodaļu slimniekus. Šajā rakstā centīsimies atspoguļot hospitālī iegūtas pneimonijas diagnostikas un ārstēšanas aktuālās, Amerikas Torakālās biedrības un Amerikas Infekcijas slimību biedrības kopīgi izstrādātās, vadlīnijas.
Dati par hospitālī iegūtu pneimoniju
- No visām hospitālī iegūtajām infekcijām HIP gadījumā ir visaugstākā letalitāte, un tā ir piektais biežākais kopējās hospitālās letalitātes cēlonis (HIP letalitātes statistikas dati gan bieži ir neprecīzi, jo nereti pie tās nepareizi pieskaita arī no pamatslimības mirušos).
- ASV ik gadu hospitālī iegūtā pneimonija skar aptuveni divus miljonus hospitalizēto pacientu un no tās nomirst ap 90000 cilvēku. ASV ik gadu HIP slimnieku ārstēšanai tērē vairāk par diviem miljardiem dolāru - ap 40000 dolāru vienam slimniekam (Latvijā šādi pētījumi nav veikti).
- HIP ārstēšanai izlieto 50% intensīvās terapijas nodaļās izmantoto antibiotiku.
- ASV slimnieks HIP dēļ vidēji slimnīcā pavada astoņas dienas ilgāk nekā citi pacienti.
Terminoloģija un HIP epidemioloģija
Pie pilnīgas pneimoniju klasifikācijas nekavēsimies, jo to autoru kolektīvs atspoguļoja publikācijā par sadzīvē iegūtām pneimonijām (Doctus, septembris 2007, 14-21).
Hospitālī iegūta pneimonija
HIP (hospital-acquired pneumonia - HAP) sākas 48 un vairāk stundas pēc iestāšanās slimnīcā un tā iestāšanās brīdī nebija inkubācijas periodā.
Ventilatorasociēta pneimonija (VAP)
VAP (ventilator-associated pneumonia) sākas 48-72 un vairāk stundas pēc trahejas intubācijas. Šajā definīcijā nav iekļauti daži smagas norises HIP pacienti, kam var būt nepieciešama trahejas intubācija un kuri ir jāārstē tāpat kā pacienti ar VAP. No visiem intubētajiem slimniekiem VAP skar 9-27%. Intensīvās terapijas nodaļā ap 90% VAP gadījumu sastop mākslīgās plaušu ventilācijas (MPV) laikā, kad VAP gadījumu skaits progresē šādi: pirmajās piecās MPV dienās - 3% dienā, piektajā līdz desmitajā MPV dienā - 2%, pēc tam 1% dienā.
VAP gadījumu skaitu bieži nosaka neprecīzi, ja, piemēram, pie VAP nepareizi pieskaita mehāniski ventilēto personu infekcijas traheobronhītu. Vai arī aprēķinātais VAP gadījumu skaits var būt divas reizes lielāks tad, ja apakšējo elpceļu sekrētu bakterioloģiskai izmeklēšanai lieto neprecīzo kvalitatīvo vai puskvantitatīvo metodi un nelieto precīzo mūsdienu kvantitatīvo bakterioloģisko metodi.
Vislabāk izpētīta ir tieši VAP, jo pacientam pēc trahejas intubācijas ir vieglāk pareizi paņemt izmeklējamo materiālu no apakšējiem elpceļiem kvantitatīviem mikrobioloģiskajiem un rezistences pētījumiem. Autoritātes uzskata, ka iegūtie VAP pacientu mikrobioloģiskie dati pārklājas un ir attiecināmi arī uz HIP un HCAP pacientiem, uzsverot riska faktoru nozīmi katra specifiska patogēna gadījumā.
Ir iegūti pārliecinoši dati, kas nosaka HIP/VAP ārstēšanas stratēģiju un prognozi:
- agrīnā HIP/VAP sākas pirmajās četrās hospitalizācijas dienās, tai ir daudz labāka prognoze, jo ir krietni lielāka varbūtība, ka to izraisa pret antibiotikām jutīgas baktērijas, tāpēc tās empīriskajai sākumterapijai var lietot ierobežota spektra antibiotikas;
- vēlīnā HIP/VAP sākas piektajā hospitalizācijas dienā un vēlāk; tai ir daudz sliktāka prognoze, jo pastāv krietni lielāka varbūtība, ka tās izraisītājas ir pret antibiotikām rezistentas un multirezistentas baktērijas, tāpēc empīriskajai sākumterapijai jālieto plaša spektra antibiotikas.
Ar veselības aprūpi saistīta pneimonija (HCAP)
HCAP (healthcare-associated pneumonia) iekļauj jebkuru pacientu, kurš ir hospitalizēts divas un vairāk dienas (līdz 90 dienām) no infekcijas sākuma, dzīvo veco ļaužu pansionātos vai ilgstošas aprūpes iestādēs, vai arī pacientus, kuri nesen (30 dienas pirms hospitalizācijas) ir saņēmuši antibakteriālu terapiju, ķīmijterapiju, brūces ārstēšanu vai apmeklē slimnīcu vai hemodialīzes centru.
Smagas norises hospitālī iegūtās pneimonijas definīcija
- HIP dēļ slimnieks ir jāpārved uz intensīvās terapijas nodaļu (ITN).
- Elpošanas mazspēja: lai slimniekam nodrošinātu O2 parciālo spiedienu arteriālajās asinīs (PaO2) > 90%, ir nepieciešamība veikt mākslīgo plaušu ventilāciju.
- Strauja negatīva procesa dinamika: plaušu rentgenogrammā vērojama strauja multilobāras vai destruktīvas pneimonijas attīstība.
- Smagas sepses pazīmes: hipotensija (arteriālais 4 h, oligūrija (diurēze
Etioloģija
- Visbiežāk (50-70%) HIP izraisa aerobās Gram negatīvās nūjiņas, kā Pseudomonas aeruginosa (17%), Klebsiella pneumoniae (7,5), Escherichia coli (6,5%), Serratia marcescens (5,5%) un Acinetobacter sugas (5%) - 1. tabula. P. aeruginosa infekcijas risku palielina ilgstoša atrašanās slimnīcā, īpaši intensīvās terapijas nodaļā, prednizolona vai citu glikokortikosteroīdu un antibiotiku lietošana, hroniskas plaušu slimības, AIDS, neitropēnija.
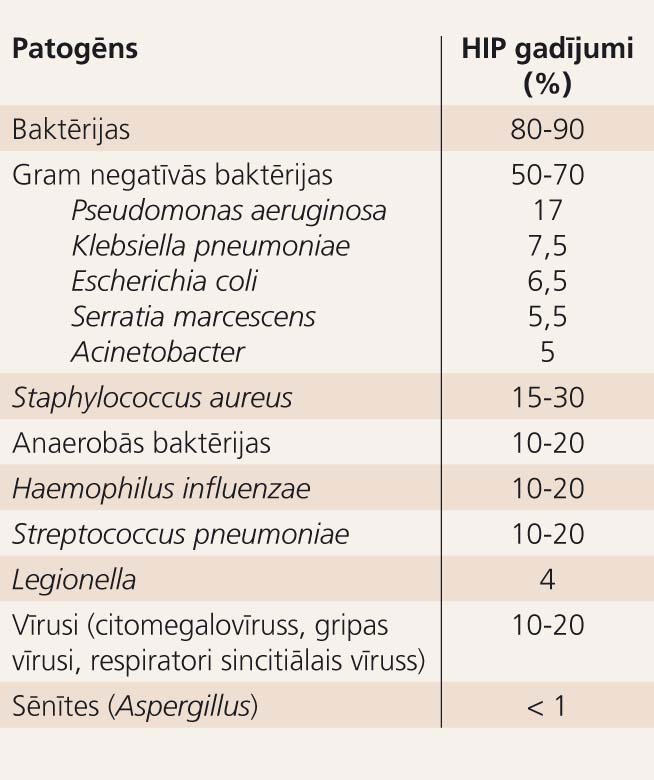

1. tabula
Hospitālī iegūtas pneimonijas biežākie izraisītāji
- Otrais biežākais HIP izraisītājs ir Staphylococcus aureus (15-30%). Visā pasaulē strauji pieaug meticilīnrezistento S.aureus (MRSA) celmu izplatība. S.aureus biežāk HIP izraisa cukura diabēta, komas, nesenas smagas gripas, galvas traumas un intensīvās terapijas nodaļā ievietotajiem slimniekiem.
- Anaerobās baktērijas, Haemophilus influenzae un Streptococcus pneumoniae katru izsēj ap 10-20% gadījumu. Anaerobās infekcijas risku palielina aspirācija un abdominālā ķirurģija. Anaerobo baktēriju izraisīta HIP pēc aspirācijas bieži attīstās neintubētiem pacientiem, bet ir reti sastopama slimniekiem ar VAP. Par anaerobo infekciju liecina krēpas ar izteiktu nepatīkamu (puvuma) smaku.
- Legionella sugas ir atbildīgas aptuveni par 4% HIP gadījumu. Legionella infekcijas risku palielina gaisa kondicionētāju lietošana, prednizolona vai citu glikokortikosteroīdu nozīmēšana. Dažkārt slimnīcā Legionella infekcija ir endēmiska vai epidēmiska un izplatās ar kontaminētu gaisa kondicionēšanas iekārtu, dušas vai karstā ūdens apgādes sistēmu starpniecību.
- Vīrusi ir HIP izraisītāji 10-20% gadījumu. Imūnkompetenti pieaugušie visbiežāk slimo ar A un B gripas vīrusu izraisītu primāru vai sekundāru pneimoniju. Imūnkompromitēti pieaugušie ar nomāktu celulāro imunitāti biežāk slimo ar citomegalovīrusu izraisītu pneimoniju. Retāk HIP izraisa adenovīrusi, RSV, VZV un HHV-6.
- Ir aprakstītas intrahospitālas multirezistentās tuberkulozes epidēmiski uzliesmojumi, kas skar arī medicīnas personālu. Sevišķi uzņēmīgas ir personas ar nomāktu celulāro imunitāti (piemēram, transplantāta recipienti, kas saņem imūnsupresorus, HIV/AIDS pacienti).
- Aspergillozes intrahospitāla izplatīšanās ir reta, tā biežāk skar personas ar nomāktu celulāro imunitāti un/vai neitropēniju.
- Polimikrobiskas mikrofloras izraisītas HIP biežums dažādos pētījumos ir ļoti variabls, bet īpaši augsts tas ir slimniekiem ar pieaugušo respiratoro distresa sindromu (ADRS - adult respiratory distress syndrome).
- Visā pasaulē strauji pieaug multirezistento (MR) HIP izraisītāju biežums. MR patogēnu izolēšanas biežums stipri atšķiras dažādās valstīs, slimnīcās, nodaļās, pacientu populācijās, kā arī mainās laika gaitā. Tāpēc katrā konkrētā slimnīcas nodaļā laiku pa laikam ir jānosaka MR patogēnu izplatības biežums. Šie dati dod iespēju nozīmēt efektīvāku empīrisko antibakteriālo terapiju un samazināt HIP/VAP/HCAP slimnieku mirstību.
Klīniskā aina, kritēriji un riska faktori
HIP parasti izpaužas ar drudzi, klepu ar strutainām krēpām, tahipnoju. Auskultējot konstatē bronhiālu elpošanu, plaušās dzirdami trokšņi. Asinsainā parasti ir leikocitoze ar novirzi pa kreisi, retāk leikopēnija.
HIP kritēriji ir sekojoši:
- krūšu kurvja rentgenogrammā redzama jauna infiltrāta parādīšanās plaušās;
- divas no šādām atradēm:
- ķermeņa temperatūra > 39,3o C;
- palielinās krēpu daudzums;
- skābekļa parciālais spiediens arteriālajās asinīs (PaO2)
- divas no sekojošām atradēm:
- tahipnoja, auskultējot bronhiāla elpošana, plaušās dzirdami trokšņi vai ir klepus;
- asinsainā ir leikopēnija (L 12 000/mm3) ar novirzi pa kreisi (stabiņkodolainie >10%);
- parādās strutainas krēpas (> 25 neitrofilajiem leikocītiem redzes laukā).
HIP riska faktori hospitalizētiem pacientiem atspoguļoti 2. tabulā. No tiem svarīgākais ir trahejas intubācija vai traheostomija, kas palielina saslimšanas risku ar HIP 7-21 reizi. Modificējamo riska faktoru maiņa būtiski samazina saslimstību ar hospitālī iegūto pneimoniju.


2. tabula
Hospitālī iegūtas pneimonijas riska faktori
3. tabulā parādīti multirezistentas HIP riska faktori.


3. tabula
Multirezistentas hospitālī iegūtas pneimonijas riska faktori
Hospitālī iegūtas pneimonijas patoģenēzes īpatnības
- Pneimonija attīstās tad, ja ir bojāts kāds no saimnieka elpceļu aizsardzības mehānismiem, elpceļos nonāk liels mikroorganismu daudzums vai arī mikroorganismi ir ļoti virulenti un saimniekam nav imunitātes pret tiem.
- HIP izraisītāju avots var būt ierīces, aparāti un priekšmeti, ko lieto pacienta ārstēšanai, ārējās vides elementi (gaiss, ūdens, slimnīcas iekārtas, mēbeles, veļa un citi priekšmeti), kā arī slimnīcas personāls vai citi pacienti.
- HIP attīstību visbiežāk nodrošina orofaringeālo patogēnu aspirācija un augšējo elpceļu sekrētu ieplūšana apakšējos elpceļos gar trahejas intubācijas cauruli tās intubācijas laikā. Ja intubācijas cauruli klāj inficēta bioplēve (biofilm), tad tā var inficēt apakšējos elpceļus. Šāds patoģenēzes mehānisms var būt svarīgs VAP gadījumā.
- Reti HIP attīstās pēc hematogēnas patogēnu nonākšanas plaušās no inficētiem intravenoziem katetriem, adatām un šļircēm.
- HIP attīstību stimulē apstākļi, kas veicina augšējo elpceļu vai kuņģa un zarnu trakta augšējās daļas virsnormas kolonizāciju ar Gram negatīvām nūjiņām. Šādu kolonizāciju veicina smagas slimības, īpaši plaušu, akūtas respiratoras vīrusu infekcijas, antibiotiku lietošana, ilgstoša atrašanās slimnīcā vai pansionātā, alkoholisms, cukura diabēts, azotēmija, neitropēnija, liels vecums, apziņas traucējumi, koma, novājēšana, trahejas intubācija vai traheostomija, nazogastrāla zonde, torakālā vai abdominālā ķirurģija.
Izmeklējumi
Plaušu rentgenogramma
Plaušu rentgenogrammu nepieciešams veikt ikvienam pacientam ar aizdomām par pneimoniju vai citu plaušu slimību. Tomēr nav ieteicams zīlēt ierosinātāju, pamatojoties tikai uz plaušu rentgenogrammu, jo plaušu pārmaiņas nav specifiskas. Aizēnojums plaušās ne vienmēr ir HIP. Atipiskas pneimonijas (mikoplazmu, hlamīdiju) gadījumā izmaiņas plaušu rentgenogrammā var būt arī minimālas vai pat pilnīgi nebūt.
Krēpu izmeklēšana
Bakterioloģiska un bakterioskopiska krēpu izmeklēšana dod pozitīvu rezultātu tikai 50-70% pacientu un izmaksā dārgi. Rezultātu interpretācija nav viennozīmīga, jo ir ierobežotas iespējas atšķirt mutes dobuma normālo no pneimoniju izraisošās mikrofloras. Krēpu analīžu galvenā nozīme ir konkrētu patogēno mikroorganismu izraisītu pneimoniju - tuberkulozes, leģionellozes, sēnīšu, Pneumocystis carinii - izslēgšanai (vairāk noliedzoša nekā apstiprinoša vērtība). Krēpu izmeklēšanu vīrusu noteikšanai veic ārkārtīgi reti, tādēļ ka tas ir dārgi, ilgi un darbietilpīgi.
Bronhoskopija
Bronhoskopija ir vērtīga, informatīva un ļoti nepieciešama VAP/HIP pacientu izmeklēšanas metode, ko veic pirms empīriskās antibakteriālās terapijas uzsākšanas, kā arī tās efektivitātes kontrolei. Bronhoskopija dod iespēju iegūt nekontaminētu apakšējo elpceļu sekrētu bakterioloģiskai izmeklēšanai.
Apakšējo elpceļu sekrētu paraugu kvantitatīva bakterioloģiska izmeklēšana
Ar PSB (analīžu ņemšanas birstītēm - protected specimen brush) un BAL (bronhoalveolārā lavāža) iegūto apakšējo elpceļu sekrētu bakterioloģiskai izmeklēšanai ļoti ieteicams lietot precīzo mūsdienu kvantitatīvo bakterioloģisko metodi. Šo materiālu kvantitatīva bakterioloģiska izmeklēšana dod iespēju precīzi noteikt HIP diagnozi un diferencēt to no plaušu neoplazmas, embolijas, atelektāzes, hemorāģijas, pieaugušo respiratorā distersa sindroma (ARDS). Ja ar BAL iegūtā apakšējo elpceļu sekrētā atrod > 104 kfv/ml vai ar PSB iegūtā paraugā > 103 kvf/ml, tad HIP diagnoze ir droša (kvf - kolonijas veidojošā vienība).
Ja, piemēram, apakšējo elpceļu sekrētu bakterioloģiskai izmeklēšanai lieto neprecīzo kvalitatīvo vai puskvantitatīvo metodi, tad var iegūt maldinošu bakterioloģisko informāciju, kas neļauj ārstam uzstādīt precīzu bakterioloģisko diagnozi, kā arī nozīmēt efektīvu antibakteriālo terapiju, tādējādi radot fatālu seku draudus.
HIP/VAP izraisītāju rezistences/jutības pret antimikrobiskajiem līdzekļiem noteikšana
Tā noteikti ir jāveic visiem HIP/VAP slimniekiem. Rezistence un multirezistence ir nelaime, kas strauji izplatās, un tā ir jāņem vērā, lai nozīmētā antibakteriālā terapija būtu adekvāta un maksimāli efektīva.
Hemokultūra
Ļoti vērtīga izmeklēšanas metode, ar kuru izdodas izolēt HIP izsaucēju ap 24-25% gadījumu.
Asinsaina
Izmantojama tikai kā indikators pacienta stāvokļa un hospitalizācijas nepieciešamības novērtēšanai.
Aknu raudzes un elektrolītu noteikšana
Šie izmeklējumi nespēj sniegt nekādu palīdzību empīriskās terapijas izvēlē vai slimības prognozē, tāpēc parasti nav indicēti.
Seroloģiskie izmeklējumi
Seroloģiskie izmeklējumi sniedz tikai retrospektīvus datus un ir noderīgi vienīgi epidemioloģiskiem mērķiem.
Torakocentēze
Torakocentēze jāveic visos gadījumos, kad ir ievērojams pleiras eksudāta daudzums. Eksudātā jānosaka etioloģiskais aģents (bakterioskopiski un bakterioloģiski) un tā rezistence/jutība pret antimikrobiskajiem līdzekļiem.
Autoru kolektīva publikācijā par sadzīvē iegūtām pneimonijām (Doctus, septembris, 2007, 21. lpp.) sniegts pārskats par pneimoniju izraisītāju atklšānas testiem.
Hospitālī iegūtas pneimonijas ārstēšana
Ja HIP norit viegli, to ārstē parastā slimnīcas nodaļā, savukārt smagi noritošu - intensīvās terapijas nodaļā.
Empīriskā antimikrobiskā sākumterapija
HIP empīriskā antimikrobiskā sākumterapija parādīta 4. tabulā.
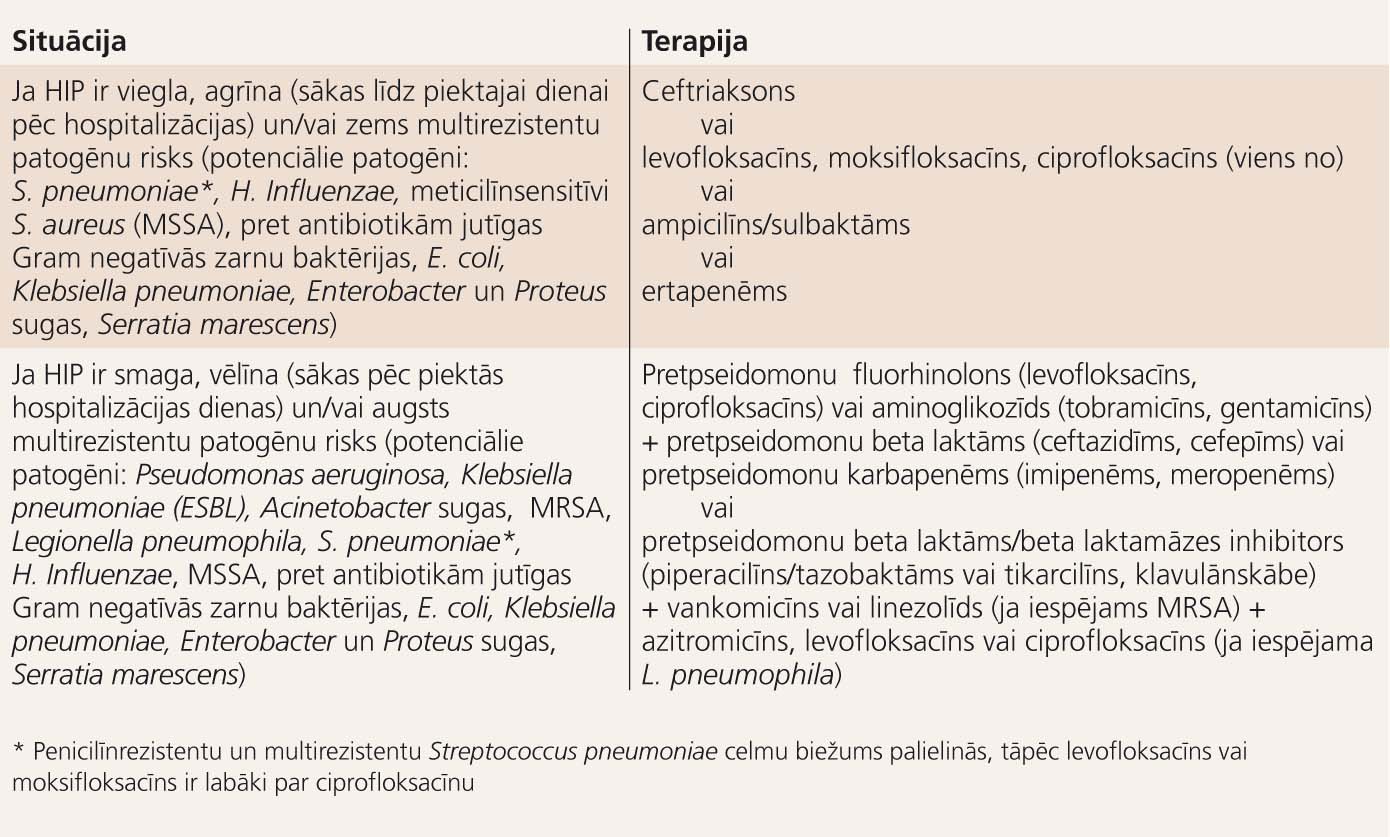

4. tabula
Hospitālī iegūtas pneimonijas iniciālā empīriskā antimikrobiskā terapija
- Ja HIP pacients pieder pie pirmās grupas (HIP ir viegla, agrīna un/vai ir zems multirezistentu patogēnu risks), nozīmē ierobežota spektra empīrisko antibakteriālo sākumterapiju, ja pie otrās grupas (HIP ir smaga, vēlīna un/vai ir augsts multirezistentu patogēnu risks) - nozīmē plaša spektra empīrisko antibakteriālo sākumterapiju.
- Antibakteriālo līdzekļu izvēle ir atkarīga arī no multirezistentu patogēnu izolēšanas biežuma katrā konkrētā slimnīcas nodaļā. Multirezistence stipri atšķiras dažādās valstīs, slimnīcās, nodaļās, pacientu populācijās, kā arī mainās laika gaitā. Tāpēc katrā konkrētā slimnīcas nodaļā laiku pa laikam ir jānosaka MR patogēnu izplatības biežums. Šie dati dod iespēju nozīmēt efektīvāku empīrisko antibakteriālo sākumterapiju un samazināt HIP/VAP/HCAP slimnieku mirstību. Ja šādi pētījumi nav izdarīti (kas Latvijā ir bieži sastopama nekārtība), tad jāņem vērā citu valstu (ASV, Vācijas, Zviedrijas) dati (5. tabula).
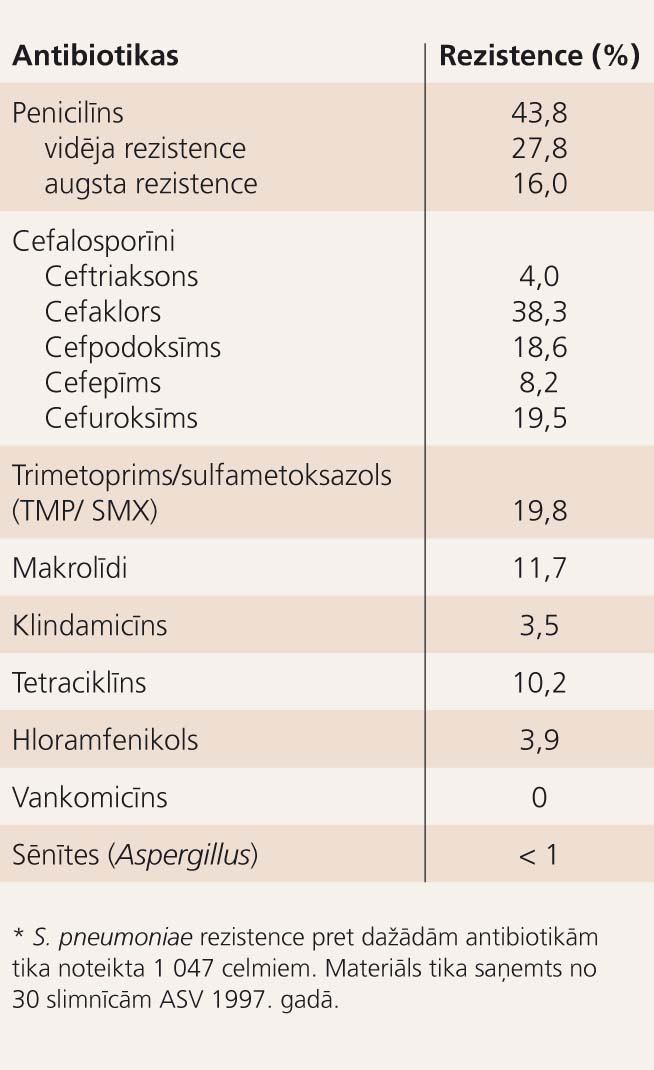

5. tabula
Streptococcus pneumoniae rezistence pret dažādām antibiotikām*
- Pacients, kam ir ar veselības aprūpi saistīta pneimonija (HCAP), ir jāārstē tāpat kā pie otrās grupas piederošs HIP pacients ar augstu multirezistentu patogēnu risku neatkarīgi no tā, kurā hospitalizācijas dienā HCAP sākusies - t. i., jānozīmē plaša spektra empīriska antibakteriālā sākumterapija.
- Ja pacients nesen ir lietojis antibiotikas, tad HIP ārstēšanai jāizvēlas citas grupas antibiotikas, jo ir liela rezistences varbūtība.
HIP pacienta adekvāta iniciālā empīriskā antibakteriālā terapija ir jāsāk nekavējoties. Kavēšanās paaugstina HIP slimnieku mirstību. Neadekvāta antibakteriālā terapija (HIP izsaucējs ir rezistents pret nozīmēto antibiotiku) ir galvenais riska faktors, kas paaugstina HIP pacientu ārstēšanās ilgumu un mirstību. Neadekvāta antibakteriālā terapija ir arī galvenais rezistences un multirezistences rašanās cēlonis.
Antimikrobiskā terapija,ja izraisītājs ir noskaidrots
HIP antimikrobiskā terapija, ja izraisītājs ir noskaidrots, atspoguļota 6. tabulā.
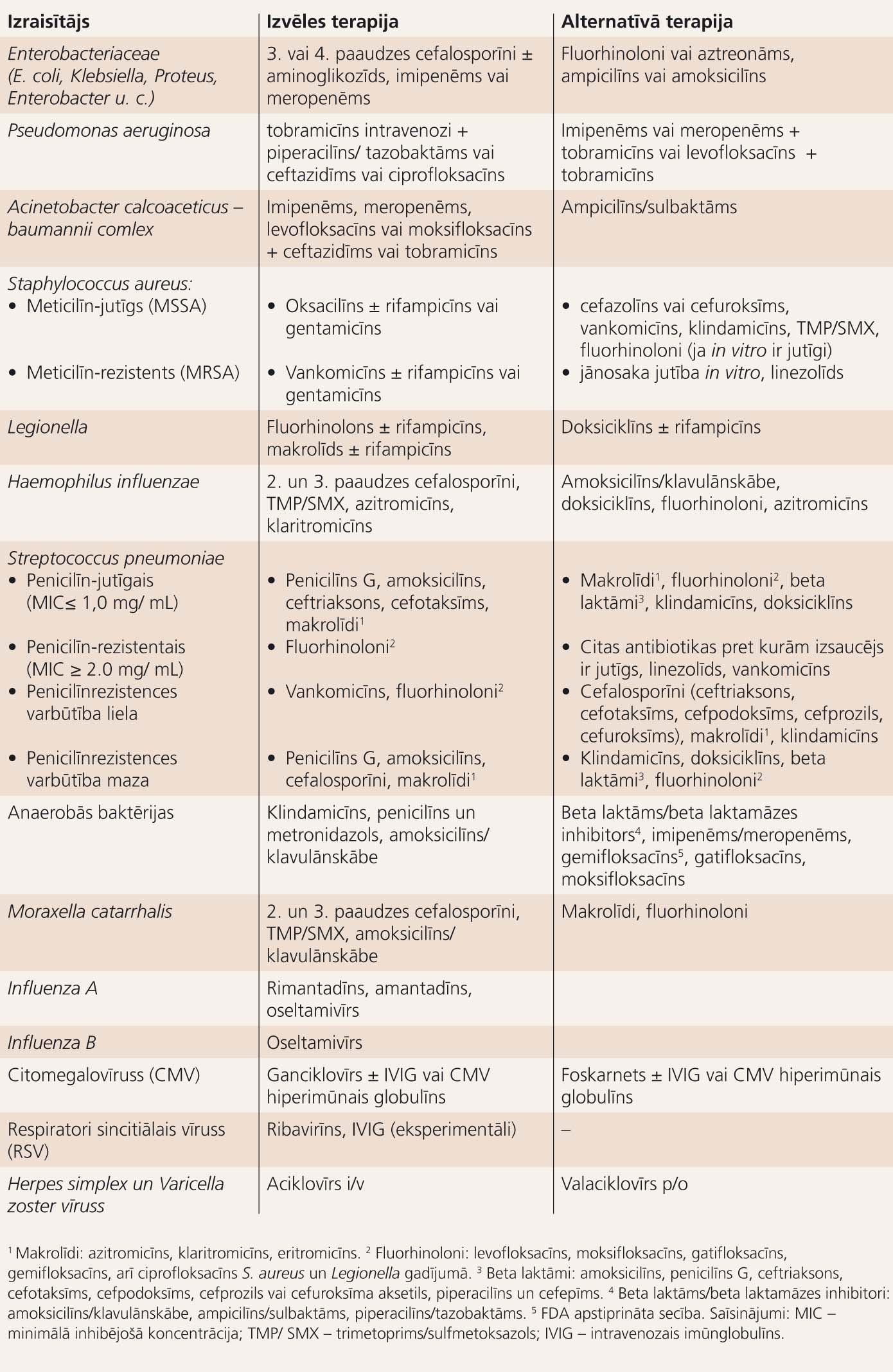

6. tabula
Hospitālī iegūtas pneimonijas antimikrobiskā terapija pieaugušajiem, ja izraisītājs ir zināms (ATS un IDSA 2005. gada rekomendācijas)
Pacientu ārstēšana, ja HIP izraisa multirezistenti patogēni
- Ja HIP izraisa P. aeruginosa, jānozīmē kombinēta antibakteriāla terapija, kas ir efektīvāka un retāk attīstās multirezistence.
- Acinetobacter gadījumā visaktīvākie ir imipenēms, meropenēms, kolistīns un polimiksīns. Kombinēta antibakteriālā terapija šajā gadījumā nav efektīvāka.
- Ja izsēj plaša spektra beta laktamāzes producējošus Enterobacteriaceae (extended spectrum beta-lactamase producing) sugas, nozīmē imipenēmu vai meropenēmu, kas ir aktīvāki par trešās paaudzes cefalosporīniem.
- Ja HIP/VAP izraisa meticilīnrezistents S. aureus (MRSA), tad vankomicīns ir izvēles antibiotika, bet linezolīds - laba alternatīva.
Optimālas antibakteriālās terapijas nosacījumi
- Lai nodrošinātu maksimāli efektīvu smagi noritošas HIP vai VAP ārstēšanu, jālieto optimālas antibiotiku devas.
- Iniciālā empīriskā antibakteriālā terapija visiem HIP pacientiem jāsāk ar intravenozu antibiotiku ievadīšanu. Ja pacientam ir laba klīniskā atbildes reakcija un nav kuņģa un zarnu trakta darbības traucējumu, tad var pāriet uz perorālu terapiju - uz fluorhinolonu un linezolīda perorālu terapiju, jo tie ļoti labi uzsūcas no kuņģa-zarnu trakta.
- Antibiotiku ievadīšana elpceļos aerosola veidā neuzlabo ārstēšanas efektivitāti, bet var izraisīt bīstamas alerģiskas reakcijas.
- Ja ir iespējams, ka pacients inficējies ar multirezistentu patogēnu, jānozīmē kombinēta antibakteriālā terapija.
- Ja pacients saņem kombinētu antibakteriālu terapiju, kurā ir iekļauts aminoglikozīds, tad pacientam ar labu klīnisko atbildes reakciju to ievadīšanu var pārtraukt pēc piecām līdz septiņām dienām.
- Monoterapiju var nozīmēt pacientiem ar smagu HIP/VAP, ja to nav izraisījis multirezistents patogēns. Šīs grupas pacientiem sākumā līdz bakterioloģisko analīžu un rezitences noteikšanas rezultātu noskaidrošanai, kas apstiprina, ka patogēns nav multirezistents, ir jāsaņem kombinēta antibakteriāla terapija.
- Ja iniciālā kombinētā antibakteriālā terapija ir efektīva, par ko liecina laba klīniskā atbildes reakcija trīs dienu laikā, un ir pārliecība, ka izsaucējs nav P. aeruginosa, tad jācenšas saīsināt ārstēšanas kurss no tradicionālās 14-21 līdz septiņām dienām.
Slimnieka atbildes reakcija uz ārstēšanu
Slimnieka atbildes reakciju uz ārstēšanu var ietekmēt šādi faktori:
- pacienta faktori: blakusslimības, vecums, komplikācijas;
- HIP izraisītāja faktori: antimikrobiskā rezistence, virulence;
- ārstējošā ārsta faktori: kļūda diagnozes, izsaucēja un/vai tā rezistences noteikšanā, nozīmēta neadekvāta antimikrobiskā terapija.
HIP iespējamo izraisītāju spektrs ir ļoti plašs, tāpēc visas iespējamās variācijas empīriskā antimikrobiskā sākumterapija nevar noklāt:
- pēc HIP/VAP izraisītāja izsēšanas no asinīm vai elpceļu sekrētiem un tā rezistences/jutības pret antimikrobiskajiem līdzekļiem noteikšanas empīriskā antimikrobiskā terapija, ja nepieciešams, ir jāmodificē; īpaši aktuāli tas ir gadījumos, kad HIP slimniekam ar sliktu atbildes reakciju izolētais izsaucējs ir neparedzēts, rezistents vai reti sastopams;
- jānozīmē šaurāka spektra antibiotikas, ja izrādās, ka HIP izsaucējs nav kā sākumā prognozēts rezistents MRSA, P. aeruginosa vai Acinetobacter, bet ir mazāk virulents un jutīgs pret šaurāka spektra antibiotikām.
Atbildes reakcijas uz ārstēšanu novērtēšanas rekomendācijas
- Atbildes reakciju uz empīrisko antibakteriālo sākumterapiju novērtē, nosakot dinamikā vienkāršus klīniskos parametrus - ķermeņa temperatūru, leikocītu skaitu un oksigenizāciju -, kā arī bakterioloģiskās izmeklēšanas rezultātus. Balstoties uz šo izmeklējumu rezultātu dinamikas rādītājiem, ja nepieciešams, atbilstoši izmaina empīrisko antibakteriālo terapiju.
- Adekvātas terapijas gadījumos klīniska uzlabošanās ir samanāma pēc 48-72 stundām. Ja slimnieka stāvoklis nepasliktinās, pirmajās trijās ārstēšanas dienās empīrisko antibakteriālo terapiju mainīt nevajag.
- Ja slimnieka atbildes reakcija uz antimikrobisko terapiju ir laba, tad, ņemot vērā arī bakterioloģiskās izmeklēšanas rezultātus, var sašaurināt empīriskās antibakteriālās terapijas spektru un nozīmēt ierobežota spektra antibiotikas.
- Ja slimnieka atbildes reakcija uz antibakteriālo terapiju ir slikta (nerespondents), tad rūpīgi jāizvērtē tās iespējamie cēloņi (attēls):

Attēls
Slimnieka atbildes reakcija uz ārstēšanu: ne-respondentu novērtēšana
- nepareizi noteikta diagnoze un īstenībā slimniekam ir M. tuberculosis, trombembolija, atelektāze, neoplazma vai hemorāģija;
- kļūda izsaucēja noteikšanā vai ir rezistents HIP izraisītājs - baktērija, M. tuberculosis, vīruss, sēnīte;
- komplikācijas, tādas kā empiēma vai plaušas abscess, okulta infekcija, zāļu drudzis vai Clostridium difficile kolīts.
Lai operatīvi atklātu šos un citus neveiksmīgas antimikrobiskās terapijas cēloņus, slimnieks enerģiski jāizmeklē papildus.
HIP dinamikas novērtējums
Parasti HIP dinamikas novērtēšanai lieto vienkāršus klīniskos parametrus - ķermeņa temperatūras, leikocītu skaita un oksigenizācijas daudzkārtēju noteikšanu. Ja HIP slimnieka antimikrobiskā terapija ir adekvāta, tad šie rādītāji trīs līdz septiņu dienu laikā progresīvi uzlabojas.
HIP pacienta izveseļošanās gaitu novērē klīniski un/vai mikrobioloģiski.
- Klīniski izveseļošanās gaitu novērtē kā uzlabošanos, aizkavētu uzlabošanos, recidīvu, ārstēšanas neveiksmi un slimnieka nāvi.
- Mikrobioloģiski izveseļošanās gaitu novērtē atkarībā no pēc 72 stundām atkārtotā bronhoskopijā ar PBS vai BAL iegūto apakšējo elpceļu sekrētu kvantitatīvas bakterioloģiskas izmeklēšanas, formulējot kā: izsaucēja izskaušana, superinfekcija ar citu mikroorganismu, recidīvs (pēc eliminācijas atgriežas sākotnējais izsaucējs) vai izraisītāja persistence.
- Ja HIP pacienta PSB parauga analīze liecina, ka aug mazāk baktēriju par 103 kvf/ml, tad izveseļojas ap 93% slimnieku.
- Ja PSB paraugā aug vairāk baktēriju par 103 kvf/ml - izveseļojas tikai ap 44% slimnieku.
Krūšu kurvja rentgenogramma ar novēlošanos un nepietiekami adekvāti atspoguļo smagas HIP dinamiku, īpaši slimniekiem ar hroniskām plaušu slimībām. Ja 48 stundās aizēnojums palielinās vairāk nekā par 50% un kļūst multilobārs, tad bieži attīstās destrukcija vai liels izsvīdums pleiras dobumā.
Hospitālī iegūtas pneimonijas profilakse
HIP profilakse parādīta 7. tabulā.


7. tabula
Hospitālī iegūtās pneimonijas profilakse
Ne mazāk svarīgi ir nodrošināt adekvātu blakusslimību ārstēšanu un visaptverošu HIP pacienta aprūpi (kopšanu, ēdināšanu, bronholītisko un mukolītisko līdzekļu inhalācijas, citus atveseļošanās pasākumus).