Balsta—kustību aparāta slimības ir slimību grupa, kuru ārstēšanā ļoti bieži nepieciešami dažādi rehabilitācijas pasākumi. Ceļa locītavas osteoartrīts (OA) ir viens no galvenajiem senioru darbspēju ierobežotājiem un bieža problēma šajā vecuma kategorijā kopumā.
Ultrasonogrāfiskas atrades ceļa osteoartrīta pacientiem: perspektīvs novērošanas šķērsgriezuma pētījums
AVOTS: Abicalaf, C. A. R. P. et al. (2021) ‘Ultrasonography findings in knee osteoarthritis: a prospective observational cross-sectional study of 100 patients’, Scientific reports, 11(1), p. 16589. doi: 10.1038/s41598-021-95419-3.
Ceļa locītavas OA ir 11. vietā pasaulē no iemesliem, kas izraisa invaliditāti, un attiecināms uz kopumā 2,2 % dzīves gadu, kas pavadīti darbnespējā. Šobrīd nav neviena specifiska slimību modificējoša pasākuma, lai gan locītavas bojājuma patofizioloģija izprasta molekulārā līmenī. Starp citu, ir pierādīta ļoti zema korelācija starp locītavas audu bojājumu un sāpju intensitāti. Ap 10 % pacientu ar smagām sāpēm ceļgalos ir normāls Rtg izmeklējums.
Vairāki autori jau identificējuši intraartikulāru vai periartikulāru (saites, cīpslas, locītavas somiņas) bojājumu pacientiem ar sim-
ptomātisku OA — galvenās izmaiņas ceļa locītavas USG ir locītavas efūzija, popliteālas cistas un tendinopātijas.
Pētījuma mērķis bija aprakstīt pamata izmaiņas ceļa locītavas USG simptomātiskiem pacientiem ar primāru ceļa locītavas OA, kā arī korelēt USG izmaiņu skaitu un Rtg atrades smaguma pakāpi, lietojot Kellgren and Lawrence radioloģiskos rādītājus, un noteikt, vai ir nozīmīga korelācija starp izmaiņām USG un sāpju intensitātē, kas mērīta pēc VAS skalas un funkcionālajiem testiem (TUG, WOMAC).
Materiāli un metodes
Perspektīvā novērošanas šķērsgriezuma pētījumā bez kontroles grupas tika iekļauti simt pacienti ar primāru simptomātisku OA (194 ceļgali) pēc atbilsmes šādiem kritērijiem: vecums > 50 gadi, klīniska un radioloģiska OA diagnoze, sūdzības par augstas vai vidēji augstas pakāpes sāpēm (VAS virs 4), sāpes ir vismaz trīs mēnešus, fonā nav nevienas nopietnas psihiatriskas blakusslimības, nav fibromialģijas, sistēmisku iekaisīgu reimatoloģisku slimību, anamnēzē nav neoplazmu vai sāpju citās locītavās.
Pacienti tika izmeklēti radioloģiski: Rtg AP projekcijā un USG ceļa locītavai. Ceļa locītavas tūska jeb efūzija tika apstiprināta, ja locītavas šķidrums bija vairāk nekā 4 mm, vizualizēts kā hipogēns vai anehogēns saturs ceļa locītavas dobumā.
Rezultāti
Visbiežākās izmaiņas ceļa locītavās bija locītavas efūzija, pes anserinus bursīts, kvadricepsa cīpslu entezopātija, paceles cistas, iliotibiālās saites tendinīts un ceļa skriemeļa tendinīts. Pīrsona korelācijas analīze uzrādīja vērā ņemamu vidēji pozitīvu asociāciju starp VAS rezultātu un USG atražu skaitu (r = 0,36; p < 0,0001). USG atražu skaits atšķīrās starp Kellgren and Lawrence I un III pakāpi (p = 0,041), I un IV pakāpi (p < 0,001), II un IV pakāpi (p = 0,001, variāciju analīze veikta ar Bonferroni korekcijas metodi).
Bija vērā ņemama asociācija starp USG atražu skaitu un rezultātiem funkcionālajos testos — TUG (r = 0,16; p < 0,028) un WOMAC (r = 0,16; p < 0,029) — un fiziskās funkcionalitātes domēniem (r = 0,16; p < 0,028). Visbiežāk konstatētā izmaiņa no normas USG bija locītavas efūzija. Periartikulārās struktūras varētu būt potenciāli saistītas ar sāpju un darbnespējas cēloni.
Doc. A. Mihailova: “USG izmeklējumi ļoti palīdz ikdienas praksē, lai diagnosticētu, novērtētu un arī pamatoti ārstētu. Tomēr šādi iegūtie dati rūpīgi jāanalizē. Piemēram, izmeklējumā redzot osteofītus, varam to uzskatīt par pārliecinošu OA pazīmi. Savukārt palielināts šķidruma daudzums ir atrade, kas jāizvērtē kritiski, piemērojot visus iemeslus, kas var radīt šķidruma krāšanos locītavā. Artrīts pacientam var kombinēties, tāpēc ne vienmēr, ieraugot šķidrumu ceļa locītavā, varam teikt, ka ir OA.
Meniska bojājums var radīt iekaisumu un šķidruma krāšanos. Skrējējiem uzreiz pēc slodzes ceļa locītavā arī mēdz veidoties šķidrums. Tomēr neviens no šiem gadījumi neliecina par OA.
Savukārt Beikera cista, kas parasti veidojas ceļa locītavas aizmugurē, ir netiešs hroniska sinovīta simptoms, kas var liecināt par OA. Ja izmeklējumā redzami arī osteofīti, samērā droši var izvirzīt OA diagnozi. Publikācijā minētās izmaiņas cīpslās liecina par pārslodzi. Arī pārslodze ir viens no iemesliem OA attīstībai.”
ESCEO un OARSI rekomendāciju salīdzinājums neķirurģiskai ceļa osteoartrīta pārvaldībai
AVOTS: Arden NK, Perry TA, Bannuru RR, Bruyère O, Cooper C, Haugen IK, Hochberg MC, McAlindon TE, Mobasheri A, Reginster JY. Non-surgical management of knee osteoarthritis: comparison of ESCEO and OARSI 2019 guidelines. Nat Rev Rheumatol. 2021 Jan;17(1):59-66. doi: 10.1038/s41584-020-00523-9. Epub 2020 Oct 28. PMID: 33116279.
Osteoartrītu, kas ir viena no biežākajām hroniskajām locītavu slimībām, raksturo lokāls locītavas iekaisums un strukturālas izmaiņas, kas pacientam sagādā sāpes un ikdienas funkcionalitātes zudumu, pasliktina dzīves kvalitāti. Vieni no līderiem darbnespējas izraisīšanā ir gūžas un ceļa locītavas OA.
OA pārvaldības rekomendācijas parasti izdala nefarmakoloģiskas, farmakoloģiskas un ķirurģiskas metodes vai arī kategorizē pēc slimības smaguma pakāpes un skartās locītavas. Citi rekomendāciju varianti ietver pieeju, kas centrēta uz pacientu, ģeogrāfisku skatījumu. Taču rekomendāciju varianti un literatūras dažādība speciālistiem rada apjukumu.
Tomēr lielākajā daļā vadlīniju par ceļa locītavas OA apstiprināti galvenie terapijas principi: pacienta izglītošana, ārstnieciskā vingrošana un svara zaudēšana. Ārstēšana parasti notiek ar analgētiķiem, NSPL, intraartikulārām kortikosteroīdu injekcijām. Smagākos gadījumos rekomendē locītavas protezēšanu.
2019. gadā gan OARSI (Osteoarthritis Research Society International), gan ESCEO (European Society for Clinical and Economic Aspects of Osteoporosis, Osteoarthritis and Musculoskeletal Diseases) atjaunoja rekomendācijas neķirurģiskai ceļa locītavas OA pārvaldībai. Aplūkotajā publikācijā izsvērts līdzīgais un atšķirīgais šajās rekomendācijas.
Rekomendāciju salīdzinājums
Līdzīgais
Gan OARSI, gan ESCEO rekomendē ārstēšanas taktiku pa soļiem un sāk ar pacienta izglītošanu, fiziskām aktivitātēm un svara mazināšanu (adipozam pacientam). Tikai pēc tam jāpiemēro pirmās un otrās līnijas metodes (attēls). ESCEO iesaka aerobos un spēka/pretestības vingrinājumus, OARSI — strukturētus spēka, kardiovaskulāro veselību uzlabojošus, līdzsvara un neiromuskulārus vingrinājumus, dažādus prāta—ķermeņa vingrinājumus (taiči, jogu u.c.).
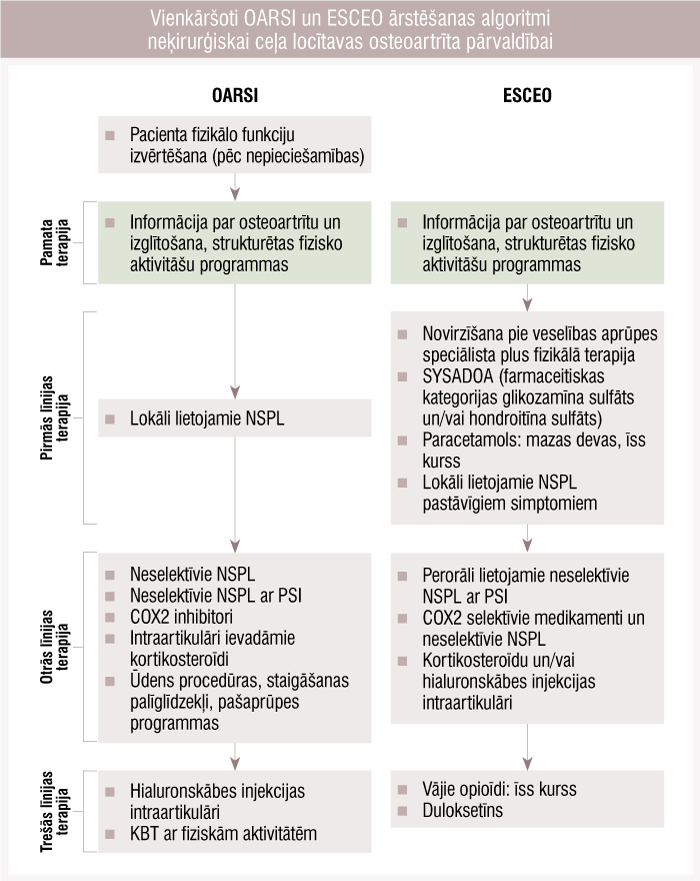

Attēls
Vienkāršoti OARSI un ESCEO ārstēšanas algoritmi neķirurģiskai ceļa locītavas osteoartrīta pārvaldībai
Kā pirmās izvēles līdzekļus gan OARSI, gan ESCEO iesaka lokāli lietojamos NSPL, ņemot vērā zemos kuņģa—zarnu trakta, kardiovaskulāros un nieru blakņu rādītājus. Abās vadlīnijās norādīts, ka paracetamola lietošana ilgtermiņā nebūtu rekomendējama kā pirmā izvēle.
Rekomendāciju sadaļā pastāvīgiem simptomiem kā otrās pakāpes terapiju abas institūcijas rekomendē per os lietot NSPL, kas pielāgots pacienta kardiovaskulārās un kuņģa—zarnu trakta veselības profilam. NSPL jālieto iespējami īsāko periodu iespējami mazākajā devā. Kuņģa—zarnu trakta aizsardzībai rekomendē NSPL lietot protonu sūkņu inhibitoru aizsegā vai arī lietot selektīvos COX2 inhibitorus.
Abās vadlīnijās atbalstītas intraartikulāras injekcijas ar kortikosteroīdiem, bet norādīts, ka to efektivitāte ticamāk būs īstermiņa, nevis ilgtermiņa. Arī intraartikulāras injekcijas ar hialuronskābi rekomendētas abās vadlīnijās, piemēram, ja nav palīdzējuši ne lokāli, ne perorāli lietoti NSPL (ieskaitot COX2 inhibitorus) vai ja ir kontrindikācijas NSPL lietošanai.
Atšķirības
Jau minēts, ka abās vadlīnijās kā pirmās izvēles līdzekļi minēti lokāli lietojamie NSPL. OARSI rekomendē to lietošanu pilnīgi visiem pacientiem, izņemot tiem, kam ir hroniskas sāpes vairākās ķermeņa daļās. ESCEO vadlīnijas iesaka: ja sāpes turpinās pēc īstermiņa glābjošas analgēzijas ar paracetamolu (devā, kas nepārsniedz 3 g dienā), izmantojamas arī lēnas darbības zāles OA ārstēšanā (SYSADOA), kas ir mikrokristālu glikozamīna sulfāts un hondroitīna sulfāts, un fizikālā terapija.
ESCEO vadlīnijas sniedz rekomendācijas par SYSADOA lietošanu: stingras rekomendācijas par mikrokristālu glikozamīnu un hondroitīnu un vājas rekomendācijas par nepārziepojama avokado un sojas pupiņu eļļas un diacerīna lietošanu. Ja ESCEO izdala mikrokristālu formas no pārējām un izsaka labvēlīgu rekomendāciju par pirmajām, tad OARSI šādu dalījumu neveic un nerekomendē SYSADOA.
Kā pēdējās farmakoloģiskās intervences abās vadlīnijās minēti antidepresanti: duloksetīns varētu būt lietderīgs pacientiem ar centrālu sāpju sensibilizāciju, taču OARSI par tā indicēšanu izsakās nedaudz piesardzīgāk, uzsverot tā drošumu tikai pacientiem ar plašām sāpēm un depresiju. ESCEO atbalsta arī opioīdu (piemēram, tramadola) lietošanu īstermiņā.
Secinājumi
Atšķirības ārstēšanas rekomendācijās skaidrojamas ar pētījumu analīzes metodoloģiskajām atšķirībām. Lai gan analizēti līdzīgi dati, abas speciālistu grupas izteikušas atšķirīgas rekomendācijas, pieļaujot, ka vēl aizvien ir jautājumi un neskaidrības par OA pārvaldību. Viens no risinājumiem — veidojot vadlīnijas, sadarboties gan starptautiskā, gan vietējā līmenī, lai nonāktu pie viena konsensus visiem.
Doc. A. Mihailova: “OA ir slimība, kas ārstējama praktiski tikai simptomātiski. Turklāt jāpatur prātā, ka pēc būtības tas ir vilciens, kas dodas vienā virzienā — uz locītavas endoprotezēšanu. Protams, vislabāk tajā “vilcienā” neiesēsties, bet vismaz braukt lēnam. Vesela cilvēka uzdevums ir rūpēties par normālas ķermeņa masas uzturēšanu un regulārām, nepārspīlētām fiziskām aktivitātēm, jo tā ir pietiekami efektīva profilakse, lai neattīstītos OA. Tomēr, ja OA attīstījies, abi šie pamatprincipi ir izšķirīgi arī slimības gadījumā.
Viena no veiksmīgākajām izvēlēm OA pacientu fiziskās aktivitātes uzturēšanai ir ārstnieciskā vingrošana, jo visas muskuļu grupas tiek nodarbinātas saudzīgi. Šai vingrošanai jākļūst par daļu no turpmākās dzīves.
Kursu veidā tai nav jēgas. Labi trenēti muskuļi atslogo locītavas, kas ir neatsverams ieguvums dzīvei bez sāpēm. Piemēram, pētījumā par sievietēm pēc 50 gadu vecuma ar diagnosticētu ceļa locītavas OA, tām pētījuma dalībniecēm, kam bija trenēti un stipri augšstilba muskuļi, endoprotezēšanu bija iespējams attālināt pat vairākus gadus. Vienīgi OA pacienta fiziskajām aktivitātēm jābūt saudzīgām, jo pārmērīga slodze tikai veicinās artrīta attīstību. OA pacienti bieži sūdzas par sāpēm dienas beigās. Šīs sāpes galvenokārt liecina par OA progresēšanu, bet arī par pārmērīgu slodzi — vai nu ķermeņa masa joprojām ir par lielu, vai arī fiziskās aktivitātes dienas garumā bijušas pārāk intensīvas. Piemēram, ja pacients stāsta, ka pastaigā noiet 8000 soļus, bet vakarā jūt sāpes, tad efektīvāk būtu šo pastaigu dalīt vai nedaudz saīsināt distanci, lai dienas beigās nesāpētu. Nereti pacienti paši meklē bezrecepšu līdzekļus sāpju mazināšanai — dažādas ziedes un uztura bagātinātājus: glikozamīnus, hondroitīnus un citus. Ja vien tas palīdz — lieliski. Turklāt ir pētījumi, kas liecina, ka glikozamīna un hondroitīna lietošana var mazināt sāpes, neietekmējot skrimšļa stāvokli. Tomēr vairākums pacientu tomēr ir spiesti lietot pretsāpju, pretiekaisuma zāles. OA pacientam būtiski apzināties, ka medikamenti palīdz vienīgi izvairīties no sāpēm, bet jācenšas nepieļaut sāpes. Lai reāli uzlabotu stāvokli, ir jāmaina dzīvesveids, galveno uzmanību veltot uztura un kustību samērīgumam.”
Vai vieglas pakāpes ceļa locītavas osteoartrīta gadījumā vajadzīga pilna ceļa locītavas artroplastika?
AVOTS: Leppänen, S. et al. (2021) ‘Mild knee osteoarthritis predicts dissatisfaction after total knee arthroplasty: a prospective study of 186 patients aged 65 years or less with 2-year follow-up’, BMC musculoskeletal disorders, 22(1), p. 657. doi: 10.1186/s12891-021-04543-8.
Ceļa locītavas artroplastika tiek veikta arvien biežāk, īpaši jauniem pacientiem darbspējīgā vecumā. Tomēr neapmierinātību ar iznākumu viņi izsaka biežāk nekā seniori, kam veikta artroplastika.
Pētījuma mērķis bija novērtēt neapmierinātības rādītājus un pastāvīgas sāpes pēc totālas ceļa locītavas artroplastikas un izvērtēt iznākumu paredzošos faktorus.
Materiāli un metodes
Perspektīvā novērošanas pētījumā ar apsekošanu divus gadus tika iekļauti 186 pacienti (ne vairāk kā 65 gadus veci), kuriem veikta unilaterāla totāla ceļa locītavas artroplastika. Iznākuma izvērtēšanai, lai noteiktu apmierinātību un pastāvīgas sāpes miera periodā vai fiziskas aktivitātes laikā, tika izmantotas vizuālo analogu skalas.
Vērā ņēma arī saistību ar pacienta demogrāfiskajiem rādītājiem, radiogrāfisko atradi, pacienta ziņoto iznākumu mērījumiem (PROM), neapmierinātību un pastāvīgām sāpēm un pārbaudīja ar vienvarianta loģistiskās regresijas analīzi.
Vieglas pakāpes OA tika definēts pēc nosacījumiem Kellgren and Lawrence II pakāpei, smags OA — Kellgren and Lawrence III un IV pakāpei. Lai pārbaudītu statistiski nozīmīgas saistības, pētnieki izmantoja daudzkārtīgo loģistiskās regresijas analīzi.
Rezultāti
Pēc diviem gadiem neapmierināti ar operācijas iznākumu bija 12 % pacientu (n = 23), par pastāvīgām sāpēm fiziskas slodzes laikā ziņoja 27 % (n = 50), miera stāvoklī — 10 % (n = 18).
Pacienti ar vieglas pakāpes OA ievērojami biežāk (p = 0,003) bija neapmierināti (28,6 %) ar iznākumu nekā pacienti ar smagas gaitas OA (8,7 %). Jaunākiem pacientiem bija lielāks risks būt neapmierinātiem un lielāka varbūtība, ka attīstīsies pastāvīgas sāpes.
Secinājumi
Vieglas pakāpes radioloģiski noteikts OA ir galvenais faktors, kāpēc pacients pēc totālas ceļa locītavas artroplastikas būs neapmierināts ar iznākumu. Tāpēc artroplastikas veikšana šai pacientu grupai ir nopietni apsverams jautājums.
Šie pacienti jāinformē par paaugstinātu neapmierinātības risku. Līdzīgi ir jaunākiem pacientiem — arī šai grupai ir augstāki neapmierinātības riski. Interesanti — ja totālu ceļa locītavas artroplastiku veic pacientiem ar smagāku OA, apmierinātības rādītāji šķiet augstāki, nekā iepriekš ziņots citos pētījumos.
Doc. A. Mihailova: “Lai endoprotezētu ceļa locītavu, jābūt ļoti nopietnām indikācijām: ievērojamai nodiluma pakāpei, funkcionāliem ierobežojumiem ar izmainītu kustības apjomu (piemēram, pacients nevar iztaisnot kāju), izmainītai ekstremitātes asij, sāpēm, ko grūti kupēt ar pretsāpju, pretiekaisuma līdzekļiem. Ceļa locītavai ir ļoti sarežģīta biomehānika: endoprotezējot šo locītavu, arī pēc operācijas saglabāsies gan funkcionālo spēju ierobežojumi, gan arī disciplinārie ierobežojumi. Cilvēks varēs kāpt pa kāpnēm, saliekt celi līdz 120 grādu leņķim, bet nevarēs veikt kustības ar ceļa locītavas rotāciju, nevarēs pilnībā pietupties — pēc būtības nedrīkst pat mēģināt to kustību izstrādāt. Šādi ierobežojumi var būt ļoti neērti. Tāpēc saprotams, ka cilvēki ar ne smagu OA biežāk nav apmierināti ar ceļa locītavas endoprotezēšanas rezultātu.
Pacienti, kam ir smags OA, locītavas endoprotezēšanu izvēlas tad, kad viņiem ilgstoši bijis grūti sadzīvot ar sāpēm un diskomfortu. Šādos apstākļos pacients ļoti novērtē to, ka pēc operācijas vairs nesāp, var pietiekami brīvi kustēties.
Jo sliktāk cilvēks juties līdz operācijai, jo vairāk izbaudīs uzlabojumus pēc ceļa locītavas endoprotezēšanas. Bet jaunam OA pacientam bez nopietnām sūdzībām šādi uzlabojumi var šķist nebūtiski un dzīvi ierobežojoši. Gados jaunam OA pacientam vajadzētu maksimāli censties attālināt ceļa locītavas endoprotezēšanu. Interesanti — pilnīgi cita situācija ir ar gūžas locītavas endoprotezēšanu. Jāteic gan, ka šīs locītavas biomehānika atšķiras, bet pēc gūžas locītavas endoprotezēšanas cilvēks var atgriezties sportā un visās ikdienas dzīves aktivitātēs bez jebkādiem funkcionāliem ierobežojumiem.”
Fiksētas kombinētas intraartikulāras injekcijas vai hialuronskābe monoterapijā
AVOTS: Stagni, C. et al. (2021) ‘Randomised, double-blind comparison of a fixed co-formulation of intra-articular polynucleotides and hyaluronic acid versus hyaluronic acid alone in the treatment of knee osteoarthritis: two-year follow-up’, BMC musculoskeletal disorders, 22(1), p. 773. doi: 10.1186/s12891-021-04648-0.
Pirmā gada starpposma divu gadu pētījuma analīzē tika pieņemts, ka pacientiem ar OA intraartikulāras injekcijas ar augsti attīrītu, dabiskas izcelsmes polinukleotīdu un hialuronskābi fiksētā kombinācijā (PNHA) varētu uzlabot ceļa locītavas funkciju un mazināt locītavas sāpes efektīvāk nekā hialuronskābe (HA) monoterapijā. Šīs otrā gada analīzes apraksta vai pirmās analīzes iznākumi saglabājas visā divu gadu novērošanas periodā.
Materiāli un metodes
Nejaušinātā, divkārt maskētā, ar HA kontrolētā klīniskā pētījumā specializētā terciārās aprūpes klīnikā piedalījās simts OA pacienti (nejaušināti iedalīja 98, pētījumu pabeidza 79). Iecerētā efektivitātes atšķirība starp PNHA un HA tikai noteikta 20 %. Ārstēšanas cikls: trīs i/a injekcijas ceļa locītavā, ik nedēļu ievadot PNHA vai HA.
Izvērtējumam izmantoja WOMAC (Western Ontario and McMaster Universities) skalu un KSS (Knee Society Score) skalu, ko aizpildīja pētījuma sākumā, tad 2, 6, 12 un 24 mēnešus pēc ārstēšanas, kā arī novērtēja sinoviālā šķidruma līmeni (sākumā un pēc ārstēšanas cikla). Blaknes izvērtēja pēc katras kontroles vizītes. Statistikas analīzei tika izmantots Kruskal–Wallis tests pēc vidējo lielumu korekcijas pēc vecuma, ĶMI, Kellgren and Lawrence pakāpes.
Rezultāti
KSS kopējais rezultāts un KSS sāpju skalas rezultāts uzrādīja ievērojamu simptomu uzlabojumu abās grupās, bet lielāku sāpju mazinājumu konstatēja PNHA saņēmēju grupā (samazinājums par 2 punktiem) nekā HA grupā (samazinājums par 1 punktu). Abās grupās ievērojams uzlabojums bija WOMAC kopējā rezultāta mazināšanās: pēc 24 mēnešiem ievērojami augstāks uzlabojums bija vērojams PNHA grupā ar stabilu 16 % atšķirību par labu PNHA, izvērtējot rezultāus WOMAC sāpju apakšskalā. Nozīmīgas klīniskas blaknes netika novērotas nevienā no grupām.
Secinājumi
Divus gadus ilgušā pētījuma iznākumi apstiprina ārstēšanu īsa cikla veidā, intraartikulāri ievadot polinukleotīdus (ilgas darbības viskozitāti uzlabojošas īpašības, hondrocītu aktivācija, sāpes mazinoša iedarbība) fiksētā devā ar hialuronskābi, uzlabojot ceļa locītavas funkcionalitāti un mazinot sāpes pacientiem ar OA.
Doc. A. Mihailova: “Neesmu savā praksē OA pacientiem veikusi intraartikulāru injekciju, kurā kombinēti polinukleotīdi un hialuronskābe. Bet, protams, ir virkne pētījumu, ka hialuronskābes injekcijas OA pacientiem mazina sāpes un kustību ierobežojumus, to apliecina arī mana klīniskā pieredze. Ir pētījumi, kas norāda, ka šādas injekcijas var palīdzēt līdz pat pieciem gadiem attālināt nepieciešamību endoprotezēt. Saistībā ar intraartikulāro injekciju iespējām OA ārstēšanā gribētu pieminēt steroīdu injekcijas. Zinot, ka OA ir viļņveida gaita ar paasinājumiem un remisijām, injekcija, kas laicīgi veikta paasinājuma sākumā, dažkārt līdz pat gadam var attālināt simptomātiku. Tomēr nevajadzētu absolutizēt intraartikulāro injekciju iespējas. Izvēloties ārstēšanas taktiku, nozīme ir OA tipam un nodiluma pakāpei. Piemēram, OA ar pavadošu hronisku sinovītu nedrīkst ārstēt ar hialuronskābes injekcijām. Tas pacienta stāvokli var vēl pasliktināt. Tāpat 4. pakāpes OA nodilumam, kur nav skrimšļa, bet ir vairs tikai kaili kaulu gali, injekcija uz dienu vai divām var mazināt sāpes, bet šāda terapijas izvēle noteikti nebūs mērķtiecīga. Jau minēju to iepriekš, bet uzsvēršu vēlreiz: arī tad, ja ārstēšanā izvēlas izmantot intraartikulārās injekcijas, būtiski pievērst uzmanību pacienta svaram un dzīvesveidam. Ja cilvēkam ir liekie kilogrami un viņš ir mazkustīgs, injekcijas nepalīdzēs un nedos cerēto efektu. Uzlabojumi būs iespējami tikai līdz ar dzīvesveida maiņu.”