Grāmatas autori sniedz aktuālu informāciju par urīnceļu infekcijas ārstēšanu un profilaksi primārās veselības aprūpes speciālista vajadzībām. Grāmatas pamatā ir Eiropas Urologu asociācijas, Eiropas Bērnu urologu biedrības vadlīnijas, ASV un Kanādas urologu asociācijas rekomendācijas.
Ievads
Grāmatā sniegti pamatoti ieteikumi ārstiem par urīnceļu infekcijas (UCI) ārstēšanu un profilaksi un iekļauta mūsdienīga informācija par UCI primārās veselības aprūpes (ģimenes ārsta prakses) vajadzībām: aprakstīts galvenokārt cistīts un pielonefrīts, netiek apskatītas uroloģiskas patoloģijas (uretrīts, orhīts, epididimīts, prostatīts), urosepse un dažas specifiskas situācijas, kas pietiekami pamatīgi aplūkotas iepriekšējā grāmatā. [1] Šajā izdevumā aktualizēti tikai daži UCI ambulatoras ārstēšanas aspekti.
Pieņemot lēmumu par pacienta ārstēšanu, nevienas vadlīnijas nevar aizstāt specializētas klīniskās zināšanas. Vadlīnijas var sniegt vien orientējošas norādes klīnisku lēmumu pieņemšanā, un šajā procesā jāņem vērā gan pacienta īpatnības un vēlmes, gan konkrētie apstākļi. Turklāt jāatceras, ka Eiropas un ASV farmācijas tirgū nav dažu mums ierasto preparātu, bet mūsu rīcībā nav dažu preparātu no Eiropas un ASV medikamentu klāsta.
Šajā grāmatā rakstīto pamato Eiropas Urologu asociācijas 2020. gadā pieņemtās vadlīnijas par urīnceļu infekcijas problēmām [2] un Eiropas Bērnu urologu biedrības 2020. gadā pieņemtās vadlīnijas, [3] kā arī 2019. gadā pieņemtās ASV un Kanādas rekomendācijas par recidivējošām UCI. [4] Informācija par terapijā izmantojamiem antibakteriālajiem līdzekļiem pielāgota Latvijas realitātei un pēdējām publikācijām. [5]
Urīnceļu infekcijas (UCI) ir vienas no izplatītākajām infekcijas slimībām. Apmēram 15 % no visām antibiotiku receptēm ASV izrakstītas UCI pacientiem. UCI veido līdz pat 40 % no visām slimnīcā iegūtajām infekcijām un vairākumā gadījumu saistītas ar urīna katetru lietošanu. Bakteriūrija attīstās līdz 25 % pacientu, kam vismaz nedēļu veikta urīnpūšļa katetrizācija, un risks bakteriūrijas attīstībai ar katru dienu pieaug par 5—7 %.
Satraucošs ir pašreizējais mikrobu rezistences attīstības stāvoklis. Antibiotiku lietošana Eiropas valstīs atspoguļo rezistentu patogēnu celmu globālu pieaugumu. Arvien vairāk izplatās paplašināta spektra bēta laktamāzi (ESBL — extended spectrum beta–lactamase) veidojošās baktērijas, kas ir rezistentas pret lielāko daļu antibiotiku, izņemot karbapenēmu grupu.
Īpašs apgrūtinājums ir pieaugošā rezistence pret tādām plaša spektra antibiotikām kā fluorhinoloni un cefalosporīni. To izraisījusi šo abu antibiotiku grupu pārmērīga lietošana un paralēla līdzrezistences attīstība pret citām antibiotikām. Situāciju sarežģī fluorhinolonu blaknes, kas izslēdz tos no preparātu pirmās rindas UCI ārstēšanā.
Papildus jārēķinās ar Covid–19 specifiku, jo arvien vairāk pierādījumu liecina, ka Covid–19 pacientiem ir augstāks risks aritmiju attīstībai, bet aritmijas būtiski ietekmē kopējos mirstības rādītājus. Makrolīdi (īpaši azitromicīns) un fluorhinoloni ir atpazīstamas antibiotikas, kas pagarina QT intervālu. [6; 7]
Paredzams, ka jaunas antibiotikas vismaz nākamajos desmit gados netiks ieviestas, tāpēc antibiotiku saprātīga lietošana ir vienīgais veids, kā aizkavēt rezistences attīstību. Svarīgi izvērtēt gan vietējo mikrobiālo vidi un rezistences ainu, gan rezistentu mikrobu veidošanās riska faktorus individuāliem pacientiem.
Bakteriālās rezistences veidošanās apdraud UCI ārstēšanu un uroloģisko ķirurģisko operāciju profilaksi. Korelācija starp antibiotiku lietošanu un rezistences veidošanos ir tieša, tāpēc steidzami jācīnās pret rezistences attīstību, antibiotikas lietojot saprātīgi. [8]
Urīnceļu infekcijas raksturojums
Patoģenēze
Biežākais UCI cēlonis ir mikroorganismu ascendēšana no apakšējām urīnizvadceļu daļām. Tas īpaši attiecas uz zarnu mikrofloru (E. coli un citas zarnu jeb enterobaktērijas). Tikai retos gadījumos mikroorganismi urīnceļos var nonākt hematogēnā ceļā vai ar limfu. Tas loģiski izskaidro, kāpēc sievietēm UCI rodas biežāk nekā vīriešiem un kāpēc lielāks infekciju risks ir pēc urīnpūšļa katetrizācijas vai izmeklēšanas ar instrumentiem.
Urīnceļu infekcija pēc katetra vienreizējas ievietošanas urīnpūslī rodas 1—2 % no ambulatorajiem pacientiem. Ilgkatetri ar atvērtās drenāžas sistēmu pēc 3—4 dienām gandrīz 100 % gadījumu izraisa bakteriūriju. Izmantojot slēgtās drenāžas sistēmas ar pretatplūdes vārstu, infekciju attīstība tiek aizkavēta, bet ne novērsta. Uzskata, ka baktērijas pārvietojas mukopurulentajā jeb gļotaini strutainajā telpā starp urīnizvadkanālu un katetru un apmēram četrās nedēļās gandrīz visiem pacientiem izraisa bakteriūriju.
Papildu risku rada bioplēves veidošanās, kas bieži pavada katetrizāciju un sastopama arī citu komplicētu UCI gadījumā. Bioplēves ievērojami pastiprina baktēriju rezistenci un padara dažas antibiotikas neefektīvas, jo liedz tām piekļuvi baktērijām.
Laboratoriskā atrade
Baktēriju skaitu uzskata par svarīgu kritēriju UCI diagnosticēšanai. 1956. gadā E. Kass izstrādāja nozīmīgas bakteriūrijas jēdzienu (≥ 105 KVV/ml). Taču vēlāk noskaidrots, ka nav konkrēta baktēriju skaita rādītāja, kas liecinātu par nozīmīgu bakteriūriju un ko varētu piemērot visu veidu UCI verifikācijai visos apstākļos.
Urīna paraugus ņem no urīna vidējās strūklas, nepieciešamības gadījumā arī ar katetru vai ar urīnpūšļa punkcijas palīdzību. Paraugos, kas iegūti ar urīnpūšļa punkciju virs kaunuma kaula, nozīmīgs ir jebkāds baktēriju skaits.
Svarīgs faktors veiksmīgai ārstēšanai ir floras jutība, bet jāatceras, ka arī šie rezultāti nav vērtējami viennozīmīgi, jo tie ir in vitro un var neatbilst reālai jutībai in vivo. Šāda nesakritība ir raksturīga fosfomicīnam un nitrofurānu atvasinājumiem, proti, šie preparāti var darboties pat tad, ja uzsējums uzrāda floras nejutīgumu (rezistenci) pret tiem. [9; 10]
Svarīga UCI diagnostikā ir leikocitūrija, par patoloģisku pieņemts uzskatīt leikocītu skaitu virs 103 l/mm3.
Diagnozes noteikšana
UCI ir kombinēta diagnoze, un to nosaka, ja konstatē:
- klīniskos simptomus (dizūrija, sāpes, drudzis),
- izmaiņas urīna sedimentā (leikocitūrija) un
- verificē bakteriūriju (ar nitrītu testu un/vai kultūras uzsējumu).
Visi trīs komponenti ir obligāti UCI diagnozes noteikšanai. Ja kāds iztrūkst, UCI diagnoze ir apšaubāma un pacients jāizmeklē papildus, lai noskaidrotu patiesos sūdzību vai laboratorisko izmaiņu cēloņus.
Klasifikācija
UCI iedalījums: nekomplicētas un komplicētas UCI un urosepse (1. attēls). Praksē UCI klasificē pēc infekcijas anatomiskā līmeņa (cistīts, pielonefrīts u.c.). Papildus var vērtēt infekcijas smaguma pakāpi, riska faktorus, mikrobioloģiskās atrades.
UCI simptomātika un laboratoriskās atrades norāda uz infekcijas anatomisko līmeni un slimības smaguma pakāpi. UCI riska faktoru analīze palīdz noteikt papildu terapeitiskos pasākumus (piemēram, drenāžu).
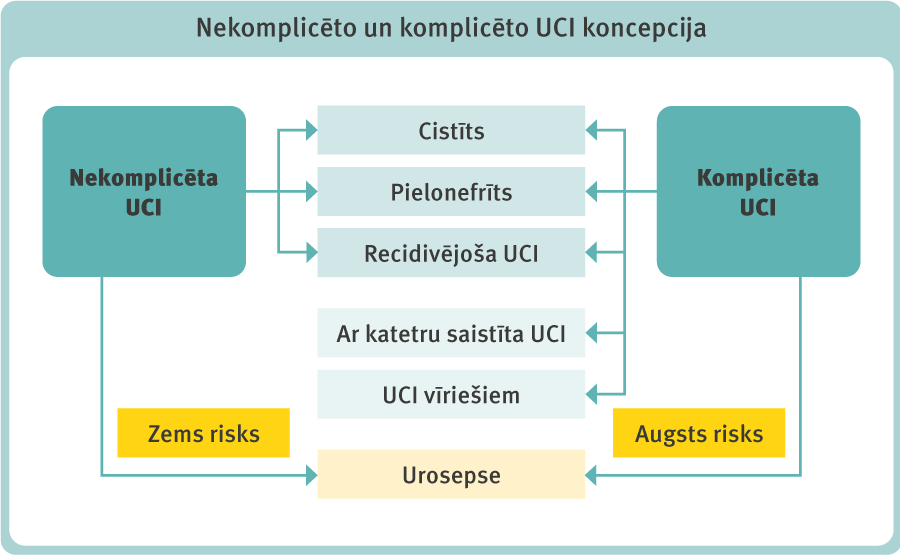

1. attēls
Nekomplicēto un komplicēto UCI koncepcija
Nekomplicētas UCI (nUCI)
Akūta, sporādiska vai atkārtota apakšējā (nekomplicēts cistīts) un/vai augšējā (nekomplicēts pielonefrīts) UCI sievietēm, kas nav grūtnieces, bez zināmām anatomiskām un funkcionālām novirzēm urīnceļos, bez blakusslimībām, bez recidivējošas UCI (rUCI).
Komplicētas UCI (kUCI)
Pēc vadlīniju definīcijām tās ir visas UCI, kas nav definētas kā nekomplicētas. Reāli tas nozīmē tikai to, ka UCI pacientam ir palielināta iespējamība komplikāciju attīstībai: visi vīrieši, grūtnieces, pacienti ar anatomiskām vai funkcionālām novirzēm urīnceļos, urīna katetri, nieru slimības un/vai citas vienlaikus imūnkompromitējošas slimības, piemēram, cukura diabēts.
Šāds sadalījums nereti ir mulsinošs, jo dažreiz komplicētu UCI uztver kā patoloģiju, kurai vajadzīga atšķirīga pieeja un ārstēšana, kam ne vienmēr ir pamatojums. Abos gadījumos empīriskās terapijas izvēle ir vienāda!
Recidivējošas UCI (rUCI)
Nekomplicētas vai komplicētas UCI atkārtošanās ar biežumu vismaz trīs epizodes gadā vai divas epizodes pēdējos sešos mēnešos.
Ar katetru saistītas UCI (cUCI)
Ar katetru saistīta UCI rodas cilvēkam, kura urīnceļi šajā brīdī ir katetrizēti vai kuram pēdējās 48 stundās urīnceļos bijis katetrs.
Urosepse
Urosepse ir dzīvībai bīstama orgānu disfunkcija, ko izraisa nepietiekami regulēta organisma reakcija uz infekciju, kas iziet no urīnceļiem un/vai vīriešu dzimumorgāniem.
Urīnceļu infekcijas diagnostika un ārstēšana
Akūtas, nekomplicētas UCI pieaugušajiem nozīmē sporādiskas akūta cistīta un akūta pielonefrīta infekcijas epizodes citādi veselām personām. 70—95 % gadījumu ierosinošais patogēns ir E. coli, kas arī nosaka empīriskās terapijas izvēli.
Akūts nekomplicēts cistīts sievietēm pirms menopauzes, bez grūtniecības
Akūta nekomplicēta cistīta diagnozi var noteikt, izvērtējot urīnceļu kairinājuma simptomus (dizūrija, urinēšanas biežums un neatliekamība), ja nav izdalījumu no maksts vai maksts kairinājuma un sievietei nav citu komplicētu UCI riska faktoru.
Akūta nekomplicēta cistīta gadījumā urīnu pārbauda ar teststrēmeli, nevis izmeklē mikroskopiski. Indikācijas urīna kultūras parauga ņemšanai:
- ja simptomi nepāriet vai atkārtojas 2—4 nedēļas pēc ārstēšanas,
- sievietēm ar netipiskiem simptomiem.
Sievietei ar akūta nekomplicēta cistīta simptomātiku par diagnozes rādītāju uzskatāms uropatogēnu koloniju skaits ≥ 10³ KVV/ml mikrobioloģiskajos izmeklējumos.
Ārstēšana
Kritēriji, izvēloties antibakteriālu terapiju:
- uropatogēnu spektrs un jutīgums,
- klīniskajos pētījumos noskaidrotā efektivitāte konkrētajai indikācijai,
- panesība un nevēlamās blaknes,
- nelabvēlīga ietekme uz vidi,
- izmaksas,
- pieejamība.
Pēc šiem principiem un informācijas par jutīguma ainu gan Eiropā, gan ASV par pirmās izvēles medikamentiem uzskata:
- nitrofurānu atvasinājumus 50—100 mg divas reizes dienā 5—7 dienas,
- fosfomicīna trometamola vienreizēju 3 g devu,
- kotrimoksazolu 160/800 mg divas reizes dienā 3—5 dienas, ja zināms, ka rezistence pret E. coli populācijā ir < 20 %,
- pivmecilinama hidrohlorīdu 400 mg trīs reizes dienā 3—5 dienas.
Ja simptomi pēc terapijas izzūd, kontroles urīna analīzes un uzsējumu neveic. Sievietēm, kam līdz ārstēšanas beigām simptomi nepazūd vai kam simptomi pazūd, taču divu nedēļu laikā atjaunojas, jāveic urīna uzsējumi un jāpārbauda jutība uz antibakteriālajiem līdzekļiem. Šādā gadījumā jāpieņem, ka infekciju izraisījušais organisms nav jutīgs pret sākotnēji lietoto medikamentu. Jāapsver atkārtots septiņas dienas ilgs ārstēšanas kurss ar citu preparātu.
Autoru komentārs par terapijas kursa ilgumu
Par terapijas kursa ilgumu UCI gadījumā tiek diskutēts jau vairāk nekā 40 gadus, konsensus joprojām nav panākts (ieteikumi nitrofurānu atvasinājumu lietošanai: piecas dienas Eiropā, septiņas dienas ASV, trīs dienas Lielbritānijā un līdz desmit dienām Kanādā).
Terapijas ilgums lielākoties atkarīgs no blakņu biežuma un daudz mazākā mērā no antibiotikas izvēles. Ar trīs dienu kursu gandrīz vienmēr pietiek simptomātiskam efektam (klīniskam uzlabojumam), bet tas nenodrošina pilnīgu baktēriju izvadīšanu. [11]
Autoru pieredze ir līdzīga: 1980. gadu sākumā Bērnu klīniskajā universitātes slimnīcā mēģināja nitrofurānu atvasinājumu kursa ilgumu UCI gadījumā saīsināt izteikto blakņu dēļ (jāpiebilst, ka Furamags® mums vēl nebija pieejams). Klīniskais efekts (simptomu mazināšanās un urīna analīžu sanācija) tika iegūts trešajā dienā. Diemžēl jau pēc pāris nedēļām šiem pacientiem tika reģistrēti UCI recidīvi. Pēc pāris mēnešiem novērojumu pārtrauca, jo recidīvu skaits pieauga virs 30 %. Tā kā tas bija slimnīcas iekšējais (un neveiksmīgs) eksperiments, dati netika publicēti.
Rezumējot: jo mazāk toksisks preparāts, jo ilgāku kursu var un vajadzētu nozīmēt. Lietojot maztoksisku preparātu (Furamags®), ieteicams garāks terapijas kurss.
Īsumā par preparātiem
Par nitrofurānu atvasinājumiem jāpiebilst, ka Rietumeiropā un ASV pieejams tikai nitrofurantoīns mikrokristāliskā un makrokristāliskā formā, kā arī abu formu kombinācijā (piemēram, Macrobid®, ar daudz labāku biopieejamību un mazāk izteiktām blaknēm).
Austrumeiropā un vairākās Āzijas valstīs pieejami modernāki nitrofurānu atvasinājumi (piemēram, Furamags® ar vēl labāku biopieejamību un mazāk izteiktām blaknēm, salīdzinot ar Macrobid®). Turklāt pēdējie pētījumi liecina, ka Furamags® minimālā inhibējošā koncentrācija pret E. coli ir ne tikai četras reizes labāka (zemāka) nekā nitrofurantoīnam, bet Furamags® terapeitiskajā koncentrācijā ir efektīvs pret E. coli bioplēvi un tādējādi kļūst par izvēles līdzekli ar katetru saistītu UCI ārstēšanā un profilaksē. [12; 13]
Fosfomicīna vienas devas efekts ir labs, bet pētījumi rāda, ka ilgtermiņa efektivitāte ir krietni zemāka nekā nitrofurantoīnam, tāpēc izskan ieteikumi to lietot atkārtoti pēc 48 un/vai 72 stundām vai arī nozīmēt 3—5 dienu kursu (2. attēls). Šāda pieeja izsvītro tā galveno priekšrocību (vienas devas kurss) un ievērojami palielina ārstēšanas izmaksas. [14]
Kotrimoksazola rezistence pret E. coli Latvijā pēc dažādiem datiem sasniedz pat 80—90 %, tātad mūsu praksē šis preparāts nav noderīgs. Pivmecilinama hidrohlorīds Latvijā nav pieejams un šeit netiek apskatīts.
Aminopenicilīni nav piemēroti empīriskai terapijai, jo E. coli visā pasaulē ir milzīga rezistence pret aminopenicilīniem. Aminopenicilīnu un bēta laktamāzes inhibitora kombinācijas, piemēram, ampicilīns/sulbaktāms vai amoksicilīns/klavulānskābe, un perorāli lietojamie cefalosporīni kopumā nav tik efektīvi īstermiņa ārstēšanā. Eiropā tos empīriskā terapijā neiesaka, bet atsevišķos gadījumos šo līdzekļu lietošana ir pieļaujama un dažas ASV rekomendācijas šos preparātus pirmajā rindā tomēr iekļauj.
Fluorhinoloni UCI ārstēšanā ir bēdu stāsts. Tā ir patiesi iedarbīga antibiotika, diemžēl katru gadu pēdējos desmit gados pieaudzis ziņojumu skaits par blakusparādībām, kas izraisa invaliditāti (piemēram, cīpslu plīsumi), ir paliekošas (nemazinās un neizzūd pēc antibiotikas atcelšanas) un letālas (piemēram, aortas aneirisma un aortas plīsums). Šādas blaknes rodas arī bērniem. [15] Tas bija iemesls, kāpēc sākotnēji ASV un vēlāk arī Eiropā apturēja vai ierobežoja hinolonu un fluorhinolonu antibiotiku lietošanu. [16]
Fluorhinoloni nav jālieto rīkles infekciju, hroniska prostatīta, UCI un citu vieglu vai vidēji smagu baktēriju infekciju gadījumā, izņemot atsevišķas reizes, kad citu antibiotiku lietošana nav iespējama. [19] Arī Latvijas Zāļu valsts aģentūra veselības aprūpes speciālistiem izsūtīja vēstuli par fluorhinoloniem. [20] Rezumējot: par fluorhinoloniem UCI gadījumā labāk aizmirst!
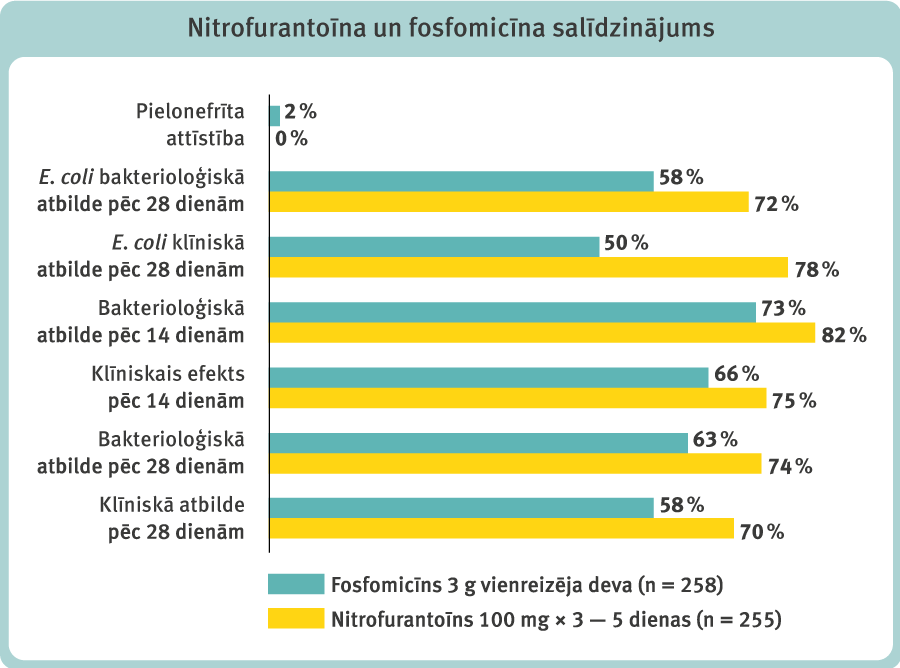

2. attēls
Nitrofurantoīna un fosfomicīna salīdzinājums
Akūts nekomplicēts pielonefrīts sievietēm pirms menopauzes, bez grūtniecības
Par akūtu pielonefrītu liecina sāpes sānos, slikta dūša un vemšana, drudzis (> 38 °C) vai jutīgums kostovertebrālajā leņķī, un šī slimība var rasties arī bez cistīta simptomiem. Ieteiktā standarta diagnosticēšanas metode ir urīna analīze (ar teststrēmeli), kur novērtē arī leikocītu, eritrocītu un nitrītu rādītājus.
Par klīniski nozīmīgu bakteriūriju liecina uropatogēnu koloniju skaits ≥ 105 KVV/ml. Empīriskā terapijā jāvadās pēc datiem par nekomplicēta cistīta ārstēšanu.
Urīnceļu ultrasonoskopiska izmeklēšana
Augšējo urīnceļu izmeklēšana ar ultraskaņu jāveic tādēļ, lai izslēgtu urīnceļu obstrukciju vai nierakmeņus. Papildu izmeklējumi, piemēram, spirāldatortomogrāfija (DT), ekskrēcijas urogrāfija vai nieru dinamiskā scintigrāfija ar dimerkaptosukcīnskābi (DMSA) jāapsver tad, ja 72 stundas pēc ārstēšanas sākuma pacientei nav mazinājies drudzis. Šādā gadījumā, izsverot uzsējuma atbildes rezultātus, jāapdomā arī preparāta nomaiņa un nepieciešamība stacionēt.
Viegls un vidēji smags akūts nekomplicēts pielonefrīts
Viegla un vidēji smaga akūta nekomplicēta pielonefrīta gadījumā parasti pietiek ar 10—14 dienas ilgu kursu perorāli. Ja 72 stundas pēc ārstēšanas sākuma pacientam nav mazinājies drudzis, pēc kultūras rezultātu izskatīšanas jāapsver preparāta nomaiņa, jo pēc trīs dienas ilgas empīriskas terapijas būtu jābūt vismaz kaut kādam efektam. Apsverama arī parenterāla terapija ar trešās paaudzes cefalosporīniem vai aminopenicilīniem vai nepieciešamība stacionēt.
Smags akūts nekomplicēts pielonefrīts
Par smagu pielonefrītu pēc Harvard Health Publishing informācijas uzskata gadījumus ar drudzi un drebuļiem, sliktu dūšu un vemšanu, kad medikamentus nav iespējams uzņemt iekšķīgi un ir dehidratācijas pazīmes. [21]
Smaga pielonefrīta pacientiem sākotnējai terapijai jāizvēlas kāda no šīm antibiotikām:
- 3. paaudzes cefalosporīnu grupas preparāts (parenterāli),
- aminopenicilīns kopā ar bēta laktamāzes inhibitoru (parenterāli),
- aminoglikozīds vai karbapenēmu grupas preparāts (parenterāli).
- alternatīva: ciprofloksacīns (parenterāli) — tikai tad, ja iepriekš uzskaitītie preparāti nedarbojas vai nav pieejami (pēdējās izvēles preparāts)!
Ja ar diagnostikas metodēm, kas ir ārsta rīcībā, nevar izslēgt komplicēšanās faktorus un/vai pacientam ir klīniskas pazīmes un simptomi, kas liecina par urosepsi, jāapsver stacionēšana.
Pēc uzlabošanās pacients 1—2 nedēļas var perorāli lietot kādu no iepriekš minētajiem antibakteriālajiem līdzekļiem, ja tie ir aktīvi pret infekciju ierosinošo organismu. Asimptomātiskiem pacientiem urīna analīzes vai urīna uzsējumu pēc ārstēšanas neveic.
Sievietēm, kam pielonefrīta simptomi pēc trīs dienu kursa neuzlabojas, jāveic atkārtoti urīna kultūru uzsējumi, jāpārbauda jutība uz antibakteriālajiem līdzekļiem un jāveic nepieciešamie izmeklējumi, piemēram, nieru ultrasonogrāfija, DT vai nieru scintigrāfija.
Recidivējošas UCI (rUCI)
Recidivējošas UCI bieži rodas jaunām, veselām sievietēm, pat ja viņu urīnceļu kopējais stāvoklis ir anatomiski un fizioloģiski normāls. Recidivējošas UCI gadījumā jāveic urīna uzsējumi un būtu vēlams kultūru salīdzinājums ar iepriekšējām epizodēm.
Sievietēm ar recidivējošu UCI parasti neiesaka augšējo urīnceļu attēldiagnostikas izmeklējumus un cistoskopiju, taču netipiskos gadījumos, lai izslēgtu urostāzi, tos tomēr vajadzētu veikt.
Antibiotiku terapija ir tāda pati kā sporādisku nekomplicētu UCI gadījumā:
- nitrofurānu atvasinājums 50—100 mg divas reizes dienā līdz septiņām dienām,
- fosfomicīna trometamols — vienreizēja deva 3 g,
- kotrimoksazols 160/800 mg divas reizes dienā līdz septiņām dienām, ja zināms, ka rezistence pret E. coli ir < 20 %.
Autoru komentārs par terapijas kursa ilgumu
Literatūrā jau ilgstoši diskutē par medikācijas kursa ilgumu, ārstējot rUCI un akūtas UCI. Vienprātības joprojām nav (piemēram, nitrofurānu atvasinājumus ASV iesaka lietot vismaz septiņas dienas). Maztoksisku preparātu kursi varētu būt garāki.
Urīnceļu infekciju profilakse
Profilaktiskā terapijā ievērojama nozīme varētu būt nitrofurānu grupas preparātiem (piemēram, Furamags®), uz kuriem joprojām ir relatīvi nozīmīga jutība.
Pirms profilakses ar antibakteriālajiem līdzekļiem 1—2 nedēļas pēc ārstēšanas jāiegūst negatīvs rezultāts urīna uzsējumā, lai pārliecinātos, ka iepriekšējā UCI izārstēta. Antibakteriālo līdzekļu profilaktiska lietošana (pastāvīga vai pēc dzimumakta), lai novērstu UCI atkārtošanos, jāapsver tikai pēc vizītes, kad pacients apņēmies mainīt paradumus, kā arī tad, ja citi pasākumi, kas neietver antibakteriālo līdzekļu lietošanu, bijuši nesekmīgi.
Nozīmīga urostāze ir jāārstē, viena no metodēm — intermitējoša katetrizācija. Sievietēm pēc menopauzes jāapsver hormonu aizstājterapija. Antibiotiku izvēles nosacījumi ir tādi paši kā sporādisku nekomplicētu UCI gadījumā.
Antibakteriālo līdzekļu profilaktiska lietošana
Antibakteriālos līdzekļus profilaktiski var lietot vai nu pastāvīgi ilgāku periodu (3—6 mēnešus), vai vienreizējā devā pēc dzimumakta (1. tabula).
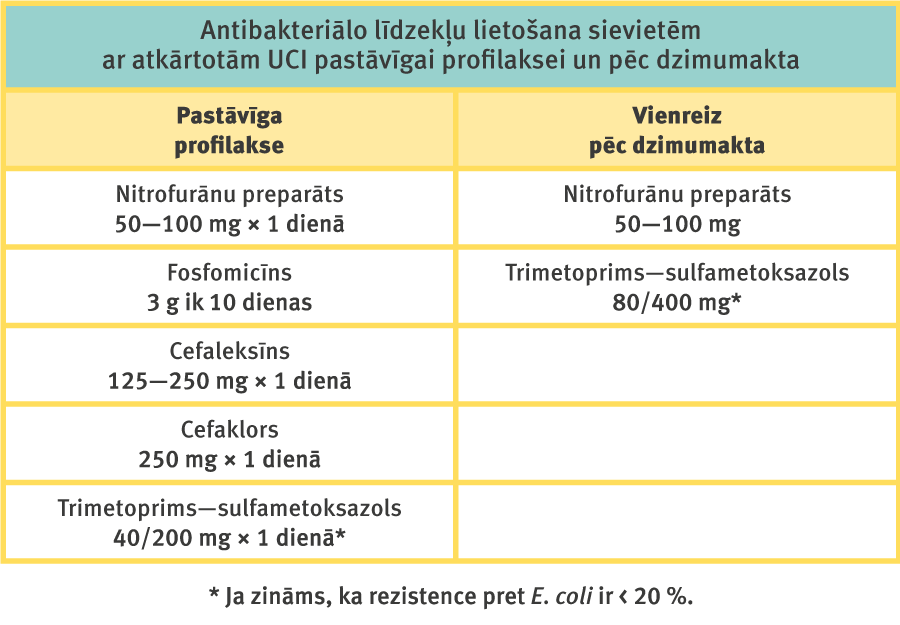

1. tabula
Antibakteriālo līdzekļu lietošana sievietēm ar atkārtotām UCI pastāvīgai profilaksei un pēc dzimumakta
Ne–antibakteriāla profilakse
Ir daudzi ar antibakteriālajiem līdzekļiem nesaistīti pasākumi, ko iesaka UCI atkārtošanās profilaksei, taču tikai daži no tiem izvērtēti kvalitatīvos pētījumos, no kuriem izriet ar pierādījumiem pamatoti ieteikumi.
Ieradumu pārskatīšana
Kaut pārliecinošus datus par saistību ar rUCI pētījumos iegūt nav izdevies, tomēr iesaka uzmanību pievērst potenciāli riskantiem ieradumiem: urinācijas aizturēšanai, samazinātam šķidruma patēriņam, nepareizajam noslaucīšanās virzienam pēc defekācijas, cieši piegulošai apakšveļai u.c.
Hormonāla profilakse pēcmenopauzes periodā
Vaginālie (bet ne orālie) estrogēni samazina risku UCI attīstībai.
Profilaktiska imunitāti aktivējošo līdzekļu lietošana
Pietiekami labi dokumentēti tikai dati par OM–89 (Uro–Vaxom®). Vairākos pētījumos ar iedalījumu pēc nejaušības principa tas bijis efektīvāks par placebo. Tāpēc to var ieteikt kā imunitāti aktivējošu profilaktisku līdzekli sievietēm ar recidivējošām nekomplicētām UCI. Par citiem imūnterapijas līdzekļiem ieteikumus sniegt nav iespējams.
Probiotiku profilaktiska lietošana
Nav izdevies iegūt pārliecinošus pierādījumus Lactobacillus preparātu efektivitātei rUCI profilaksē. Nav iespējams sniegt ieteikumus.
Dzērveņu lietošana UCI profilaksē
Nelielā skaitā pētījumu izteikts pieņēmums, ka dzērvenes (Vaccinium macrocarpon) palīdz mazināt apakšējo UCI biežumu sievietēm. Meta–analīzē (24 pētījumi, dati par 4473 dalībniekiem) konstatēts, ka, lietojot dzērveņu produktus, simptomātisku UCI biežums nozīmīgi nesamazinās.
Pretrunīgo rezultātu dēļ dzērveņu produktu lietošanu ikdienā rUCI profilaksē ieteikt nav iespējams.
Asimptomātiska bakteriūrija
Nosaukums ir pašdefinējošs un nozīmē jebkādu simptomu, sūdzību un citu izmaiņu neesību — ir tikai bakteriūrija. Asimptomātisku bakteriūriju (ABU) diagnosticē, ja paraugos, kas ņemti ar vismaz 24 stundu starplaiku, divas kultūras (vīriešiem — viena kultūra) uzrāda bakteriūriju ar uropatogēnu skaitu ≥ 105 KVV/ml. Ja urīna paraugs ņemts ar katetru, baktēriju skaits ABU gadījumā var būt tikai 10² KVV/ml.
Papildu izmeklējumi nav nepieciešami, un šie pacienti nav jāārstē. Izņēmums ir grūtnieces, kad pieļaujama ABU ārstēšana ar standarta kursiem (ne ilgāk par septiņām dienām).
Urīnceļu infekcija grūtniecēm
Grūtniecības laikā bieži rodas UCI un ABU. Lielākajai daļai sieviešu ir nosliece uz ABU vai tā radusies jau pirms grūtniecības, un pielonefrīts grūtniecības laikā attīstās 20—40 % sieviešu ar ABU.
Urīnceļu infekcijas diagnostika grūtniecēm
Akūta cistīta un pielonefrīta diagnostikas kritēriji citādi veselām grūtniecēm ir tādi paši kā sievietēm, kas nav grūtnieces. Taču cistīta gadījumā ļoti ieteicams veikt fizikālo izmeklēšanu un urīna analīzes, urīna uzsējumus. Ja ir aizdomas par pielonefrītu, jāveic arī nieru un urīnceļu ultrasonogrāfija.
Bakteriūrijas definīcija grūtniecēm
Asimptomātisku bakteriūriju grūtniecēm diagnosticē, ja divos secīgos urīna paraugos vienas baktēriju sugas augšanas rādītājs ≥ 105 KVV/ml vai vienā ar katetru iegūtā paraugā uropatogēna augšanas rādītājs ≥ 105 KVV/ml.
Grūtniecēm ar UCI simptomiem nozīmīgu bakteriūriju diagnosticē, ja parastā vai ar katetru iegūtā urīna paraugā uropatogēna augšanas rādītājs ir ≥ 10³ KVV/ml. Grūtniecības pirmajā trimestrī jāveic bakteriūrijas sijājošā diagnostika.
Asimptomātiskas bakteriūrijas un akūta cistīta ārstēšana
Ieteicamie antibakteriālie preparāti:
- nitrofurantoīns 100 mg × 2, ilgums 3—5 dienas (jāizvairās G6PD deficīta gadījumā un jāpievērš uzmanība konkrētā preparāta zāļu aprakstam, jo ne visus nitrofurānu atvasinājumus drīkst ordinēt grūtniecēm),
- amoksicilīns 500 mg × 3, ilgums 3—5 dienas,
- amoksicilīns/klavulānskābe 500/125mg × 2, ilgums 3—5 dienas,
- cefaleksīns 500 mg × 3, ilgums 3—5 dienas,
- fosfomicīns 3 g vienreizējā devā.
Asimptomātiskas bakteriūrijas un cistīta ārstēšanai grūtniecības laikā jāapsver antibakteriālo līdzekļu lietošana ne ilgāk par trim dienām. Urīns uzsējumam jāņem 1—2 nedēļas pēc tam, kad grūtniecei pabeigta ABU un simptomātiskas UCI ārstēšana. Sievietēm, kam UCI bieži bijušas pirms grūtniecības, tās laikā jāapsver profilakse pēc dzimumakta, lai mazinātu UCI risku.
Pielonefrīta ārstēšana grūtniecēm
Ja grūtniecei pielonefrīts norit ar viegliem simptomiem un ir iespējama stingra uzraudzība, jālieto piemēroti antibakteriālie preparāti. Ieteicamie parenterālo antibiotiku režīmi pielonefrīta ārstēšanai grūtniecēm apkopoti 2. tabulā. Pēc klīniskas uzlabošanās no parenterālās terapijas var pāriet uz perorālo; kopējam ārstēšanas ilgumam jābūt 7—10 dienas.
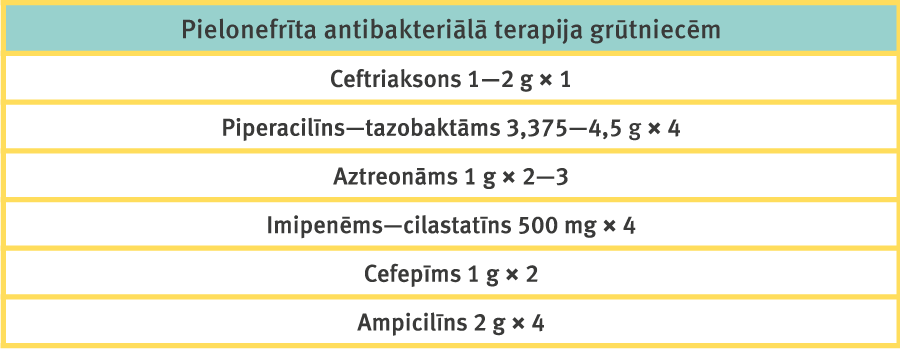

2. tabula
Pielonefrīta antibakteriālā terapija grūtniecēm
Komplicētas urīnceļu infekcijas grūtniecēm
Lai diagnosticētu komplikācijas veidojošos faktorus urīnceļos, vēlams izmantot ultrasonogrāfijas vai magnētiskās rezonanses attēlveidošanas metodes, lai mazinātu augļa apstarošanas risku. Obligāts 7—10 dienas ilgs terapijas kurss ar piemērotu antibakteriālo līdzekli, jāārstē visas uroloģiskās patoloģijas. Parasti paciente jāstacionē.
Urīnceļu infekcija sievietēm pēc menopauzes
Gados vecākām stacionētām pacientēm nozīmīgākie ar UCI saistītie riska faktori varētu būt urīnceļu katetrizācija un nieru funkciju pasliktināšanās. Citi riska faktori:
- atrofisks vaginīts,
- urīna nesaturēšana, cistocēle un nepilnīga urīnpūšļa iztukšošanās,
- UCI pirms menopauzes.
Diagnostika un ārstēšana
Diagnosticējot UCI sievietēm pēc menopauzes, vienmēr jāņem vērā anamnēze, fizikālā izmeklēšana, urīna analīzes un urīna uzsējums. Jāatceras, ka uroģenitālie simptomi ne vienmēr saistīti ar UCI un ne vienmēr ir nepieciešama antibakteriāla terapija.
Cistītu un pielonefrītu sievietēm pēc menopauzes ārstē līdzīgi kā sievietēm pirms menopauzes. Asimptomātiska bakteriūrija gados vecākām sievietēm nav jāārstē. Ja izslēgti komplikācijas veidojošie faktori, piemēram, urīnceļu obstrukcija un neirogēni urīnpūšļa traucējumi, jāordinē profilaktisks antibakteriālo līdzekļu kurss līdzīgi kā sievietēm pirms menopauzes.
Akūta urīnceļu infekcija jauniem vīriešiem
Tikai neliels skaits vīriešu 15—50 gadu vecumā slimo ar akūtām UCI. Minimālais antibakteriālās terapijas ilgums šajos gadījumos ir septiņas dienas.
Vairākumam vīriešu, kam UCI noris ar drudzi, vienlaikus ir arī prostatas infekcija, ko var noteikt pēc PSA līmeņa pārejošas paaugstināšanās serumā un pēc prostatas tilpuma. Pusaudžiem un vīriešiem, kam ir UCI ar drudzi, pielonefrīts vai atkārtota infekcija, jāveic standarta uroloģiskā novērtēšana. Ieteicamais minimālais ārstēšanas ilgums ir divas nedēļas.
Ar katetra lietošanu saistīta UCI (cUCI)
Urīnceļi ir biežākā nozokomiālo infekciju lokalizācija, īpaši, ja veikta urīnpūšļa katetrizācija. Lielākā daļa ar katetru asociēto UCI rodas no paša pacienta resnās zarnas mikrofloras, bet katetrs veicina UCI attīstību.
Galvenais riska faktors bakteriūrijas attīstībai ir katetrizācijas ilgums. Ar īslaicīgu katetru lietošanu saistītās bakteriūrijas lielākoties ir asimptomātiskas, tās izraisījis kāds atsevišķs patogēns. Vairāku veidu mikroorganismi urīnceļos nonāk pacientiem, kam katetrizācija ilgusi vairāk par 30 dienām. Pacientiem, kam nepieciešama katetrizācija, jāievēro divas prioritātes:
- katetra sistēmai jābūt noslēgtai,
- katetrizācijas laikam jābūt iespējami īsākam.
Antibakteriālā terapija ieteicama tikai simptomātisku infekciju gadījumā!
Katetra apkope
Katetra urīna drenāžas sistēmai vienmēr jābūt noslēgtai (jābūt pievienotam aizvērtam urīna maisam). Vienmēr jānodrošina brīva urīna drenāža:
- jāizvairās no katetra un drenāžas cauruļu pārliekšanās,
- urīna maisam vienmēr jābūt novietotam zemāk par urīnpūsli,
- urīna maiss regulāri jāiztukšo.
Svarīgi ievērot regulāru personisko higiēnu (urīnizvadkanāla zonas apmazgāšana vismaz reizi dienā). Manipulācijas ar katetru veikt tikai ar tīrām, nomazgātām rokām, izmantojot vienreizlietojamos cimdus.
Tīra urīna maisa pievienošana jāveic ik septiņas dienas, izmantojot aseptiskas metodes. Katetra nomaiņa rutīnā nav rekomendēta, taču jāapsver pēc klīniskām indikācijām (UCI, katetra obstrukcija, katetra un drenāžas sistēmas bojājums).
Urīnceļu infekcija bērniem
UCI ir kombinēta diagnoze, kuras noteikšanu pamato klīniskā aina (simptomi un sūdzības) un verifikācija (urīna analīzes un uzsējums jeb kultūra). Abi komponenti ir obligāti.
UCI ir biežākā infekcija bērniem un zīdaiņiem, iespējams, pat biežāka nekā augšējo elpceļu un gremošanas trakta infekcijas. UCI izplatība atkarīga no vecuma un dzimuma. Pirmajā dzīves gadā zēniem UCI konstatē divreiz biežāk nekā meitenēm, vēlāk proporcija mainās (meitenēm pret zēniem 3 : 1). UCI ir biežākais neskaidras etioloģijas drudža cēlonis vecumā līdz trīs gadiem. UCI klīniskās izpausmes bērniem var būt dažādas, sākot ar drudzi un beidzot ar kuņģa—zarnu trakta un apakšējo/augšējo urīnceļu simptomiem.
Izmeklējumi jāveic pēc divām UCI epizodēm meitenēm un pēc vienas epizodes zēniem. Mērķis ir izslēgt obstrukciju, vezikoureterālo atvilni jeb refluksu (VUR) un neirogēnus urinācijas traucējumus. [22]
UCI iznākums parasti ir labdabīgs, taču agrā vecumā UCI var izraisīt nieru rētas, īpaši, ja ir iedzimtas urīnceļu anomālijas un VUR. Hroniska pielonefrīta izraisītas nieru rētas rodas jau ļoti agrīnā vecumā, nieru rētas displāzijas dēļ jau intrauterīni. Ar nieru rētām saistītas vēlīnās sekas ir hipertensija, proteinūrija, nieru bojājumi un hroniska nieru mazspēja, kuras dēļ var būt nepieciešama dialīze.
Etioloģija
Izplatīti patogēni ir Grama negatīvie organismi, lielākoties enterobaktērijas. Līdz 90 % gadījumu primāro UCI izraisītājs ir E. coli. Grama pozitīvās baktērijas (īpaši enterokoki un stafilokoki) izraisa 5—7 % UCI gadījumu. Slimnīcā iegūtajām un atkārtotajām UCI ir plašāks agresīvo baktēriju spektrs, piemēram, Klebsiella, Serratia un Pseudomonas spp.
Jaundzimušajiem bieži konstatē A un B grupas streptokokus. Paraugos, kas ņemti bērniem ar UCI, arvien biežāk izolē S. saprophyticus, lai gan šīs baktērijas iesaiste vēl nav pilnīgi noskaidrota.
Asimptomātiska bakteriūrija sastopama 3,4 % jaundzimušo, 1,3 % zīdaiņu un 0,8 % pirmsskolas vecuma zēnu un meiteņu. Simptomātiska bakteriūrija sastopama 0,14 % jaundzimušo, bet vecumā līdz sešiem mēnešiem sastopamība pieaug līdz 0,7 % zēniem un 2,8 % meitenēm.
Patoģenēze un riska faktori
Urīnceļi ir sterila telpa ar necaurlaidīgu iekšējo izklājumu. Biežākais inficēšanās mehānisms ir retrogrādā ascendēšana. Retāk UCI iegūtas slimnīcā vai ir daļa no kādas sistēmiskas infekcijas.
Biežākie UCI iemesli ir obstrukcija un disfunkcija. Fimoze rada noslieci uz UCI. No zarnu floras atvasinātās enterobaktērijas veido kolonijas priekšādiņas maisā, uz dziedzeru virsmas un urīnizvadkanāla distālajā daļā. Šo patogēnu klāstā ietilpst E. coli celmi, kas izraisa P. fimbriae ekspresiju, liekot patogēnam pieķerties priekšādiņas iekšējam slānim un uroepitēlija šūnām.
UCI iemesls var būt dažādas iedzimtas urīnceļu anomālijas, kas obstrukcijas gadījumā var izraisīt UCI, piemēram, urīnizvadkanāla vārstuļi, obstrukcija urīnvada un nieres bļodiņas savienojuma vietā vai neobstruktīvs urīna sastrēgums (piemēram, atkarenā vēdera sindroms vai VUR). Retāki, taču arī nozīmīgi UCI cēloņi ir kaunuma lūpu saaugums un hronisks aizcietējums.
Ja citādi veselam bērnam ir urinēšanas traucējumi, var rasties neregulāra urīnpūšļa iztukšošanās, ko pastiprina urīna aizturēšanas paņēmieni, piemēram, kāju sakrustošana un tupēšana uz papēžiem. Neiropātiska urīnpūšļa disfunkcija (spina bifida vai slēdzējmuskuļa disfunkcija) var izraisīt urīna uzkrāšanos pēc urinēšanas un sekundāru VUR.
Saistība starp nieru bojājumiem un UCI ir pretrunīga. Obstruktīvas nefropātijas norises mehānisms ir skaidrs, taču VUR gadījumā izmaiņas ir nemanāmākas. Gandrīz droši, ka nepieciešamie komponenti ietver VUR, intrarenālo atvilni un UCI. Vajadzīga visu šo elementu mijiedarbība agrīnā bērnībā, kad augošās nieres ir uzņēmīgākas pret parenhīmas infekciju. Vēlāk bērnībā bakteriūrija maz ietekmē rētu progresēšanu un ļoti retos gadījumos izraisa jaunu rētu veidošanos. Cits veicinošais faktors ir intrauterīni attīstījusies nieru audu displāzija, lai gan arī šos daudzskaitlīgos veidojumus mēdz dēvēt par rētām.
Pazīmes un simptomi
UCI simptomi bērniem ir nespecifiski un mainīgi dažādos bērna vecumos un dažādām slimības smaguma pakāpēm. UCI jaundzimušajam var būt nespecifiska un nelokalizēta. Maziem bērniem UCI var izpausties kā kuņģa—zarnu trakta simptomi, piemēram, vemšana un caureja.
UCI sastopamība bērniem ar drudzi 0—3 mēnešu vecumā ir 7,2 %, 3—5 mēnešu vecumā 6,6 %, 6—12 mēnešu vecumā 5,4 %, kā arī 4,5 % bērnu 1—2 gadu vecumā, bet vecākiem bērniem ar UCI simptomiem un/vai drudzi — 7,8 % gadījumu. Urosepse rodas reti. UCI pazīmes maziem bērniem var būt neizteiktas, bet vēlāk, pēc divu gadu vecuma, var būt tādi simptomi kā bieža urinēšana, dizūrija un sāpes virs kaunuma kaula, vēdera apakšdaļā vai muguras jostas daļā, ar drudzi/bez drudža.
Dizūrija bez urīnceļu infekcijas
Dizūrija bez UCI mēdz būt prostatīta un uretrīta gadījumā zēniem, trigonīta un vaginīta gadījumā meitenēm, kā arī tad, ja bērnam ir kāda urīnceļu un dzimumorgānu anomālija, veidojumi, neirogēns urīnpūslis, hormonu disbalanss un psihogēni traucējumi, pēc traumām. Arī citas sūdzības (drudzis, sāpes vēderā vai sānos) nav patognomoniskas UCI. Nav pieļaujams, ka UCI diagnozi nosaka tikai pēc dizūrijas un tāpēc ordinē antibiotikas!
Bakteriūrija bez leikocitūrijas
Bakteriūriju bez leikocitūrijas parasti konstatē šādos gadījumos:
- urīna parauga bakteriāla kontaminācija,
- asimptomātiska bakteriūrija (ABU),
- ja paraugs ņemts pirms iekaisuma reakcijas sākšanās.
Lai precizētu situāciju, pēc 24 stundām urīna analīze jāatkārto. Pat ja bērnam ir drudzis un pozitīvs rezultāts urīna kultūru uzsējumā, leikocitūrijas neesība liek apšaubīt UCI diagnozi. Tad jāapsver ABU ar vienlaicīgu sepses perēkli, kas izraisa drudža sindromu.
Bērnu populācijā ABU agrīnā vecumā konstatē 0,5—2,5 %, pirmsskolas vecumā 0,5—1,3 %, pusaudžiem 1,1—1,8 %, biežāk meitenēm. [24]
Leikocitūrija bez bakteriūrijas
Leikocitūrija bez bakteriūrijas mēdz rasties šādu iemeslu dēļ:
- nepilnīga antibakteriālā terapija UCI ārstēšanai,
- urolitiāze un svešķermeņi,
- infekcijas, ko izraisa pret augšanas apstākļiem izvēlīgas baktērijas, piemēram, Chlamydia trachomatis.
Svarīgi! Nedz bakteriūrija, nedz leikocitūrija vai pozitīvas nitrītu analīzes izolēti nav uzskatāmas par uzticamiem kritērijiem UCI diagnosticēšanai vai izslēgšanai. Šie pacienti nav ārstējami ar antibiotikām! Turklāt papildus viņi jāizmeklē tikai tad, kad izmaiņām urīnā pievienojas attiecīga klīniskā aina.
Klasifikācija
Šobrīd pastāv piecas UCI klasifikācijas sistēmas bērniem.
- Klasifikācija pēc lokalizācijas: cistīts vai pielonefrīts.
- Klasifikācija pēc epizodēm: pirmā epizode, neizārstēta UCI (antibakteriālie līdzekļi nesasniedz terapeitisko līmeni, nepakļaušanās ārstēšanai jeb slikta līdzestība, malabsorbcija, rezistenti patogēni), persistējoša jeb noturīga UCI ar vienu un to pašu mikroorganismu (iemesls var būt noturīgs infekcijas perēklis urīnceļos, kad, iespējams, jāiejaucas ķirurģiski vai urinēšanas traucējumi jāārstē medikamentozi) un atkārtota infekcija ar dažādiem mikroorganismiem (var parādīties atšķirīgi E. coli serotipi).
- Klasifikācija pēc smaguma: par smagām uzskata UCI ar drudzi virs 39 °C, sliktu pašsajūtu, persistējošu vemšanu un dehidratāciju, kas parasti asociējas ar pielonefrītu.
- Klasifikācija pēc simptomiem: simptomātiska un asimptomātiska. Šeit jāpiemin dizūrija bez UCI, ABU (bakteriūrija bez leikocitūrijas) un asimptomātiska UCI (leikocitūrija bez bakteriūrijas).
- Klasifikācija pēc komplikācijām: komplicēta un nekomplicēta. Komplicēta UCI pēc Eiropas rekomendācijām ārstējama stacionārā, antibiotikas ievadot parenterāli, un šie pacienti jāizmeklē nekavējoties (USG), lai izslēgtu mehāniskas vai funkcionālas anomālijas. Komplicētas UCI diagnozes noteikšanai bez pozitīvas urīna kultūras obligāti jābūt vismaz vienam no šiem kritērijiem:
- jaundzimušais — UCI par komplicētu uzskatāma visiem jaundzimušajiem,
- pielonefrīta klīniskā aina,
- mehāniska (urīnizvadkanāla vārstulis, striktūras, konkrementi) vai funkcionāla (VUR un neirogēni vai ne–neirogēni apakšējo urīnceļu traucējumi) urīnceļu obstrukcija.
UCI klasifikācija pēc slimības smaguma pakāpes — 3. tabulā. Klīniski jāizšķir vieglas un smagas UCI formas, jo simptomu smaguma pakāpe zināmā mērā nosaka to, cik steidzami jāveic izmeklēšana un jāsāk ārstēšana.


3. tabula
UCI klīniskā klasifikācija bērniem
Diagnostika
Fizikālā izmeklēšana
Obligāti jāpārbauda, vai nav fimozes, kaunuma lūpu saaugumu, pielonefrīta pazīmju, epididimoorhīta un spina bifida pazīmju, piemēram, matainu plankumu uz ādas krusta kaulu apvidū. Tas, ka nav drudža, neizslēdz infekcijas procesu.
Laboratoriskās analīzes
Lai noteiktu galīgo infekcijas diagnozi, nepieciešams pozitīvs rezultāts urīna kultūras uzsējumā. Urīna paraugs uzsējumam jāiegūst bakterioloģiski uzticamos apstākļos. Pozitīvs rezultāts urīna kultūras uzsējumā definēts kā > 105 KVV/ml viena patogēna.
Urīna paraugu ņemšanas metodes bērniem
Ja bērns ir jaunāks par četriem gadiem (kad bērnam pilnībā jāmāk lietot podiņu), urīna parauga ņemšana var būt sarežģīta, tāpēc tiek ieteiktas vairākas paraugņemšanas metodes. [25]
Urīna strūklas vidējā porcija
Pirmā izvēles metode bērniem, kas spēj kontrolēt urināciju. Der gan parastai urīna analīzei, gan uzsējumiem, ievērojot rūpīgu higiēnu.
- Meitenēm jāatbīda kaunuma lūpas, starpene 2—3 reizes jānotīra ar neputojošu antiseptisku šķīdumu vai vieglas koncentrācijas ziepēm. Menstruāciju laikā meitenēm pirms parauga ņemšanas var ievietot tamponu, ja paciente (un vecāki) tam piekrīt.
- Zēniem urīnizvadkanāla atvere jānotīra līdzīgā veidā. Pirms tīrīšanas tiem, kas ir neapgraizīti, priekšādiņai jābūt atvilktai. Pirms urīna savākšanas starpenes apmazgāšana ar ziepēm var mazināt piesārņojuma līmeni.
- Urīna plūsmas saskari ar gļotādu samazina šādi: zēniem atvelk priekšādiņu, meitenēm urinācijas laikā atbīda kaunuma lūpas.
- Bērnam jāurinē tualetē vai podiņā. Paraugs ir jāuztver sterilā urīna traukā.
- Pēc paraugņemšanas priekšādiņa noteikti jāatvelk līdz normālai pozīcijai, lai nerastos parafimoze.
Šo metodi var izmantot arī paraugņemšanai no bērniem, kas vēl nekontrolē urināciju, un izraugās vienu no stimulācijas paņēmieniem.
- Urīnpūšļa stimulācija:
- 20 minūtes atļauj zīdainim ēst,
- dzimumorgānus notīra ar antiseptisku līdzekli (piemēram, Povidonum iodinatum šķīdumu),
- palīgam vai vienam no vecākiem zīdainis jātur uz rokām (zēna kājas karājas uz leju, meitenes kājas saliektas gurnos — sēdus stāvoklī),
- palīgam zem pacienta jātur sagatavota urīna tvertne,
- ar pirkstgaliem 30 sekundes viegli jāuzsit urīnpūšļa apvidum ar ātrumu ~ 100 × minūtē, tad 30 sekundes līdz urinēšanai jāveic paravertebrālā masāža. Visu procedūru drīkst atkārtot ne ilgāk par piecām minūtēm!
- Stimulācija ar aukstumu — simfīzes reģionu stimulē ar aukstu šķidrumu (Quick–Wee metode): aukstu šķidrumu (piemēram, sālsūdenī izmērcētu marles tamponu) klīnicists simfīzes reģionam uzliek uz laiku līdz piecām minūtēm.
Urīnpūšļa katetrizācija
Otrā izvēles metode urīna uzsējuma iegūšanai. Ļoti jutīga, droša un efektīva metode. Sāpju mazināšanai jālieto lidokaīnu saturoša katetru želeja. Higiēnas pasākumi līdzīgi kā urīna strūklas vidējās porcijas ievākšanā. Uzsējums uzskatāms par pozitīvu, ja atrod 105 KVV/ml vai vairāk abiem dzimumiem. Visizplatītākā metode uzsējumu iegūšanai pasaulē.
Urīnpūšļa aspirācija
Aspirācija ar punkciju virs kaunuma kaula — metode ar visaugstāko jutīguma pakāpi, taču urīnu izdodas iegūt vidēji tikai 23 % gadījumu. Izmanto tikai tad, kad urīna paraugu nav iespējams iegūt ar citām metodēm. Neizmanto bērniem, kas vecāki par diviem gadiem. Procedūra ir invazīva, sāpīga un sarežģīta:
- pacients nedrīkst urinēt vismaz 60 minūtes pirms procedūras,
- nepieciešama US kontrole (papildu tehnika un personāls),
- nepieciešama lokāla anestēzija ar zemādas lidokaīna injekciju,
- nepieciešams palīgs (vecāki) vai papildu personāls pacienta fiksācijai,
- atļauti tikai divi neveiksmīgi mēģinājumi, tad jāveic katetrizācija,
- iespējamās komplikācijas: makrohematūrija, vēdera priekšējās sienas abscess, < 1 % gadījumu — zarnu perforācija ar peritonītu.
Uzsējums, izmantojot aspirācijas metodi, par pozitīvu uzskatāms jebkādam koloniju skaitam abiem dzimumiem. Ņemot vērā sarežģītību, komplikāciju risku un papildu izmaksas, metode mūsu praksē nebūtu atbalstāma.
Urīna savācēji
Dzimumorgāniem piestiprināts plastmasas maisiņš. Tā kā iegūtie paraugi 85—99 % gadījumu uzrāda nepatiesi pozitīvu rezultātu, praksē šī metode nav ieteicama kā UCI apstiprinošs tests. Bet, ja šādā veidā savākts urīns neuzrāda leikocitūriju vai nitrītus, UCI var droši izslēgt.
Citas metodes
Citām urīna paraugu iegūšanas metodēm, piemēram, urīna izspiešanai no autiņbiksītēm, marles vai vates tamponiem, rezultāti nevar būt ticami, tāpēc tās nav pieļaujamas.
Urīna paraugu analīze
Jebkurš urīna paraugs būtu jāanalizē nekavējoties, jo formas elementu skaits urīnā ar laiku mazinās (tie “izšķīst”), savukārt baktērijas — savairojas. Optimālais ilgums urīna parauga nogādāšanai laboratorijā ir viena stunda. Pēc divām stundām urīna analīzes interpretācija jau ir nekorekta: var būt nepatiesi negatīvs rezultāts uz leikocitūriju un nepatiesi pozitīvs rezultāts uz baktērijām.
Teststrēmeles
Teststrēmeles metode palīdz ātri un uzticami izslēgt UCI, ja gan nitrītu, gan leikocītu esterāzes analīzē iegūti negatīvi rezultāti. Ja analīžu rezultāti pozitīvi, rezultāti jāapstiprina ar klīniskajiem simptomiem un citām analīzēm. [27]
Standarta teststrēmeles leikocitūriju kā pozitīvu uzrāda, sākot ar 25 l/µl. Ja teststrēmeles rezultāti negatīvi, urīna mikroskopija un uzsējums nav nepieciešami un UCI var izslēgt. [28]
Iekaisuma rādītāji
Asinsainā leikocitoze ar neitrofilozi liecina par bakteriālu infekciju. C reaktīvais olbaltums (CRO) ir nespecifisks, bet palīdz noteikt, vai bakteriūriju izraisījis akūts pielonefrīts vai ir kāds cits iemesls. Kaut gan par klīniski nozīmīgu koncentrāciju uzskata > 20 mg/l, pielonefrīta gadījumā skaitļi parasti ir lielāki. Normāli CRO skaitļi pielonefrītu izslēdz ar 80 % varbūtību. [30]
Izmeklēšanas algoritms
Tikai nelielam skaitam bērnu ar UCI ir kāds uroloģisks traucējums, bet, ja šādi traucējumi ir, tie var izraisīt nopietnus bojājumus. Tāpēc izmeklējumi jāveic jau pēc pirmās UCI epizodes (3. attēls).
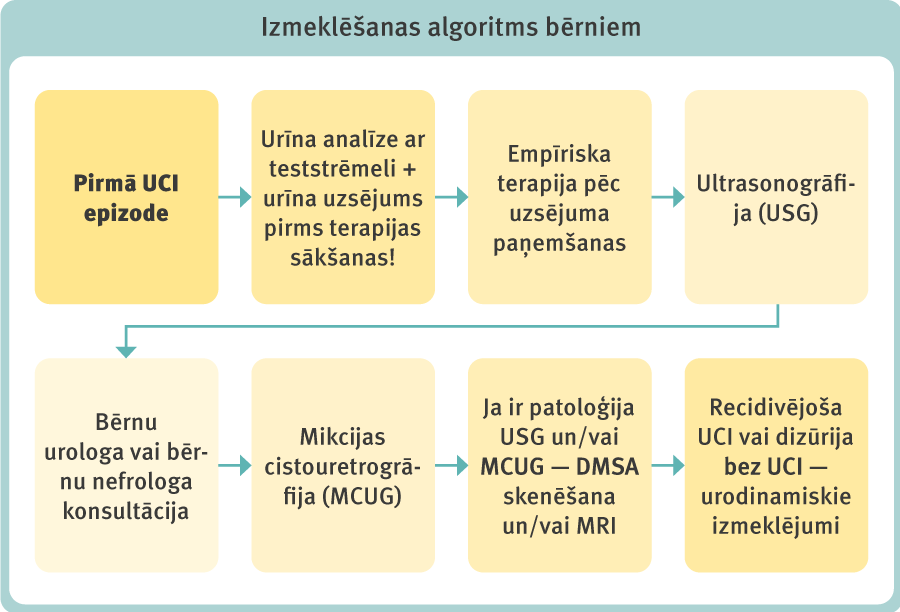

3. attēls
Izmeklēšanas algoritms bērniem
Izmeklēšanas metodes
Eiropas vadlīnijās (EAU Guidelines 2020) ieteikts veikt nieru un urīnpūšļa USG 24 stundu laikā visiem zīdaiņiem ar febrilu UCI, vecākiem bērniem — iespējami drīz.
MCUG (mikcijas cistouretrogrāfija) plānveidā veicama meitenēm un zēniem līdz viena gada vecumam pēc pirmās febrilās UCI epizodes, lai izslēgtu vezikoureterālu refluksu (VUR).
Bērniem ar patoloģisku atradi USG un/vai MCUG (VUR) plānveidā papildus var veikt DMSA skenēšanu (radionukleotīdu izmeklēšanu ar dimerkaptosukcinskābi jeb scintigrāfiju) vai MRI (magnētiskās rezonanses attēlveidošanas) izmeklējumu.
Urodinamiskie izmeklējumi plānveidā ieteikti visiem bērniem, kas apguvuši podiņa lietošanu, pēc febrilas UCI un recidivējošu UCI gadījumā, kā arī dizūrijas bez UCI gadījumā. Indikācijas attēldiagnostikas veikšanai, izņemot USG, vienmēr nosaka bērnu nefrologs vai bērnu urologs.
Empīriska UCI terapija
Empīrisku UCI terapiju bērniem sāk ar Furamags®, bērniem ar ķermeņa masu virs 30 kg deva ir 50 mg trīs reizes dienā (p/o). 1—10 gadus veciem bērniem deva ir 5 mg/kg/dnn, dienas devu sadalot divās vai trīs reizes devās. Ja dienas devu nevar sadalīt vienādās reizes devās, lielāko devas daļu lieto pirms naktsmiera. Bērniem līdz sešu gadu vecumam zāļu lietošana kapsulu veidā ir saistīta ar aizrīšanās risku, jo pilnīga rīšanas refleksa kontrole attīstās līdz sešu gadu vecumam. Lietojot bērniem līdz sešu gadu vecumam, kapsulas saturu ieteicams norīt pēc tās atvēršanas. Alternatīva varētu būt kotrimoksazols 10—20 mg/kg/dnn p/o (tikai tad, ja floras rezistence populācijā zem 20 %) vai cefuroksīms p/o 20—30 mg/kg/dnn.
Citi preparāti vai nu ir mazāk efektīvi rezistences dēļ (piemēram, amoksicilīns, amoksicilīns—klavulānskābe), vai pieejami tikai parenterāli, vai Latvijā vispār nav pieejami. Fluorhinoloni (piemēram, ciprofloksacīns) vairs nav lietojami UCI ārstēšanai rezistences un blakņu dēļ un paturami tikai kā rezerves antibiotikas. [30]
Cistīta ārstēšanai jāilgst vismaz septiņas dienas, pielonefrīta gadījumā 10—14 dienas. [31; 32] Ja pēc trim dienām klīniskās atbildes nav vai ja nav iespējama zāļu lietošana iekšķīgi, vai ja rodas komplikācijas, bērns jāstacionē, lai pārietu uz zāļu ievadi parenterāli.
Negatīvs uzsējums vai floras rezistence pret nitrofurantoīnu nav pamats empīriskās terapijas pārtraukšanai vai preparāta nomaiņai, ja pirmajās trīs dienās ir klīniska atbildreakcija. [33]
Bērnu UCI ārstēšanas principi
Četri ārstēšanas pamatmērķi:
- novērst simptomus un likvidēt akūtu bakteriūriju,
- novērst nieru rētu veidošanos,
- novērst UCI atkārtošanos,
- koriģēt saistītos uroloģiskos bojājumus.
Smagas gaitas urīnceļu infekcijas
Antibakteriālā terapija arī šajā gadījumā jāsāk empīriski, bet jaundzimušajiem un zīdaiņiem līdz divu mēnešu vecumam, kad urosepses risks un pielonefrīta smaguma pakāpe ir lielāka, ieteicama parenterāla terapija ar cefuroksīmu 75 mg/kg/dnn × 3 i/v kopā ar parenterālu šķidruma aizstājterapiju. Līdzko ir kultūras uzsējuma rezultāti, terapiju var pielāgot, ja no empīriskas terapijas trīs dienu laikā nav klīniskā efekta.
Urīnceļu infekciju recidīvu profilakse
Pacientiem ar atvilni un atkārtotām UCI ieteicams profilaktiski lietot mazas antibiotiku devas. [34] Šādu pieeju var izmantot arī pēc akūtas UCI epizodes, kamēr tiek pabeigts diagnostikas process. Izvēles preparāts ir Furamags® 1—2 mg/kg/dnn × 1 p/o pirms miega, alternatīva (ja ir floras jutība) — kotrimoksazols 5 mg/kg/dnn × 1 p/o pirms miega vai cefaleksīns 10 mg/kg/dnn × 1 p/o pirms miega. Ilgtermiņā Furamags® lietošana bērniem ir droša pat traucētu nieru funkciju gadījumā. [38]
Kopsavilkums par bērnu urīnceļu infekcijām
- UCI ir kombinēta diagnoze, kuras noteikšanu pamato klīniskā aina (simptomi un sūdzības), leikocitūrija un verifikācija ar bakteriūriju (urīna kultūru). Visi komponenti ir obligāti.
- Nav pieļaujams, ka UCI diagnozi nosaka tikai pēc dizūrijas un tāpēc ordinē antibiotikas!
- Nedz bakteriūrija, nedz leikocitūrija vai nitrītu analīzes izolēti nav uzskatāmas par uzticamiem kritērijiem UCI diagnosticēšanai vai izslēgšanai. Šie pacienti nav ārstējami ar antibiotikām, viņi nav arī papildus jāizmeklē.
- Obligāti jāpārbauda, vai nav fimozes, kaunuma lūpu saaugumu, pielonefrīta pazīmju, epididimoorhīta un spina bifida pazīmju.
- Drudža neesība neizslēdz infekcijas procesu.
- Vienlaicīga leikocitūrija un drudzis bērniem ar lielāko varbūtību norāda uz akūtu pielonefrītu.
- Urīna strūklas vidējā porcija ir pirmā izvēles metode bērna urīna parauga iegūšanai un, ievērojot rūpīgu higiēnu, der gan standarta urīna analīzei, gan uzsējumam.
- Urīnpūšļa katetrizācija ir otrā izvēles metode urīna uzsējuma iegūšanai. Ļoti jutīga, droša un efektīva metode, visizplatītākā pasaulē.
- Urīna paraugs jāanalizē nekavējoties, maksimālais laiks urīna parauga nogādāšanai laboratorijā ir viena stunda.
- Ja teststrēmeles rezultāti ir negatīvi, urīna mikroskopija un uzsējums nav nepieciešami un UCI var izslēgt.
- Jau pēc pirmās UCI epizodes bērns jāizmeklē.
- Ārstēšanas ilgums: vismaz septiņas dienas cistīta gadījumā, 10—14 dienas pielonefrīta gadījumā. Ja trīs dienu laikā klīniskās atbildes uz ārstēšanu nav vai rodas komplikācijas, bērns jāstacionē, lai medikamentus ievadītu parenterāli.
Fitoterapija
Tautas medicīnā augu izcelsmes produktus lieto plaši, arī UCI ārstēšanai un profilaksei, taču populārais izteiciens “viss, kas ir dabisks, ir drošs un labs veselībai” diemžēl nav patiess.
Pirmkārt, tie nav medikamenti un nav pakļauti stingrām efektivitātes un kvalitātes pārbaudēm. Otrkārt, augi nav pietiekami izpētīti, dažas aktīvās vielas to sastāvā un to iedarbība uz cilvēka organismu vēl nav zināma. Treškārt, daži augi lielās devās var būt kaitīgi vai pat indīgi. Ceturtkārt, augi var būt nesaderīgi ar medikamentiem. Piektkārt, augi, kas auguši brīvā dabā, var saturēt nesamērīgi daudz pesticīdu, smago metālu un citu kaitīgu vielu.
Noteikti jāpievērš uzmanība fitoterapijas preparātu izcelsmei un kvalitātei un jāatceras, ka nekas labs nemēdz būt lēts.
Dzērvenes
Pēdējos gados vislielāko popularitāti UCI gadījumā izpelnījušās dzērvenes. Diemžēl dzērveņu efektivitāte nav pierādīta ne UCI ārstēšanā, ne profilaksē. [39]
ASV institūcija National Center for Complementary and Integrative Health skaidri norāda, ka dzērvenes neārstē UCI un ka infekcijas jāārstē ar antibiotikām, un ka bērniem dzērveņu preparātus dot nevajag. [40]
Dzērvenes satur A tipa proantocianidīnus (PAC), kas varētu mazināt E. coli fimbriju pielipšanu uroepitēlijam, bet katra suga (Vaccinum macrocarpon — Amerikas dzērvene, Vaccinum oxycoccus — Eiropas dzērvene, Vaccinum vitis–idaea — brūklene) satur atšķirīgus PAC un to lietošanas rezultāti nav savstarpēji salīdzināmi.
Dzērveņu efekts ir tieši proporcionāls devai; [41] pozitīvs efekts novērojams tikai pēc ievērojama patēriņa (pieaugušo pētījumos dzērveņu sula lietota devās līdz četriem litriem dienā, kas atbilst sešiem kilogramiem dzērveņu!). Skaidrs, ka neviens cilvēks šādu dzērveņu daudzumu ikdienā patērēt nevar, turklāt jāņem vērā arī gremošanas trakta pārslodze ar skābēm un oksalātiem, nierakmeņu veidošanās risks, tāpēc tiek ražoti dzērveņu koncentrāti.
Viena CystiCran® 40 kapsula (ASV) satur dzērveņu koncentrātu 4800 : 1, kas ir ekvivalents 423 g dzērveņu un satur 36 mg PAC. Tātad dažas šādas kapsulas dienā it kā varētu nodrošināt vēlamo efektu, bet drošas devas bērniem nav noteiktas. Viena šāda kapsula maksās ap 2 € vai vairāk.
Kopsavilkums par fitoterapiju
Jebkāda fitoterapija (dzērveņu/brūkleņu sula/morss) UCI gadījumā var dot pozitīvu efektu, jo veicina diurēzi, mazinot baktēriju koncentrāciju urīnā un izvadot toksiskās vielas.
Vairākiem augiem piemīt arī pretsāpju, pretiekaisuma un spazmolītisks efekts, kas var atvieglot UCI simptomātiku. Rezumējot varētu teikt, ka fitoterapija UCI gadījumā kopumā atzīstama par pozitīvu, bet jāatceras, ka tā neaizstāj antibiotikas un lietojama tikai kā papildu metode.