
Tabula
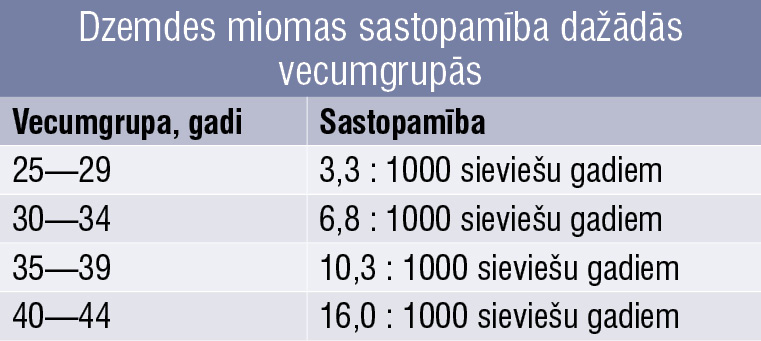
Dzemdes miomas sastopamība dažādās vecumgrupās
Dzemdes mioma ir monoklonāls labdabīgs audzējs, kas attīstās no miometrija gludās muskulatūras šūnām un fibroblastiem. Tā lielā daudzumā satur ekstracelulārās matrices komponentus (kolagēnu, proteoglikānus, fibronektīnu), un to iekļauj plāna pseidokapsula, kas veidota no saistaudiem un saspiestām muskuļšķiedrām. Dzemdes miomas cēloņi un patoģenēze nav skaidri izprasti. Tiek uzskatīts, ka nozīme ir ģenētiskai predispozīcijai, ārvides faktoriem, steroīdhormoniem, kā arī augšanas faktoriem, kuri ietekmē saistaudu veidošanās un angioģenēzes procesus.
Dzemdes miomas risku palielina iedzimtība, afroamerikāņu rase, lielāks dzemdību skaits, garāks laiks (vairāk nekā pieci gadi) pēc iepriekšējām dzemdībām, vecums virs 40 gadiem, menarhe pirms desmit gadu vecuma, arteriāla hipertensija, aptaukošanās, sarkanās gaļas un produktu ar augstu glikēmisko indeksu lietošana uzturā, alkohola lietošana, D vitamīna trūkums, pārmērīgs E vitamīna līmenis. [2]
Vairākumā gadījumu miomas mezgla augšana sākas no dzemdes ķermeņa daļas un tikai ~ 8 % gadījumu no dzemdes kakla daļas. Pēc miomas mezgla augšanas virziena izšķir intramurālus, subserozus, submukozus un intraligamentārus miomas mezglus.
![FIGO izstrādātā dzemdes miomu klasifikācija pēc miomas mezglu lokalizācijas un tipa [3]](https://cdn.doctus.lv/media/2024/03/2/original/4e1aaa660ba6.jpg)
![FIGO izstrādātā dzemdes miomu klasifikācija pēc miomas mezglu lokalizācijas un tipa [3]](https://cdn.doctus.lv/media/2024/03/2/original/4e1aaa660ba6.jpg)
1. attēls
FIGO izstrādātā dzemdes miomu klasifikācija pēc miomas mezglu lokalizācijas un tipa [3]
Šobrīd lieto Starptautiskās Ginekologu un dzemdību speciālistu federācijas (International Federation of Gynecology and Obstetrics, FIGO) miomas mezglu klasifikāciju un izšķir astoņus miomas mezglu veidus (1. attēls):
0. — uz kājiņas dzemdes dobumā;
1. — < 50 % intramurāls;
2. — ≥ 50 % intramurāls;
- citi tipi (intramurāli un subserozi):
3. — saistās ar endometriju; 100 % intramurāls;
4. — intramurāls;
5. — subserozs ≥ 50 % intramurāls;
6. — subserozs < 50 % intramurāls;
7. — subserozs uz kājiņas;
8. — cits (specifiska lokalizācija, piemēram, cervikāls);
2.—5. — subserozs un submukozs, ir iesaistīts kā endometrijs, tā peritonejs. [3]
Vairākumā gadījumu dzemdes mioma ir asimptomātiska, tāpēc to diagnosticē nejauši, veicot iegurņa izmeklēšanu. Simptomātiskas dzemdes miomas gadījumā pacientes sūdzības ir atkarīgas no miomas mezglu skaita, lieluma un lokalizācijas.
Miomas diagnostika
Anamnēze
Noskaidro sūdzības un simptomus, to ilgumu, smaguma pakāpi un ietekmi uz sievietes dzīves kvalitāti. Dzemdes miomas radītos simptomus iedala trīs grupās.
- Patoloģiska dzemdes asiņošana. Biežākā dzemdes miomas klīniskā izpausme. Patoloģiska dzemdes asiņošana raksturīga submukozi un intramurāli lokalizētiem dzemdes miomas mezgliem.
- Ar veidojumu saistītie simptomi:
- palpējams veidojums vēdera dobumā;
- sāpes vai spiediena sajūta iegurnī — pastāvīgs vai intermitējošs diskomforts, iespējamas arī sāpes mugurā, kā arī dispareīnija (sāpes dzimumakta laikā), biežāk subseroziem miomas mezgliem. Var būt akūtas sāpes vēderā, ko izraisa miomas mezgla deģenerācija, torsija vai dzimstošs miomas mezgls;
- blakus orgānu funkciju traucējumi — bieža urinācija, grūtības iztukšot urīnpūsli, var būt hidronefroze, aizcietējumi un tenesms. Urinācijas traucējumi raksturīgi dzemdes priekšējās sienas apakšējā trešdaļā lokalizētiem intramurāliem vai subseroziem mezgliem, savukārt vēdera izejas traucējumus rada miomas mezgli dzemdes mugurējā sienā;
- venoza kompresija — palielina venozas trombembolijas risku.
- Reproduktīvā disfunkcija: dzemdes miomas mezgli, kas deformē dzemdes dobumu (submukozas vai intramurālas miomas ar intrakavitāru komponentu), var būt neauglības cēlonis un palielināt spontāna aborta risku. Dzemdes mioma saistīta ar tādiem grūtniecības sarežģījumiem kā placentas atslāņošanās, augļa iegurņa priekšguļa vai šķērsguļa, priekšlaicīgas dzemdības.
Vispārējā apskate
Novērtē pacientes vitālos rādītājus un ādas krāsu, veic vēdera palpāciju.
Ginekoloģiskā izmeklēšana
- Apskate spoguļos — iespējams precizēt asiņošanas cēloni un diagnosticēt dzimstošu miomas mezglu vai dzemdes kakla miomu.
- Bimanuālā palpācija — nosaka dzemdes izmēru, kontūru deformāciju, konsistenci un kustīgumu. Palielināta, kustīga dzemde ar neregulārām kontūrām var liecināt par dzemdes miomu. Dzemdes lielums tiek noteikts grūtniecības nedēļās. Tā, piemēram, dzemde, kas palpējama līdz nabai, atbilst 20 grūtniecības nedēļām, savukārt dzemde, kas atrodas starp simfīzi un nabu, atbilst 16 grūtniecības nedēļām.
Laboratoriskā izmeklēšana
Nozīmīga diferenciāldiagnostikai, piemēram, sāpju vai patoloģiskas dzemdes asiņošanas gadījumā, lai izslēgtu grūtniecību. Pacientēm ar patoloģisku dzemdes asiņošanu jāizvērtē hemoglobīna līmenis anēmijas diagnostikai. Ja ir aizdomas par ļaundabīgu endometrija slimību, ginekoloģiskās apskates laikā jāveic endometrija aspirācijas biopsija.
Radioloģiskā un endoskopiskā diagnostika

2. attēls
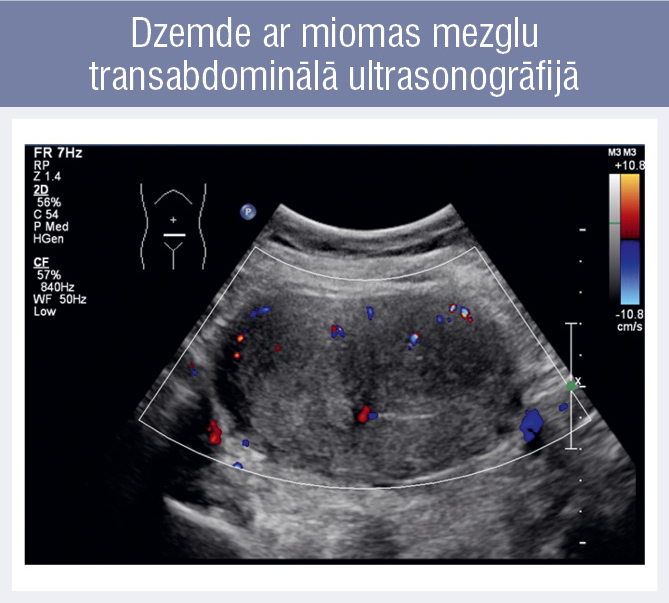
Dzemde ar miomas mezglu
transabdominālā ultrasonogrāfijā
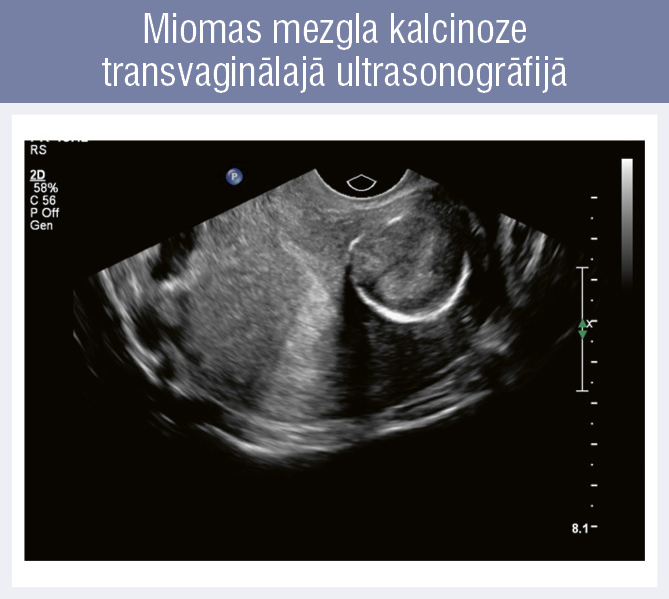
- Ginekoloģiskā ultrasonogrāfija — nosaka dzemdes lielumu, mezglu lokalizāciju, skaitu, mezglu struktūru. Lai iegūtu pilnīgu priekšstatu par miomas mezglu skaitu un lokalizāciju, jāveic gan transvagināla, gan abdomināla ultrasonogrāfija (2. attēls, 3. attēls).
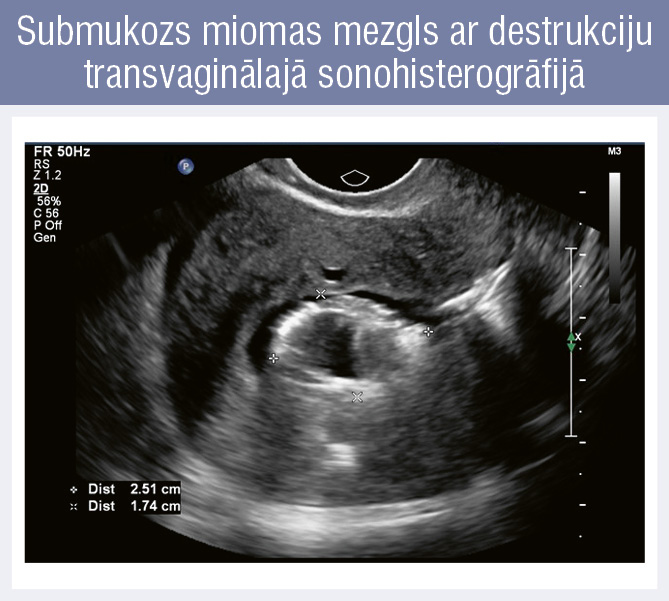
- Transvaginālā sonohisterogrāfija — ievadot dzemdes dobumā fizioloģisko šķīdumu, var labāk izvērtēt dzemdes dobuma kontūras un endometriju, īpaši, ja jāveic diferenciāldiagnostika vai nu starp endometrija hiperplāziju, endometrija polipu un submukozu miomas mezglu, vai arī starp endometrija polipu un submukozu miomas mezglu (4. attēls).
- Histeroskopija — dzemdes dobuma apskate ar endoskopu palīdz diferencēt endometrija polipu no submukoza miomas mezgla, ir iespējama tālāka ķirurģiska ārstēšana.

3. attēls
Miomas mezgla kalcinoze
transvaginālajā ultrasonogrāfijā
- Magnētiskā rezonanse — noderīga metode miomas mezgla lieluma un lokalizācijas noteikšanai. Ļauj diferencēt dzemdes miomu no citām dzemdes patoloģijām — dzemdes adenomiozes un endometrija vēža. Ņemot vērā izmeklējuma izmaksas un pieejamību, to rekomendē veikt gadījumos, ja paredzama komplicēta ķirurģiska ārstēšana, tiek plānota dzemdes artērijas embolizācija vai nepieciešams diferencēt dzemdes miomu no dzemdes sarkomas, lai gan pilnībā sarkomu no miomas var diferencēt tikai ar miomas audu histoloģiskā izmeklējuma palīdzību.
- Kontrasta magnētiskā rezonanse, magnētiskās rezonanses spektroskopija — izmanto miomas un sarkomas diferenciāldiagnostikai. [4]
Pieeja miomas ārstēšanā

4. attēls
Submukozs miomas mezgls ar destrukciju transvaginālajā sonohisterogrāfijā
Taktika dzemdes miomas gadījumā ir individuāla un atkarīga no simptomiem, mezglu lieluma un lokalizācijas, citām dzemdes slimībām, sievietes vecuma, grūtniecības plāniem, vēlmes saglabāt dzemdi, ārsta pieredzes un ārstēšanas pieejamības.
Taktika, ja pacientei ir asimptomātiska dzemdes mioma
Pacientēm ar asimptomātisku dzemdes miomu rekomendējama nogaidoša taktika. Šādā gadījumā novērošanu veic ik 6—12 mēnešus. Papildu izmeklēšana un ārstēšana nepieciešama, ja mioma aug strauji (tilpums sešos mēnešos palielinās par 20 %) vai ir papildu aizdomas par onkoloģisku iegurņa slimību.
Nogaidošu taktiku rekomendē, ja:
- dzemdes mioma ir asimptomātiska,
- paciente šobrīd dzīvo dzimumdzīvi bez izsargāšanās un vēlas palikt stāvoklī,
- miomas izmērs gada laikā nav palielinājies (ir veikti attēldiagnostikas izmeklējumi, lai to apstiprinātu),
- ir perimenopauzes vai postmenopauzes periods,
- dzemde nav abdomināli palpējama.
Nogaidoša taktika ietver:
- pacientes novērošanu un simptomu izvērtēšanu, kas varētu būt saistīti ar dzemdes miomu,
- miomas tilpuma novērtēšanu dinamikā ar ultrasonogrāfijas vai magnētiskās rezonanses izmeklējumiem,
- anēmijas izvērtēšanu laboratoriski,
- pacientes informēšanu par iespējamo slimības gaitu un tālāko ārstēšanās procesu.
Ja pacientei nav jaunu traucējošu sūdzību, ginekologa apmeklējums rekomendējams reizi gadā. [5]
Taktika, ja pacientei ir simptomātiska dzemdes mioma
Terapijas taktika tiek piemērota katrai pacientei individuāli. Ārstēšanas mērķis ir uz pacienti vērsta aprūpe: paciente tiek izglītota par terapijas metožu priekšrocībām un trūkumiem, kopā ar ārstu tiek izraudzīta iespējami labākā terapijas taktika. Indikācijas dzemdes miomas ārstēšanai:
- ir simptomi (patoloģiska dzemdes asiņošana, blakus orgānu funkciju traucējumi, reproduktīva disfunkcija),
- liels izmērs: > 12 grūtniecības nedēļām,
- strauja dzemdes miomas augšana,
- aizdomas par onkoloģisku procesu. [10]
Miomas ārstēšana var būt medikamentoza, ķirurģiska, izmantojot radioloģiskās metodes.
Medikamentoza ārstēšana
Lieto noteiktu laiku, lai atvieglotu ar miomu saistītos simptomus, kā arī pirms ķirurģiskas terapijas.
- Biežāk izmanto kombinēto hormonālo kontracepciju (kombinēto perorālo kontracepciju, maksts riņķi, transdermālos plāksterus) vai progestīnu saturošus kontracepcijas līdzekļus pacientēm, kuras vēlas arī kontracepciju. Tā neietekmē dzemdes miomas mezglu izmēru, tomēr mazina dzemdes asiņošanas apjomu un tādējādi arī dzelzs deficīta anēmiju.
- Progestīnu saturošā intrauterīnā hormonālā sistēma neietekmē miomas izmēru, taču mazina patoloģisku dzemdes asiņošanu, un to var lietot pacientes, kurām kontrindicēta kombinētā hormonālā kontracepcija. Pacientēm ar submukoziem miomas mezgliem ir paaugstināts dzemdes spirāles ekspulsijas risks.
- Antifibrinolītiskus līdzekļus — traneksāmskābi — var lietot menstruāciju laikā, lai mazinātu spēcīgu asiņošanu. Šī metode piemērota pacientēm, kas nevēlas lietot hormonālo kontracepciju vai vēlas medikamentus lietot tikai tad, kad tiek novēroti simptomi.
- Gonadotropie atbrīvotājhormona (GnRH) agonisti — triptorelinum acetas, goserelinum acetas, leuprorelini acetas — ir indicēti simptomātiskas miomas gadījumā, lai koriģētu pārmērīgi stipru asiņošanu. Tie pieejami kā deguna aerosoli, zemādas vai i/m injekcijas. Lieto pirms iespējamās mezglu enukleācijas vai histerektomijas olnīcu hormonu nomākšanai, lai mazinātu miomas apjomu un simptomus. Lietošanas ilgums 3—6 mēneši. Medikamentus var lietot kombinācijā ar steroīdhormoniem mazās devās, lai mazinātu ar estrogēnu trūkumu saistītos simptomus.
- GnRH antagonisti ar papildinošo terapiju — piemēram, relugolixum ar estradiolum — vidēji smagu vai smagu miomas simptomu korekcijai sievietēm reproduktīvā vai pirmsmenopauzes vecumā. Tā ir kā medikamentoza pāreja uz menopauzi bez ķirurģiskas iejaukšanās. Terapija piemērota ilgstošai lietošanai, aptur miomas augšanu, iespējama ātra pārmērīgi stipras asiņošanas un sāpju korekcija, miomas apjoms var samazināties par ~ 20 %.
- Selektīvie progesterona receptoru modulatori (SPRM) darbojas uz receptoriem gan kā GnRH agonisti, gan kā antagonisti, tādējādi samazinot asiņošanu un veicinot miomas mezglu sarukšanu.
- Ulipristāla acetāts (ulipristalum, UPA) indicēts vidēji smagu vai smagu miomas simptomu ārstēšanai sievietēm reproduktīvā un pirmsmenopauzes periodā. UPA samazina dzemdes miomas izmēru un saistītos simptomus. UPA lietošana var radīt smagus aknu bojājumus un nepieciešamību veikt aknu transplantāciju, tāpēc to lietot šobrīd neiesaka.
- Mifepristonum, lietojot 3—6 mēnešus, samazina patoloģisku dzemdes asiņošanu un miomas izmēru, taču atsevišķos gadījumos var radīt izmaiņas endometrijā.
- Danazolum ir sintētiskais steroīds, kas nomāc gonadotropīnu darbību un miomas mezglu izmēru samazina par 20—25 %. Izteiktā androgēnu efekta dēļ lieto ļoti reti. [5; 7; 11]
Ķirurģiska ārstēšana
Optimālākā ārstēšanas metode ir atkarīga no pacientes vēlmēm, dzemdes miomas mezglu izmēra un skaita.
- Histerorezektoskopiska miomektomija — izvēles metode submukoza dzemdes miomas mezgla (0.—2. tips pēc FIGO klasifikācijas) ārstēšanai. Tā ir minimāli invazīva ķirurģiska operācija, kas piemērota, ja nav nepieciešama abdomināla pieeja citas lokalizācijas miomas mezgla rezekcijai un nav kontrindikāciju šai ārstēšanas metodei, piemēram, iegurņa iekaisuma slimība. Liels miomas mezgls ar platu pamatni vai intramurālu komponentu palielina perioperatīvo komplikāciju risku. Ja dzemdes dobumā ir multiplas un lielas (> 3 cm) miomas uz platas kājiņas un/vai liela daļa miomas mezgla lokalizēta miometrijā, paciente ir jāinformē, ka var būt nepieciešams operācijas otrais etaps. Atkārtotas operācijas nepieciešamību izvērtē kontroles vizītē 2—4 mēnešus pēc pirmās operācijas.
- Laparoskopiska miomektomija — piemērota dzemdes miomai, kas ir subseroza vai intramurāla. Kontrindikācijas laparoskopiskai miomektomijai ir dažādu lokalizāciju multipli miomas mezgli (jo nepieciešamas vairākas incīzijas), aizdomas par sarkomu un intramurāls mezgls, kura diametrs pārsniedz 10—12 cm.
- Laparotomiska miomektomija — pārsvarā veic intramurālam vai subserozam miomas mezglam. Šo metodi var izmantot arī tad, ja ir mioma ar intrakavitāru komponentu (submukozs intramurāls vai submukozs mezgls), tomēr tā nav pirmās izvēles metode, jo atveseļošanās ilgāka un pacientes perioperatīvā saslimstība biežāka.
- Histerektomija — iespējams veikt gan laparoskopiski, gan laparotomiski, gan vagināli. Operācijas apjoms var būt gan subtotāla histerektomija, gan totāla histerektomija ar vai bez piedēkļiem. Ja pacientei ar multipliem miomas mezgliem sūdzības rada vairāk nekā viens mezgls un viņa neplāno grūtniecību, tad rekomendē veikt histerektomiju. [5; 13; 15]
Radioloģiskas ārstēšanas metodes
Dzemdes artērijas (a. uterina) embolizācija — veic rentgenoloģiskā kontrolē ar polivinila mikrolodītēm, kas nonāk līdz dzemdes miomu barojošajiem asinsvadiem un tos okludē, tā izraisot miomas mezgla nekrozi. Salīdzinot ar abdominālu histerektomiju vai miomektomiju, šai minimāli invazīvajai metodei ir mazāks hemotransfūzijas risks, īsāka hospitalizācija, mazāks sāpju sindroms, ātrāka atgriešanās ikdienas dzīvē. Metodes priekšrocība — tā nav atkarīga no miomas mezglu skaita, nav nozīmīgu intraabdominālu saaugumu. Nerekomendē veikt pacientēm, kurām dzemde lielāka par 20 grūtniecības nedēļām.
Kontrindikācijas dzemdes artērijas embolizācijai var būt absolūtas: asimptomātiski miomas mezgli, grūtniecība, iegurņa iekaisuma slimība, ļaundabīgs dzemdes ķermeņa audzējs, kā arī relatīvas: nākotnē tiek plānota grūtniecība (nav pārliecinošu datu, ka dzemdes artēriju embolizācija nelabvēlīgi ietekmē grūtniecību nākotnē, taču tiek uzskatīts, ka tā pasliktina dzemdes perfūziju, savukārt tas var ietekmēt auglību un veicināt grūtniecības komplikācijas), pēcmenopauze, subserozi vai submukozi miomas mezgli ar tievu kājiņu (< 50 % no miomas izmēra), samazināts glomerulu filtrācijas ātrums, alerģija pret kontrastvielu.
Magnētiskās rezonanses vai ultrasonogrāfijas vadīta fokusēta ultraskaņas terapija. Audos inducē koagulācijas nekrozi. Metode izmantojama ambulatoros apstākļos. Procedūru neiesaka veikt, ja ir pieci un vairāk miomas mezgli, maksimālais miomas mezgla diametrs pārsniedz 10 cm, miomas mezgli ir slikti vaskularizēti vai ar kalcinātiem vai tos iespējams rezecēt. [5; 11; 13]