Slimības patoģenēze
Pēdējo gadu laikā arvien lielāka uzmanība tiek pievērsta psoriāzes molekulārās ģenētikas izpētei. Konstatēts, ka ģenētiski psoriāze ir poligēna slimība. Tai raksturīgs individuāls polimorfisms, kas atkarīgs no dažādas gēnu kombinācijas psoriāzei jutīgajā apvidū 6. hromosomā. Šeit lokalizēto gēnu kopumu dēvē par PSORS1 gēniem, no kuriem īpaši uzsvērti tiek HLA-C un korneodesmosīna gēni. [2] Psoriātiskā artrīta gadījumā ir konstatēta saistība ar MICA gēnu. [3] Psoriāzes ģenētika joprojām aktīvi tiek pētīta, atklājot arvien jaunus iespējamos izraisītājgēnus un to kombinācijas.
Arvien aktīvāk pēta psoriāzes saistību ar citām patoloģijām, īpaši kardiovaskulārajām un endokrinoloģiskajām slimībām. [4] Kā savstarpēji saistošie iemesli tiek aplūkoti tradicionālie riska faktori: aptaukošanās, dislipidēmija, smēķēšana, alkohola lietošana un stress, kā arī tādi patoloģiskie procesi kā endoteliālā disfunkcija un iekaisums. Ir zināms, ka metotreksāta lietošana psoriāzes pacientiem spēj mazināt vaskulāro slimību incidenci.
Psoriāze ir prototipiska Th-1 iekaisīga dermatoze ar raksturīgu Th-1 šūnu, antigēnus prezentējošo šūnu un Th-1 citokīnu klātbūtni audos. Hroniskam Th-1 iekaisumam ir svarīga nozīme metabolā sindroma, aptaukošanās, aterosklerozes un miokarda infarkta patoģenēzē. Piemēram, cirkulējošo Th-1 citokīnu, adhēziju molekulu kā E-selektīns, angioģenētisko faktoru kā vaskulārā endotēlija augšanas faktora līmenis ir paaugstināts gan psoriāzes, gan koronāro artēriju slimību un aptaukošanās gadījumā. [5] Šie iekaisuma mediatori ietekmē tādus procesus kā angioģenēze, insulīna izdale, adipoģenēze, lipīdu metabolisms, epidermas proliferācija. Pašlaik ir pierādīts, ka psoriāzes pacientiem ir lielāks risks dzīves laikā saslimt ar cukura diabētu [6] un kādu no kardiovaskulārajām slimībām. [7]
Ārstēšana
Pēdējos gados ievērojami mainījusies ne tikai izpratne par psoriāzes patoģenēzi, bet arī šīs slimības ārstēšana. Ir parādījušies jauni lokālās terapijas un sistēmiskās terapijas līdzekļi. Īpaši jāuzsver bioloģiskās terapijas ieviešana klīniskajā ikdienas praksē. Tomēr joprojām jāatceras, ka psoriāze ir sarežģīta, hroniska slimība, kas pavada pacientu visas dzīves garumā. Par spīti moderniem ārstēšanas līdzekļiem tā joprojām netiek uzskatīta par pilnībā izārstējamu.
Sadarbība starp ārstu un pacientu
Veiksmīgas ārstēšanas noslēpums ir cieša sadarbība starp pacientu un ārstu. Konstatēts, ka pacienti nogurst no regulāras un precīzas parakstīto medikamentu lokālas aplikācijas. Tikai aptuveni 60% pacientu cenšas precīzi izpildīt ārsta norādījumus. Kā galvenos nesadarbošanās iemeslus viņi min vilšanos medikamentu efektivitātē un bailes no to radītajām blaknēm.
Citi minētie iemesli ir medikamentu izmaksas, nepatīkama vai neērta to lietošana, neskaidras lietošanas instrukcijas. [8]
Lai veicinātu ārsta un psoriāzes pacientu sadarbību, visā pasaulē tiek dibinātas psoriāzes pacientu pašpalīdzības biedrības, kuru mērķis ir informēt pacientus par slimības norisi, ārstēšanu, sagaidāmiem rezultātiem. Liela nozīme ir pacientu savstarpējai pieredzes apmaiņai, kas veicina reālu izpratni par psoriāzi. Arī mūsu valstī darbojas Latvijas Psoriāzes biedrība (www.psoriasis.lv). Latviešu valodā pieejama informatīva psoriāzes mājaslapa, ko izstrādājusi Dānijas kompānija LeoPharma, kas šobrīd ir starp vadošajiem pētniekiem jaunu psoriāzes medika men tu iz pētē (www.psor info.com). Šīs mājaslapas vadmotīvs - iemācīt veiksmīgi sadzīvot ar psoriāzi.
Novitātes ārstēšanā
Lai gan ir dažādas novitātes terapijā, galvenie ārstēšanas metožu izvēles principi saglabājušies nemainīgi. Joprojām izšķiram lokālo, sistēmisko un kombinēto terapiju. Ārstēšanas izvēlē jāņem vērā:
- pacients: vecums, vispārējais veselības stāvoklis, blakus slimības, līdzesība ārstēšanā;
- psoriāze: klīniskā aina, smaguma pakāpe, lokalizācija;
- medikaments: forma, efektivitāte, blaknes, izmaksas;
- ārsts: pieredze darbā ar konkrēto slimību un medikamentu.
Psoriāzes smaguma pakāpes, to izvērtēšana
Pirms izšķirties par medikamenta izvēli psoriāzes paasinājuma kupēšanai, ļoti svarīgi ir izvērtēt psoriāzes smaguma pakāpi. Ir pieņemts psoriāzi iedalīt viegli, vidēji smagi un smagi noritošā.
Pašlaik pasaulē izšķir vairākas smaguma pakāpes izvērtēšanas shēmas. Klīniskajā praksē vispiemērotākā ir ķermeņa virsmas skartā laukuma shēma jeb BSA (Body Surface Area, max 100%). Šajā gadījumā tiek pieņemts, ka pacienta plauksta ir 1% no kopējā BSA.
Amerikas Psoriāzes biedrības dati
Pēc Amerikas Psoriāzes biedrības datiem, psoriāzi par viegli noritošu uzskata, ja BSA ir līdz 3%. Šajā gadījumā kā monoterapiju iespējams izvēlēties lokālu ārstēšanu.
Ja BSA ir robežās no trim līdz 10%, tad psoriāze ir vidēji smagi noritoša.
Ja BSA ir virs 10% - smagi noritoša psoriāze. Šajos gadījumos piemērotāka ir kombinētā terapija.
Izņēmums BSA izvērtēšanā ir pēdu un plaukstu psoriāze, kad jau 1-2% BSA var tikt uzskatīti par smagu šīs psoriāzes formas izpausmi.
PASI indekss
Otra psoriāzes smaguma pakāpes izvērtēšanas shēma ir PASI indekss (Psoriasis Area Severity Index, max 72,0, kas atbilst 100% BSA), ko aprēķina pēc noteiktām formulām, tāpēc ikdienas praksē šī nav ērti lietojama shēma. Tā galvenokārt tiek izmantota pētījumos psoriāzes objektīvai dokumentēšanai. Ja PASI ir līdz 7,0, tad psoriāze ir viegli noritoša; ja PASI ir no 7,0 līdz 12,0 - vidēji smagi noritoša psoriāze; PASI > 12,0 - smagi noritoša psoriāze. Populārs ir t. s. "desmitnieka likums", kad psoriāzi uzskata par smagi noritošu, ja BSA > 10%; PASI > 10%; DLQI (Dermatology Life Quality Index, 0-30) > 10.
Lokālā terapija
Kad precīzi noteikta psoriāzes smaguma pakāpe, varam izvēlēties atbilstīgu terapiju, proti, vieglai formai lokālā terapija kā monoterapija, bet vidēji smagai un smagai - kombinētā terapija, kur ietilpst savstarpēja lokālās terapijas, fototerapijas, sistēmiskās terapijas kombinēšana katram pacientam individuāli.
Veiksmīgu terapijas iznākumu nosaka ārsta prasme izprast psoriāzes patoģenētiskos procesus katram pacientam (do mi nē paātrināta šūnu dalīšanās, nenormāla keratinizācija vai asinsvadu paplašināšanās), piemeklējot visatbilstīgākos medikamentus. Ņemot vērā faktu, ka šādu medikamentu ir daudz, psoriāzes ārstēšanu var aplūkot kā mākslu, kad iznākums atkarīgs no pieejas radošuma.
Pirmās izvēles medikamenti
Lokālajā terapijā ir īpaši liels klāsts dažādu medikamentu. Īsi par pirmās izvēles preparātiem.
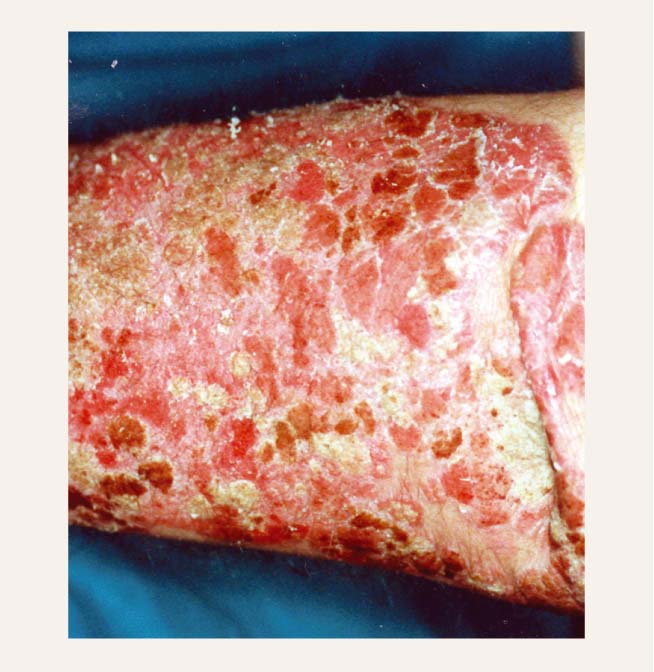

1. attēls
Psoriāzes pāpula pirms ziedes aplicēšanas
- Lokālie jeb topiskie steroīdi. Pēc spējas sašaurināt asinsvadus jeb Makenzija indeksa tos iedala septiņās stipruma grupās. Stipras darbības - I, II; vidējas darbības - III, IV, V; vieglas darbības - VI, VII. Vājas darbības steroīdi jāizvēlas bērniem vai sejas psoriāzes gadījumā. Vidējas un stipras darbības steroīdi piemēroti ķermeņa un ekstremitāšu psoriāzes ārstēšanai. Svarīga ir medikamenta forma (losjons, krēms, ziede). Ādas krokās, plānas ādas apvidos izvēle ir vājāki steroīdi krēmu veidā, lai izvairītos no blaknēm (ādas lokāla atrofija, teleangiektāzija, hipotalāma-pituitārās ass supresija u. c.). Ādas krokām savstarpēji saskaroties, rodas dabīga oklūzija, kas spēj paaugstināt to pisko steroīdu potenci par desmit līdz 100 reizēm. [9] Ilgstoši (divus līdz četrus mēnešus) lietojot steroīdus, attīstās pieradums jeb tahifilakse. [10]
- Kalcipotriols - vitamīna D analogs, kas mazina šūnu proliferāciju, palielina keratinocītu diferenciāciju. Lieto divas reizes dienā, ilgstoši. Lēna iedarbība - maksimālais efekts pēc divu mēnešu regulāras lietošanas. Nav raksturīga tahifilakse. Maz blakņu (lokāls kairinājums, hiperkalciēmija).
- Tazarotēns - vienīgais lokālais sintētiskais retionīds psoriāzes ārstēšanai; Latvijā nav pieejams.
- Kombinētā lokālā terapija. Pēdējos gados parādījusies jauna pieeja kombinētai lokālai medikamentu indicēšanai, ko dēvē par sekvencionālo terapiju. Šīs ārstēšanas būtība slēpjas ātras iedarbības medikamentu īslaicīgā nozīmēšanā psoriāzes paasinājuma kupēšanai un sasniegtā regresa uzturēšana ar lēnākas iedarbības, bet mazāk bīstamiem medikamentiem. Pašlaik Latvijā ļoti populāra sekvencionālās terapijas shēma ir kombinētā preparāta - steroīda betametazona dipropionāta un kalcipotriola - lietošana vienu reizi dienā psoriāzes progresīvajā stadijā (aptuveni divas līdz četras nedēļas- skat. 1. un 2. attēlu). Sasniedzot stacionāro stadiju, ziedi nozīmē vienu reizi dienā tikai nedēļas nogalēs. Darbdienās divas reizes dienā tiek aplicēta kalcipotriolu saturoša ziede. Šis medikaments- atšķirībā no kortikosteroīdus saturošajiem preparātiem - iedarbojas lēnām, bet pārliecinoši un bez ievērojamām blaknēm. Tas nerada ādas atrofiju, tāpēc ir piemērots ilgstošai lietošanai. Kalcipotriolu saturošu ziedi turpina indicēt arī regresijas stadijā. Jāatceras, ka kalcipotriola kopējais daudzums nedrīkst pārsniegt 100 g nedēļā, jo tādējādi rodas hiperkalciēmijas risks.
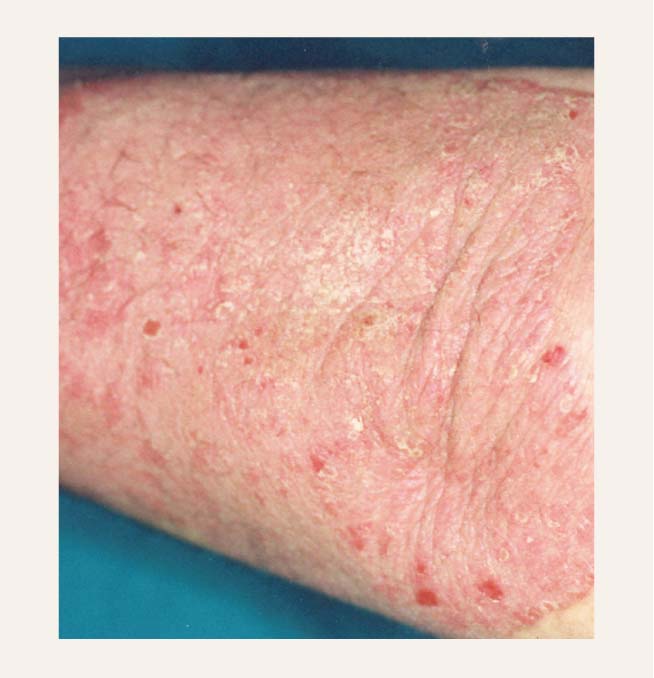

2. attēls
Psoriāzes pāpula četras nedēļas pēc ziedes aplicēšanas
Otrās izvēles medikamenti
Otrās izvēles lokālie medikamenti ir salicijskābe, lokālie kalcineirīna inhibitori, darvas preparāti, antralīns, mitrinoši līdzekļi, kurus izvēlas papildus pirmās līnijas medikamentiem - atkarībā no klīniskās ainas un dominējošā patoloģiskā procesa.
Ir svarīgi iemācīt pacientam precīzi aprēķināt aplicējamā medikamenta daudzumu. Nepieciešamais ziedes daudzums ir 0,5 g uz 300 cm2 (divu plaukstu laukums). 0,5 g ziedes no tūbiņām, kuru atveres diametrs ir 5 mm, atbilst 2 cm garai līnijai jeb rādītājpirksta gala falangas garumam (pirkstgala vienība). Ar 30 g ziedes var noklāt visu ķermeņa virsmu. Piemēram, ja psoriāze skar pilnībā abas rokas (BSA = 18%), nepieciešama piektdaļa jeb 20% no 30 g (6 g) katru dienu. Vienam mēnesim būtu nepieciešami 180 g ziedes.
Pēc Amerikas Dermatoloģijas akadēmijas datiem, aptuveni 70% psoriāzes pacientu ASV tiek ārstēti tikai lokāli, bet 30% gadījumu izvēlās lokālo terapiju kombinācijā ar fototerapiju un/vai sistēmisko terapiju. [11]
Kombinētā terapija
Gadījumos, ja lokālā monoterapija nav pietiekami efektīva vai ja ir smaga psoriāzes gaita, jāpāriet uz kombinēto terapiju.
Fototerapija
Parasti iesaka sākt ar fototerapiju, kad var izmantot ultravioletos B viļņus (UVB [], plaša spektra BB-UVB vai mūsdienās populārākos šaura spektra NB-UVB); ultravioletos A viļņus (parasti kombinācijā ar fotosensibilizatoru psoralēnu kā PUVA metodi); Excimer lāzeru (308 nm); fotodinamisko terapiju.
Ir pierādīts, ka ultravioletais starojums (UV) var izraisīt T šūnu apoptozi, DNS, prostoglandīnu un citokīnu sintēzes supresiju. [12] Vieglu psoriāzes formu gadījumā var izmantot NB-UVB terapiju kā monoterapiju, tomēr biežāk fototerapiju kombinē gan ar lokāli, gan arī sistēmiski lietojamiem medikamentiem. Piemēram, NB-UVB kombinācija ar antralīnu, kalcipotriolu vai tazarotēnu ir efektīvāka nekā šo metožu monoterapija. [13]
Jāatceras, ka fotoderapijai ar UV stariem ir arī kontrindikācijas. Absolūtās kontrindikācijas ir xeroderma pigmentosum, sistēmis kā sarkanā vilkēde, bazālo šūnu nēvusu sindroms.
Relatīvās kontrindikācijas ir fotosensitivitāte, fotodermatozes, ādas vēzis anamnēzē. Ir pierādīta PUVA spēja paaugstināt ādas ne-melanomas audzēju risku, kas netika apstiprināta UVB terapijas pacientiem. [14]
Lai izvairītos no veselās ādas pakļaušanas nevēlamam UV starojumam, pasaulē arvien plašāk tiek izmantots skartajiem laukumiem piemērojams ultravioleto viļņu Excimer lāzers, kas dārgo izmaksu dēļ pašlaik Latvijā diemžēl nav pieejams.
Sistēmiskā medikamentozā terapija
Sistēmisko medikamentozo terapiju izvēlas vidēji smagas un smagas psoriāzes gadījumā, kad ar lokālo terapiju un fototerapiju nav iespējams panākt slimības uzliesmojuma kupēšanu. Arī sistēmiskajā ārstēšanā izmantojamie medikamenti tiek iedalīti pirmās un otrās izvēles līdzekļos. Visbiežāk lietojamie pirmās līnijas preparāti ir metotreksāts, ciklosporīns un acitretīns. Par otrās līnijas preparātiem pašlaik tiek uzskatīti bioloģiskie aģenti.
Metotreksāts ir imūnsupresants, kuru psoriāzes ārstēšanā izmanto jau kopš 1970. gadiem. Tas ir folskābes anatagonists, kas spēj kavēt šūnu pārmērīgu proliferāciju, inhibējot aminoskābju un DNS sintēzi. Lai gan tiek bremzēti patoloģiski pārmainītie limfocīti un keratinocīti, tomēr paralēli cieš arī citu orgānu šūnas, un tas rada nevēlamu metotreksāta izraisītu toksisko bojājumu. Īpaši toksisks šis preparāts ir aknām un kaulu smadzenēm. Tāpēc - lai gan metotreksāts rada ātru un pārliecinošu rezultātu - to indicē vienīgi gadījumos, kad citas terapijas nesniedz pietiekamu efektu, turklāt to vēlams lietot tikai paasinājumu īslaicīgai kupēšanai. Kopīgā metotreksāta deva nedrīkst pārsniegt 2000 mg dzīves laikā. Lietojot šo preparātu, regulāri ir jākontrolē asinsaina, aknu enzīmu testi. Ja alanīna aminotransferāzes līmenis pārsniedz normu vairāk nekā trīs reizes, metotreksāta lietošana jāpārtrauc.
Parasti metotreksātu ordinē perorāli. Nedēļas deva ir 7,5-15 mg. Parasti iesaka šo devu sadalīt trijās daļās ar 12 stundu intervālu. Šī kārtība samazina nevēlamas blaknes (slikta dūša, anoreksija, nogurums, trombocitopēnija, leikopēnija, anēmija, pneimonija). Ieteicams paralēli metotreksātam lietot folijskābi, lai izvairītos no folijskābes nepietiekamības. [15]
Ciklosporīns ir ļoti iedarbīgs imūnsupresants, kas inhibē T šūnu aktivāciju un proliferāciju. To var izmantot vidējas un smagas psoriāzes pacientiem, tomēr ir jāatceras, ka ciklosporīns ir nefrotoksisks un var izraisīt nieru mazspēju. Tas piemērots smagu psoriāzes uzliesmojumu īslaicīgai kupēšanai (deva 2,5-5 mg/kg diennaktī). [16]
Acitretīns ir sintētiskais retionīds, kas ietekmē šūnu diferenciāciju. Īpaši piemērots plaukstu pustulārās psoriāzes gadījumā. Acitretīns nav tik efektīvs kā metotreksāts, tomēr to var lietot kombinācijā ar lokāliem steroīdiem un fototerapiju, lai paaugstinātu tā efektivitāti. Jāatceras, ka acitretīns ir izteikti teratogēns. [17]
Bioloģiskie aģenti
Pēdējās desmitgades laikā psoriāzes terapijā parādījušies jauni, daudzsološi preparāti - bioloģiskie aģenti. Tie tika radīti ar mērķi nodrošināt selektīvu, imunoloģisku psoriāzes ārstēšanu bez nevēlamām blaknēm, kādas raksturīgas citiem prebioloģiskiem imūnsupresantiem. Bioloģiskie aģenti specifiski iedarbojas uz dažādiem psoriāzes patoģenēzes posmiem, nebūdami toksiski tādiem or gāniem kā aknas un nieres. Pašlaik visus bioloģiskos aģentus var iedalīt divās grupās: audzēja nekrozes faktora inhibitori (Tumor Necrosis Factor, TNF - infliksimabs, etanercepts, adalimumabs) un T-šūnu inhibitori (efalizumabs, alefacepts).
Bioloģiskos aģentus izvēlas pacientiem ar vidēji smagu vai smagu psoriāzi, īpaši ar psoriātisko artrītu, kad citas pirmās līnijas terapijas nav bijušas efektīvas. Šie preparāti pašlaik tiek uzskatīti par otrās izvēles līdzekļiem, jo spēj izraisīt imūnsupresiju, kas paaugstina sekundāro infekciju un audzēju attīstības risku. [18] Eiropas Savienībā līdz šim psoriāzes ārstēšanā tika izmantoti divi bioloģiskie aģenti - efalizumabs (Raptiva) un etanercepts (Enbrel).
Efalizumabs ir monoklonālās IgG1 antivielas, kas piesaistās CD11a šūnām, tādējādi inhibējot leikocītu adhēziju pie citām šūnām. Tā kā tiek bloķēti LFA-1 receptori, pazeminās T šūnu piesaiste endoteliocītiem.
Efalizumabu nozīmē subkutānu injekciju veidā vienu reizi nedēļā, sākot ar 0,7 mg/kg, tad turpinot ar 1 mg/kg. Lietojot šo aģentu, var rasties saaukstēšanās simptomiem līdzīgas parādības (galvassāpes, slikta dūša, drebuļi, drudzis, mialģija, vemšana). Var rasties pārmaiņas asinsainā (trombocitopēnija, hemolītiskā anēmija). [19] Ir ziņots, ka 13,8% ar efalizumabu ārstēto pacientu aptuveni 12. nedēļā pēc terapijas pārtraukšanas novēro izteiktu psoriāzes uzliesmojumu. [20] Efalizumabs (Raptiva) Eiropas Savienībā centralizēti tika reģistrēts 2004. gadā un bija indicēts vidēji smagas un smagas psoriāzes ārstēšanai pacientiem, kam cita sistēmiski lietojamā psoriāzes terapija bija kontrindicēta, neefektīva vai pacients to nepanesa. 2009. gada 19. februārī Eiropas Zāļu aģentūra sniedza atzinumu, kur ieteica apturēt Raptiva reģistrācijas apliecības darbību visā Eiropas Savienībā, tostarp arī Latvijā. Atzinumā norādīts, ka ieguvums, ko Raptiva lietošana sniedz psoriāzes ārstēšanā, ir neliels un neatsver būtisku blakņu risku, arī progresējošas multifokālas leikoencefalopātijas rašanās risku. Balstoties uz šo atzinumu, 2009. gada 9. jūnijā Eiropas Komisija izdeva lēmumu par Raptiva reģistrācijas apliecības darbības atsaukšanu.
Pašlaik Eiropas Savienībā un arī Latvijā no bioloģiskajiem aģentiem ir pieejams etanercepts (Enbrel). Tas ir proteīns, kas piesaistās pie TNF, neļaujot tam saskarties ar TNF receptoriem, kas izvietoti uz šūnu virsmām, tādējādi neļaujot aktivizēt iekaisuma procesu kaskādi. Enbrel izmanto tādu iekaisīgu slimību ārstēšanā kā vidēji smaga, smaga psoriāze, psoriātiskais artrīts, reimatoīdais artrīts, juvenīlais idiopātiskais artrīts, ankilozējošais spondilīts. Etanerceptu var lietot kombinācijā ar metotreksātu vai arī monoterapijas veidā. Enbrel ievada subkutānu injekciju veidā (pieejami pildspalvinjektori) pieaugušajiem 50 mg divas reizes nedēļā trīs mēnešus, pēc tam 50 mg vienu reizi nedēļā.
Biežāk novērotās Enbrel blaknes ir reakcija injekcijas vietā (apsārtums, nieze, asiņošana, sāpes) un infekcijas pievienošanās (plaušu, urīnpūšļa, ādas infekcijas). [21] Eiropas Zāļu aģentūra secinājusi, ka pacienta ieguvums, lietojot Enbrel psoriātiskā artrīta un parastās psoriāzes ārstēšanā, pārsniedz šo zāļu radīto risku. Enbrel ir reģistrēts Eiropas Savienībā kopš 2000. gada. Reģistrācijas apliecību atjaunoja 2005. gadā. Latvijā šis preparāts iekļauts kompensējamo zāļu sarakstā. To var indicēt bērniem no astoņu gadu vecuma ar ilgstošu, smagi noritošu psoriātisko artropātiju, kas nereaģē uz citām ārstēšanas metodēm vai tās ir kontrindicētas.
Pašlaik tiek pētīti jauni medikamenti, piemēram, angioģenēzes inhibitori, fumārskābes preparāti, orālais pimekrolims, sintētisko retinoīdu jaunākā paaudze, antidiabētiskie līdzekļi, citokīnu inhibitori. Psoriāzei selektīvu medikamentu izpēte saistībā ar šīs slimības patoģenēzes novitātēm psoriāzes pacientiem sola, ka nākotnē šo mokošo slimību tomēr varēs ne tikai veiksmīgi kontrolēt, bet arī pilnībā izārstēt.