Lielākajai daļai cilvēku ādā pēc sauļošanās sezonas paliek saules “pēdas”, kas ziemas periodā var izzust, bet citiem palikt ilgstoši un pat progresēt ar katru nākamo insolācijas periodu. Arī saules iedarbība ir tūlītēja (saules apdegums), vēlīna (saules iedegums) un kumulatīva (saules radītas hroniskas izmaiņas ādā). Kumulatīvā darbība izskaidrojama ar UV starojuma “krāšanos” dzīves laikā ar katru UV starojuma ekspozīcijas epizodi. Līdz ar sezonas slēgšanos mēs apkopojam sauļošanās izraisītās ādas izmaiņas un tās reģenerācijas iespējas, iedziļinoties ādas aizsargspējās un atjaunošanās pamatprincipos.
UV starojuma ietekme uz ādu
UV starojumu iedala trīs kategorijās: UVA (315-400 nm), UVB (280-314 nm), UVC (100-280 nm). UV starojuma izraisīts primārs bojājums sākas epidermā, bojājot šūnu DNS. UVA un UVB izraisa DNS mutācijas un eventuāli arī ādas vēzi, bet darbības mehānismi ādā ir dažādi. UV starojumu, kura viļņu garums ir 245-290 nm, DNS absorbē vislabāk, tādējādi UVB starojums ir mutagēns. [1] UVB starojums izraisa DNS mutācijas tiešā veidā, veidojot ciklobutāna pirimidīna dimērus, šo savienojumu agregācija palēnina šūnu replikāciju un transkripciju, izraisot C > T un CC > TT DNS mutācijas, rezultātā attīstās onkogēna transformācija. UVA starojums darbojas netieši, izraisot šūnās DNS mutācijas ar brīvo radikāļu starpniecību; veidojas oksidatīvie produkti (reaktīvie skābekļa savienojumi ROS - reactive oxygen species), kas ir mutagēni un izraisa karcinoģenēzi.
UVA starojums ādā iekļūst dziļāk, tomēr UVB stari ir bīstamāki, jo tie ādas šūnās veicina karcinogēnos efektus: tieši bojā šūnas DNS molekulas, DNS reparācijas mehānismus, nomāc šūnu mediēto imunitāti. [5] DNS bojājums var izraisīt mutācijas, ģenētisku nestabilitāti un izmainīt šūnas funkcijas, tāpēc pieaug ādas vēža attīstības risks. Jebkura UV spektra daļas viļņi spēj radīt bojājumu ādas matricē, kolagēnajās šķiedrās, veicinot to deģenerāciju un paātrinot ādas novecošanās procesus. [6] UVB un UVA starojuma darbības mehānisma salīdzinājumu ādā skat. 1. tabulā.
![UVB un UVA starojuma darbības mehānisma salīdzinājums ādā [3; 4]](https://cdn.doctus.lv/media/2012/08/2/original/004033271d38.jpg)
![UVB un UVA starojuma darbības mehānisma salīdzinājums ādā [3; 4]](https://cdn.doctus.lv/media/2012/08/2/original/004033271d38.jpg)
1 tabula
UVB un UVA starojuma darbības mehānisma salīdzinājums ādā [3; 4]
UV starojuma izraisītas akūtās un vēlīnās klīniskās izpausmes ādā
Līdz 60% cilvēku pēc sauļošanās novēro vismaz vienu saules apdeguma pazīmi: ādas apsārtums, nieze un/vai dedzinoša sajūta, hiperpigmentācijas veidošanās, sausums, polimorfie gaismas izsitumi, gaismas inducēta medikamentu reakcija, ādas trauslums un pūšļi. Vēlāk var attīstīties solārija/saules "traipi", jauni atipiski melanocītu veidojumi, porfīrija, sistēmiskā sarkanā vilk-ēde, subakūtas ādas sarkanās vilkēdes gaitas pasliktināšanās, pieaug ādas ne-melanocītu ādas vēža un melanomas attīstības risks. [7] Ādas izmaiņas mikrolīmenī saistītas ar Langerhansa šūnu, CD3+ un CD4+ šūnu skaita samazināšanos, citokīnu indukciju TNF-α, IL-10, CD3+ un CD4+. [8; 9] UV starojuma iedarbības ādā un iespējamo bojājumu apkopojumu skat. attēlā.
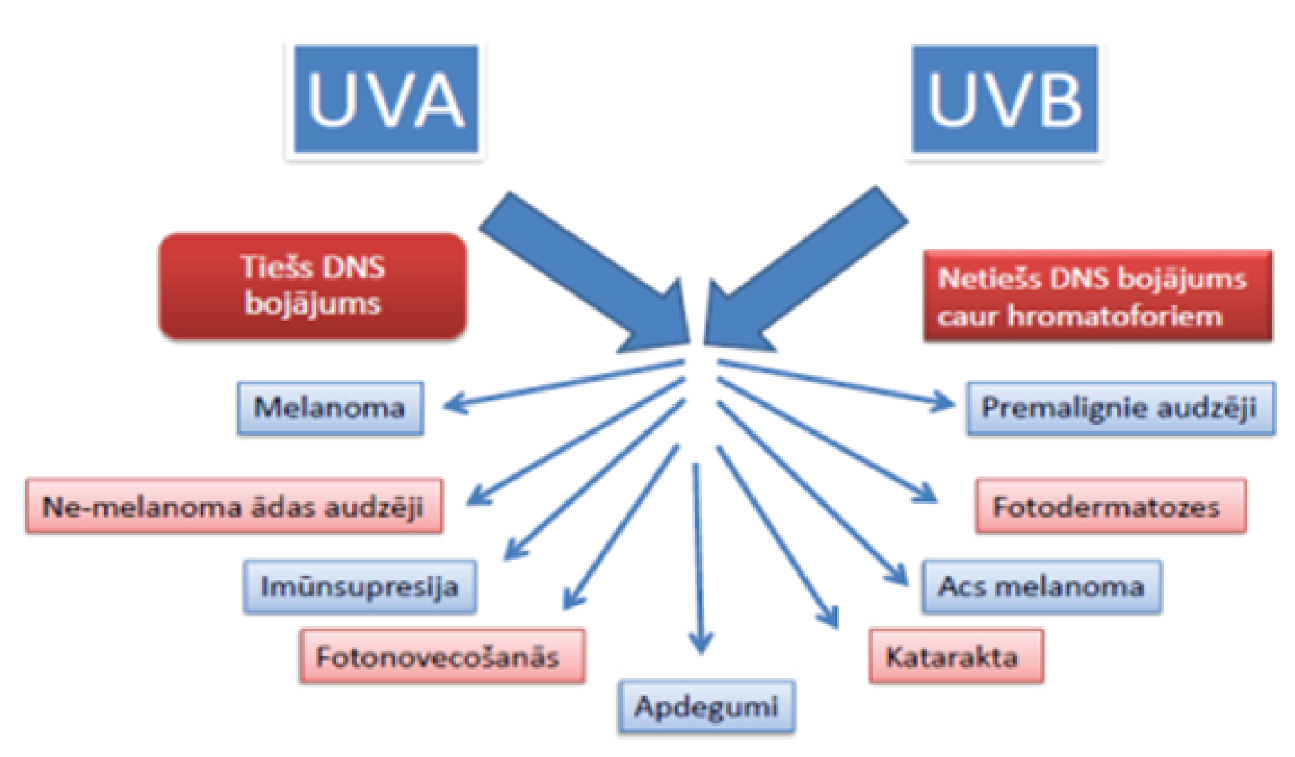

1 attēls
UV starojuma iedarbība ādā
Ādas aizsargspējas
Aizsargmehānismi katram cilvēkam ir individuāli un atkarīgi no cilvēka fototipa (pēc Fitzpatrick klasifikācijas) [10], vecuma, veselības stāvokļa, sezonas, apstarojamās ķermeņa daļas un citiem faktoriem. Aizsargmehānismi darbojas līdz noteiktai pakāpei - cilvēka foto aizsardzības resursi ir ierobežoti. Lai ierobežotu foto bojājumu, ādai ir adaptācijas, aizsargsistēmas un reparācijas mehānismu spektrs. Endogēnie ādas aizsargmehānismi: epidermas biezuma pieaugums, nevienmērīga pigmenta veidošanās, DNS atjaunošanās mehānismi, apoptoze, audu metalproteināžu inhibitori, antioksidanti, urokaīnskābes veidošanās.
Ādas iedegums
Organisma aizsardzība pret UV starojumu izpaužas ar brūna pigmenta - melanīna produkciju, kura sintēze pieaug atbilstīgi UV iedarbības ilgumam un ādas tipam. Pigments tiek transportēts no melanocītiem uz keratinocītiem, rodas iedegums. [11] Melanīna funkcija ir absorbēt UV starojumu un izkliedēt enerģiju kā nekaitīgu siltumu, tādā veidā pasargājot epidermas cilmšūnas un keratinocītus no UV bojājuma. Aizsargpigments šūnās izvietojas virs šūnu kodoliem, cenšoties pasargāt tos no UV staru iedarbības. Uzskats, ka pirms saules insolācijas ieteicams mākslīgais iedegums, kas pasargās no iespējamiem dabīgās saules izraisītiem apdegumiem, ir mīts. Tā kā solārijos pārsvarā ir UVA starojums, solārija apmeklētājam sākotnēji ādā notiek tā melanīna oksidēšanās, kas jau ir epidermas virsējā slāņa keratinocītos, to sauc par tūlītēju iedegumu. Tas ir maznoturīgs un ātri izbalē. Noturīgāks iedegums iegūstams ar starojuma uzkrāšanos - to nosaka iedeguma veidošanās spējas un UVB staru daudzums lampu starojumā. Tūlītēja tipa iedegumam nav fotoaizsargājoša efekta pret UV izraisīto ādas sārtumu vai apdegumu. UVA staru radītais permanentais iedegums nodrošina ļoti minimālu fotoaizsardzību.
Ādas antioksidanti
Ādā ir enzīmiskie un ne-enzīmiskie antioksidanti (skat. 2. tabulu). Endogēnā antioksidatīvā sistēma darbojas, pasargājot no brīvajiem radikāļiem (ROS), kas dabīgi veidojas šūnas cikla laikā. Iztrūkstot antioksidantiem, šūna nonāk oksidatīvā stresa stāvoklī. Šo aizsardzības mehānismu spēja izsīkst līdz ar organisma nodzīvotajiem gadiem. [13]
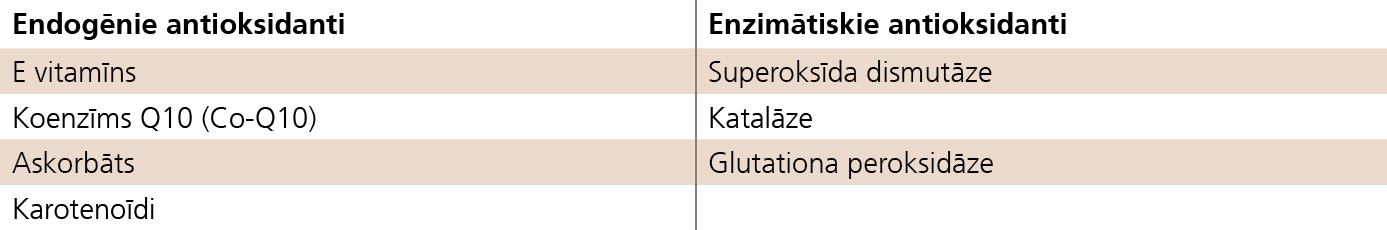

2 tabula
Enzīmiskie un ne-enzīmiskie antioksidanti
DNS bojājumu reparācija un p53
Ar UV staru ierosinātu DNS molekulas bojājumu tiek aktivēta p53 gēna transkripcija. p53 ir proteīns, kas regulē šūnas dzīves ciklu, aktivācijas rezultātā šūnas dzīves cikls apstājas G1 šūnas cikla fāzē un ieslēdzas apoptozes mehānismi. UV izraisītās mutācijas, kā ciklobutāna pirimidīna dimēru un (6-4) fotoproduktu veidošanās, tiek reparētas ar iekšējiem mehānismiem - nukleotīdu ekscīzijas un reparācijas sistēmu. [14; 15]
DNS bojājums un apoptoze
Keratinocītu apoptozes procesā lieto terminu "saules apdeguma" šūnas, ko var atrast jau 30 minūtes pēc pakļaušanas UV staru iedarbībai, apoptozes mehānismu nomākuma dēļ līdz ar gadiem arī saules apdegumu šūnu veidošanās spējas mazinās. Ja tiek bloķēts apoptozes mehānisms, paveras karcinoģenēzes attīstības ceļš, kas paaugstina ādas malignitātes attīstības riska līmeni. [16]
Ādas reģenerācijas spējas
Progresējošu fizioloģisku izmaiņu dēļ organisms noveco. Ar laiku iznīkst bioloģiskās funkcijas un organisma spēja adaptēties metabolajam stresam. Ādas reģenerācijas iespējas neatkarīgi no ādas bojājuma saistītas ar epidermas procesiem (epidermas cilmšūnas, epidermas šūnu proliferācija) un dermāliem procesiem - fibroblastiem, to ekstracelullārajiem proteīniem (elastīns, glikozaminoglikāni, fibronektīns, laminīns, kolagēns) un citām bioloģiski aktīvām vielām (prostaglandīni, leikotriēni, citokīni).Epidermas cilmšūnas ir interfolikulāro rajonu bazālajā slānī, tauku dziedzeru sieniņā, mata folikula izvelvējumā. Cilmšūnas ir ārkārtīgi svarīgas gan epidermas atjaunošanās procesā, gan epidermālas izcelsmes audzēju attīstībā.Ādas reģenerācijas spējas nav atkarīgas no ādas bojājuma. Ādas dzīšanas (reģenerācijas) procesā izšķir trīs savstarpēji dublējošās fāzes:
- iekaisuma;
- proliferatīvo;
- rekonstruktīvo (remodelēšanās).
Epidermas procesi: epidermas cilmšūnas un epidermas šūnu proliferācija. Dermālie procesi - galvenais aģents ir dermas matrices atjaunošanās ar fibroblastu starpniecību un kolagēna sintēzi (saistaudu proteīns elastīns un glikozaminoglikāni).Ekstracellulārā matrice ir ādas skelets, kur galvenās reģenerācijas, izturības un ādas karkasa funkcijas izpilda fibroblasts. Fibro-blasti ir mezodermas izcelsmes šūnas, un to galvenā funkcija ir ekstracellulārās matrices sintēze, kas sastāv no glikozaminoglikāniem, elastīna, fibronektīna, laminīna, kolagēna (vissvarīgākā sastāvdaļa ir kolagēns). Fibroblastiem ir arī sekretorā funkcija, producējot citokīnus (IL-1, IL-6, IL-10, TNF-a), augšanas faktorus, hemokīnus un iekaisuma mediatorus. Gadījumā, ja ādai trūkst aizsardzības pret UV stariem, var rasties dažādi ādas bojājumi no labdabīgiem prekursoriem līdz ļaundabīgiem jaunveidojumiem ādā. [17]
Ādas novecošanās un fotonovecošanās
Hronoloģiska novecošanās ir progresējošas fizioloģiskas izmaiņas organismā. Ar gadiem bioloģiskās funkcijas, adaptācijas mehānismi, endogēnie antioksidanti un organisma spēja pielāgoties metabolajam stresam izsīkst. Novecošanās ir ģenētiski ieprogrammēts process. [18] Ir divas ādas novecošanās pamata teorijas.
- Ģenētiski nosacīts novecošanās process, saistīts ar telomēru garumu; terminālās daļas no hromosomām saīsinās ar katru šūnas ciklu. Kad telomēri sasniedz kritisko īsumu, šūnu cikls apstājas/ieslēdzas apoptozes mehānisms.
- Apkārtējās vides kumulatīvas ietekmes izraisīta ādas novecošanās. Brīvie radikāļi normāla metabolisma dēļ producējas no skābekļa, veicinot novecošanās procesus. UV starojums bojā telomērus un paātrina šūnas novecošanos. Novecošanās lielā mērā atkarīga no apkārtējās vides faktoru kumulatīvās darbības, to paātrinātu ādas novecošanos UV starojuma dēļ sauc par fotonovecošanos, nosaukums literatūrā angļu valodā - sun damaged skin. [19; 20]
Ādas novecošanās klīniskās izpausmes
Dispigmentācija, ādas ļenganums, dzeltenīga nokrāsa, krunkas, telangiektāzijas, ādas labdabīgie veidojumi - seborejas keratoze, ādas ļaundabīgie veidojumi - bazalioma, aktīniskā elastoze un Favre-Racouchot sindroms. [21; 22]
UV starojuma radītu ādas bojājumu profilakse un ārstēšana
Profilakse
UV starojuma radītu ādas bojājumu profilakse:
- neapmeklēt solārijus/atturēties no sauļošanās dabīgajā saulē;
- izvairīties no tiešās insolācijas (īpaši no plkst.11:00 līdz 15:00);
- izmantot saules aizsarglīdzekļus ar SPF 15 pieaugušajiem, SPF 30 un vairāk bērniem. Līdzekļi jāuzklāj uz ādas pusstundu pirms iziešanas saulē, jāatkārto ik pēc 2-3 stundām;
- piemērots apģērbs aizsardzībai no intensīvā saules starojuma (kokvilnas krekliņš ar īsām piedurknēm, saulesbrilles, cepure);
- daži medikamenti un dekoratīvās kosmētikas līdzekļi pastiprina ādas jutību pret gaismu. Kosmētiskie līdzekļi var izraisīt negaidītu reakciju vai ilgstošu pigmentāciju. Tādu vielu lietošana pirms sauļošanās stingri jāierobežo.
Ārstēšana
Mūsdienu dermatoloģija, kosmetoloģija un plastiskā ķirurģija piedāvā plaša spektra risinājumus ādas reģenerācijas procesu veicināšanai. Kopumā procedūras iedalāmas ķirurģiskās un ne-ķirurģiskās. Ne-ķirurģisko metožu kopsavilkumu skat. 3. tabulā.


3 tabula
Fotonovecošanās ārstēšana
Īpaša uzmanība pēdējos gados tiek pievērsta preparātiem, kas rada optimālu vidi šūnu diferenciācijai epidermā un dermā, šūnu reģenerācijai (epidermas keratinocītu proliferācijai un dermas fibroblastiem). Paliek strīdīgs jautājums par cilmšūnu kultūru un to produktu lietošanu. Starp ķirurģiskām metodēm minamas blefaroplastija, rinoplastija, otoplastija, face-lifting operācijas, augmentācijas, liposakcijas, ablatīvie lāzeri, neablatīvie lielas jaudas lāzeri, augstas koncentrācijas skābju pīlingi un arī mamoplastija, radiofrekvences un ultraskaņas procedūras.