Šis nebija tipisks gadījums, jo ultrasonogrāfiski netika konstatētas raksturīgas maiņas, vienīgi difūzās struktūras izmaiņas, kas faktiski norādīja, ka ir tireoidīts, bet tas ir ļoti plašs jēdziens. Netipiski, ka arī pēc amiodarona pārtraukšanas vairākus mēnešus tas saglabājas un liek domāt, ka ar antiaritmisku preparātu pacients varbūt ārstēts jau uz tireotoksikozes fona, kas, savukārt, izraisa biežas mirdzaritmijas lēkmes. Šā klīniskā gadījuma demonstrācijas mērķis ir parādīt amiodarona indicētu tireotoksikozes gadījumu ar smagu gaitu un ilgstošu komplicētu ārstēšanu, kā arī atgādināt, ka, sākot terapiju ar amiodaronu, jākontrolē vairogdziedzera funkcija un struktūra.
Klīniskā gadījuma demonstrācija
(Dr. Lauma Zariņa)
Sūdzības un slimības anamnēze
Pacients, vīrietis, 63 gadus vecs. 2011. gada 31. martā akūtā kārtā stacionēts 9. nodaļā. Pārvests no reģionālās slimnīcas. Sūdzības, iestājoties P. Stradiņa Klīniskajā universitātes slimnīcā, par izteiktu nespēku, svīšanu, elpas trūkumu, sirdsklauvēm, apetītes trūkumu, krišanos svarā.
Slimības anamnēze
Pacients slikti jūtas kopš 2010. gada decembra beigām, kad parādījās nespēks, sauss lēkmjveida klepus, paaugstināta temperatūra (37,5-39º). 2011. gada 4. janvārī stacionēts reģionālajā slimnīcā.
Reģionālajā stacionārā veikto analīžu rezultāti:
- CRO 136 mg/l ;
- FT4 30,2 pmol/l (12-22) ;
- FT3 9,51 pmol/l (3,1-6,8) ;
- datortomogrāfija plaušām, videnei- infiltrāciju neredz, pneimofibroze;
- elektrokardiogramma- sinusa ritms 66x/min. Hisa kūlīša kreisās kājiņas pilna blokāde;
- ehokardiogrāfija- izteikta kreisā ātrija dilatācija, mērena kreisā kambara hipertrofija, kambaru starpsienas hipokinēzija ar saglabātu globālo sistolisko funkciju. Izsviedes frakcija 55%.
Uz antibakteriālās terapijas fona CRO mazinās (6,1 mg/l). 2011. gada 11. janvārī pacients izrakstīts ar diagnozi "hroniska bronhīta uzliesmojums". Terapijā saņēma cefalosporīnu grupas antibiotikas.
Turpinot slimības anamnēzi, būtiski ir norādīt, ar kādām slimībām pacients slimo.
- Koronāra sirds slimība: vecs miokarda infarkts; 2002.gadā veikta PTCA LAD ar stentu.
- Mirdzaritmijas paroksizmālā forma- lēkmes kopš 2008.gada, kad sākta terapija ar amiodaronu 200mg 1x dienā. Lēkmes sākotnēji vienreiz gadā, vēlāk līdz trim reizēm gadā. Tās tika kupētas ar amiodaronu i/v. Medikamentu pārtraucis lietot 2011.gada februārī.
- HSM IIFK pēc NYHA.
- Primāra arteriāla hipertensija.
- 2.tipa cukura diabēts, neinsulinējams.
Pacients nesmēķē, alerģijas neatzīmē.
2011. gada februārī ambulatori konsultējis endokrinologs. Tiek nozīmēta antitireoīdā terapija ar tirozolu pa 10 mg 3 reizes dienā, taču pacients joprojām jūtas slikti un 2011. gada 10. martā atkārtoti stacionēts reģionālajā slimnīcā ar izteiktu elpas trūkumu, nespēku, aritmisku sirdsdarbību, izteikti sliktu pašsajūtu.
Analīzēs, atkārtoti iestājoties stacionārā, konstatē paaugstinātu CRO un izteiktu tireotoksikozes ainu:
- CRO 113,33 mg/l;
- TSH
- FT4 >100pmol/l (12-22).
Veiktie izmeklējumi:
- datortomogrāfija plaušām- kreisajā plaušā S8 infiltrācijas zona. Slēdziens: kreisās puses pneimonija;
- elektrokardiogramma- ātriju fibrilācija 117x minūtē;
- ehokardiogrāfija- mērena kreisā sirds dobuma dilatācija, labais sirds dobums normāla lieluma. Viegla kreisā kambara hipertrofija, viegla kreisā kambara sistoliska disfunkcija. Izsviedes frakcija- 47%.
Dinamikā uz antibakteriālās terapijas fona iekaisuma marķieri mazinājās, taču saglabājās augsts vairogdziedzera hormonu līmenis, strauji pasliktinājās pacienta pašsajūta.
Tālākai ārstēšanai 2011. gada 31. martā pacients tiek pārvests uz P. Stradiņa Klīniskās universitātes slimnīcas Endokrinoloģijas nodaļu.
Objektīvie izmeklējumi, iestājoties PKUS Endokrinoloģijas nodaļā
Vispārējais stāvoklis smags, bet stabils. Apziņa skaidra. Izteikts nespēks. Āda bāla, silta, mikla. Auskultatīvi virs plaušām vezikulāra elpošana. Kreisā pusē novājināta, atsevišķi sausi trokšņi. Elpo 20 reizes minūtē. Sirdsdarbība aritmiska, 170 x/min., TA 140/80 mm/Hg. Vēders mīksts, palpatori nesāpīgs. Perifēru tūsku nav.
Analīžu rezultāti iestājoties.
- Asinsaina:
- WBC 5,7x109/l,
- RBC 4,15x1012/l,
- HGB 116 g/l,
- HTC 36,1% ,
- PLT 250x109/l.
- Bioķīmija:
- AlAT 41 U/l ,
- AsAT 52 U/l ,
- kreatinīns - 69 mkmol/l,
- Na - 148 mmol/l ,
- K - 4,4 mmol/l,
- Ca -2,35 mmol/l,
- glikoze 8,4 mmol/l ,
- CRO 8,2 mg/l .
- Vairogdziedzera hormoni:
- TSH 0,009 µSV/ml (norma 0,55-4,78) ,
- FT4 > 12 ng/ml (norma 0,89-1,76) ,
- FT3 13 pg/ml (norma 2,3-4,2) .
Nodaļā sākta terapija ar glikokortikoī-diem (solumedrols 250 mg i/ v), tia ma zo lu (ti rozols 20 mg x 3), beta blokatoriem (propranolols 40 mg x 3); kardiovaskulārā profila terapija: perindoprils 5 mg p/o, digoksīns 0,025 mg i/v, torasemīds 20 mg p/o, aspirīns 100 mg p/o, kā arī intensificētā insulīna terapija.
Otrajā stacionēšanas dienā pacientam pastiprinās elpas trūkums. Objektīvi: āda silta, mikla, cianotiskas lūpas, izteikta tahipnoja, elpo 28 x/min., TA 95/65 mmHg, tahiarimija ~140 x/min. Ņemot vērā pacienta smago stāvokli ar prevalējošu sirds mazspēju uz tireotoksikozes fona, aizdomām par plaušu artēriju trombemboliju, tālākai ārstēšanai pacients tiek pārvests uz Kardioloģijas centra 32. nodaļas intensīvās terapijas palātu.
Tiek veikta datortomogrāfija plaušām. Secinājums: plaušu artēriju trombembolija kreisās plaušas lejasdaivas 8. un 9. segmentā ar infarktpneimoniju 8. segmentā. Kardiomegālija.
Sākta antikoagulantu terapija. Intensīvās terapijas palātā pacients pavada 2 dienas, tālākai ārstēšanai tiek pārvests uz 32. nodaļu, kur ārstējas no 4. līdz 10. stacionēšanas dienai. Stāvoklim stabilizējoties, tiek pārvests uz 9. nodaļu.
Izmeklējumi
Ehokardiogrāfija: mērena sirds dobumu dilatācija, kreisā kambara hipertrofija, globāla sistoliska disfunkcija, pulmonāla hipertensija. MR I-II, TR I-II. Izsviedes frakcija 36%.
Kāju dziļo vēnu US doplerogrāfija: v. femoralis dx tromboze.
Ultrasonoskopija vairogdziedzerim: abas daivas nehomogēnas, ar mazliet pazeminātu ehogenitāti, ar traipveida kopā saplūstošiem apvidiem. Vaskularizācija neviendabīga, taču nav pastiprināta. Pārliecinoši masīvus mezglus vairogdziedzera audos neredz. Izmaiņas kā hroniska autoimūna tireoidīta gadījumā.
Analīzes:
- anti TPO Av 5SV/ml (≤34);
- anti Tg Av 10,2SV/ml (≤115);
- Av pret TSHR 1,2 (
- BNP 2844,1 pg/ml (>0-100).
Ārstēšana
- Antitireoīdā terapija:
- glikokortikoīdi: solumedrols 250mg i/v ® medrols 32mg p/o® 24mg;
- tiamazols: tirozols 20mg x3® 10mg x4;
- beta blokatori: propranolols 40mg x3 p/o.
- Kardiovaskulārā profila terapija:
- perindoprils/indapamīds2,5mg/0,625mg p/o;
- digoksīns 0,25mg/0,125mg pārdienās p/o;
- torasemīds 10mg p/o;
- nitrāti (Imdur) 30mg p/o;
- orfarīns 3mg p/o;
- aspirīns 100mg p/o;Preductal MR 35 mg x 2 p/o.
- Intensificētā insulīna terapija (Apidra, Lantus).
- Rehabilitācija.
Uz terapijas fona pacienta pašsajūta uzlabojas, pacients apmierinošā stāvoklī izrakstīts tālākai ambulatorai terapijai.
Klīniskā diagnoze
Smaga amiodarona inducēta tireotoksikoze.
Tireotoksiska sirds.
Plaušu artēriju trombembolija (2011. gada 1. aprīlis).
HSM III FK pēc NYHA.
Jauktas ģenēzes kardiomiopātija.
Koronāra sirds slimība: vecs MI. PTCA LAD ar stentu 2002. gadā.
Mirdzaritmijas pastāvīga forma.
Primāra arteriāla hipertensija.
Cukura diabēts, 2. tips, insulinējams.
Rekomendācijas
TSH, FT3, FT4 kontrole pēc 2 nedēļām, stingra endokrinologa uzraudzība. Terapijā turpināt:
- tirozolu 10mg x2;
- medrolu 16mg 1nedēļu® 8mg;
- beta blokatorus: Betaloc ZOK 100mg x1;
- perindoprilu/indapamīdu 2,5 mg/ 0,625 mg p/o;
- digoksīnu 0,125mg 5dienas nedēļā;
- torasemīdu 10mg 3-4x nedēļā;
- nitrātus: Imdur 30mg;
- Preductal MR 35mg x2;
- orfarīnu 3mg, INR kontrole;
- intensificēto insulīna terapiju (Apidra 6-8 DV, Lantus 8 DV 22:00).
Ambulatorā novērošana
Pacients kopš izrakstīšanās ir stingrā endokrinologa uzraudzībā. 2011. gada novembrī veiktajās analīzēs konstatē eutireozi. Analīzes: TSH 3,35 µSV/ml (0,27-4,2), FT3 4,36 pmol/l (3,1-6,8), FT4 16,1 pmol/l (12-22).
Terapijas rekomendācijas: tirozols 10 mg un L-tiroksīns 25 mkg/50 mkg pārdienās.
Diskusija
Prof. V. Pīrāgs: Vai pamanījāt, ka tiešām ļoti ilgs ir joda izdalīšanās periods no organisma, klīnicistu vidē tas bieži vien netiek pietiekami nopietni ņemts vērā. Mēs ļoti agresīvi šobrīd ārstējam kardiovaskulāros slimniekus, nozīmējot amiodaronu, īpašo tos, kam ir koronāra sirds slimība vai dilatācijas, vai kāda cita iemesla izraisīta aritmija.
Dr. S. Šteina: Vēlējos padalīties pieredzē: ja mums jāizvērtē joda inducētie vairogdziedzera darbības bojājumi, hipotireoze jau patiesībā nebūtu nekas pārāk satraucošs, to var diezgan labi kompensēt un kontrolēt, bet tireotoksikoze vienmēr ir ļoti smagi un grūti ārstējama, kā to parādīja šis klīniskais gadījums. Tāpēc varu tikai ieteikt, ka jāizvērtē, vai vienmēr vajadzīga amiodarona terapija, īpaši pacientiem ar biežiem mirdzaritmijas paroksizmiem. Varbūt labāk un drošāk pacientu atstāt ar stabilu mirdzaritmiju, tādējādi nepakļaujot viņu papildu riskiem.
Prof. V. Pīrāgs: Domāju, piekritīsit, ka amiodarons tomēr ir un paliek efektīvākais antiaritmiskais preparāts, bet jāatceras, ka joprojām ir ne pārāk saprotami gadījumi, piemēram, pacientiem ar autoimūniem procesiem ir lielāks risks, ka medikaments var inducēt hipotireozi. Jādomā, ka vairogdziedzerī, plaušās un citos orgānos ir kādi šūnu mehānismi, ko mēs vēl nezinām, kas nosaka to, ka jods uz dažu cilvēku šūnām iedarbojas toksiskāk nekā pārējiem.
Es negribētu, lai jūs aizietu ar domu, ka jods ir kaitīga un toksiska viela un tāpēc jūs vairs neēdīsit suši. Tas arī ir aplami. Jods ir vērtīgs un vajadzīgs mūsu organisma šūnu signālelements. Tajā pašā laikā pārdozēšana predisponētiem cilvēkiem vienmēr izraisa ļoti dramatiskas blaknes. Jods ir jālieto, bet fizioloģiskās devās. Joda sāli nevar pārdozēt. Var pārdozēt, agresīvi izmeklējot ar kontrastvielām un ar dažiem uzturlīdzekļiem.
Teorētiskā daļa
(Dr. Dace Seisuma)
Iemesli joda inducētai tireotoksikozei:
- pārtika, pārtikas piedevas;
- jodu saturošas kontrastvielas;
- amiodarons.
Cilvēkam dienā ar pārtiku un pārtikas piedevām uzņemamais normālais joda daudzums ir 150 mkg. Tātad, lai uzņemtu dienā nepieciešamo joda daudzumu, jāapēd 75 g laša vai 110 g butes. Ir zināms, ka Eiropā ir samērā nabadzīgi joda endēmiskie rajoni, taču mūsdienās arvien vairāk iespējams baudīt no citām valstīm ievestus produktus, kas bagātīgi satur jodu, piemēram, japāņu virtuve. To redzam arī klī nis ko gadījumu ziņojumos par pacientiem ar diagnosticētu tireotoksikozi, kuri pārmērīgi aizrāvušies ar suši restorāniem un pārtikā lietojuši dažādas jūras zāles, t.sk. brūnaļģes, kas satur 1350 mgk joda gramā.
Jodu saturoša kontrastviela
Viena no jodu saturošām kontrastvielām, ko izmanto arī mūsu slimnīcā, ir Ultravist, kur joda saturs 1 ml kontrastvielas ir 370 mg, savukārt Vizipaque 1 ml satur 320 mg joda. Lai veiktu vienu koronarogrāfijas procedūru, pacientam ievada 100 ml šīs kontrastvielas, tātad vienā reizē viņš saņem 37 g joda. Savukārt datortomogrāfijā kontrastvielas daudzums atkarīgs no pacienta svara un auguma, parasti ievada 80-120 mg kontrastvielas.
Pētījumā par joda indicētu tireotoksikozes risku pēc koronarogrāfijas (Risk of iodine-induced thyrotoxicosis after coronary angiography: an investigation in 788 unselected subjects. G. Hintze et al. European Journal of Endocrinology (1999)) piedalījās 788 īpaši neatlasīti pacienti, 659 vīrieši un 129 sievietes. Pirms procedūras visiem noteica vairogdziedzera hormonu līmeni, kā arī sonoskopiski izvērtēja vairogdziedzeri un noteica antivielas. Tālāk tika izvērtēts vairogdziedzera hormonu līmenis un joda ekskrēcija urīnā pirms koronarogrāfijas, pirmajā, ceturtajā un divpadsmitajā nedēļā pēc koronarogrāfijas. Kā vienīgais izslēgšanas kritērijs šim pētījumam bija jodu saturošu medikamentu lietošana un hipertireoze. Koronarogrāfija tika veikta ar ultravistu 100 ml. Secinājumi: 2 pacientiem no 788 attīstījās hipertireoze pēc 4 nedēļām, 10 pacientiem attīstījās hipotireoze (sešiem pēc 1 nedēļas, četriem pēc 12 nedēļām).
Ir samērā maz pētījumu par joda inducētas hipertireozes risku īpaši neatlasītiem pacientiem no joda deficīta skartiem endēmiskiem apgabaliem.
Amiodarons
Amiodarons pēc struktūras ir ļoti līdzīgs vairogdziedzera hormoniem. Šobrīd tas ir pasaulē plašāk izmantotais antiaritmiskais preparāts priekškambaru un kambaru aritmiju, kambaru fibrilāciju lēkmju kupēšanai un profilaksei. 1967. gadā to sāka lietot kā antianginālu preparātu, taču 1970. gadā sāka ievērot tā antiaritmiskās īpašības, bet tikai 1985. gadā ASV Pārtikas un medikamentu administrācija (FDA) to reģistrēja kā antiaritmisko preparātu.
Amiodarons ir benzofurāna derivāts, kas satur 37% joda. 200 mg tabletē organiskais jods ir 75 mg. Amiodarona metabolizācijas procesā asinīs nokļūst 6 mg brīvā cirkulējošā joda, kas ir 20-40 reižu vairāk par dienā nepieciešamo.
Amiodarons tiek dealkalizēts aknās, veidojas aktīvais metabolīts dezetilamiodarons (DEA). Vidējais pussabrukšanas laiks ir 40 dienas, bet DEA pussabrukšanas laiks ir 57 dienas. Taču, lai amiodarons pilnībā tiktu izvadīts no organisma, jāpaiet 142 dienām.
Tā kā medikamenta aktivitāte audos ir liela, pieminami arī citi amiodarona efekti - respiratorā sistēma tiek skarta līdz pat 17%, to raksturo intersticiāls pneimonīts, plaušu fibroze. Acīs var veidoties specifiska amiodarona retinopātija, kas pēc amiodarona pārtraukšanas likvidējas. Tipiskas izmaiņas ir arī ādā, tāpat ir ziņojumi par alopēciju un fotosensitivitāti. Aknās amiodarona blakne var būt hepatīts un aknu ciroze. Pacientiem, kas ilgstoši lieto amiodaronu, var parādīties sūdzības par gaitas problēmām, tremoru, kognitīvo funkciju traucējumiem. Miokardā tas var izraisīt bradikardiju un QT intervāla pagarināšanos.
Izmaiņas vairogdziedzerī: 70% gadījumu izmaiņas ir eutiroīdas jeb saglabājas normāla vairogdziedzera funkcija, bet 30% gadījumu tā var būt vairogdziedzera hiper- vai hipofunkcija.
Ietekme uz vairogdziedzeri: dažādi efekti - joda inducēts efekts un amiodarona efekts.
Inducēts efekts vairāk saistīts ar izmaiņām paša vairogdziedzera funkcijā - pastiprināta joda uzkrāšanās vairogdziedzerī izsauc hipo- vai hipertireozi. Savukārt amioderona kā medikamenta efekts ir divējāds:
- tas ietekmē dejodināzi, kā rezultātā tiek traucēta tiroksīna konvertācija par trijodtironīnu;
- amiodarona citostātiskā iedarbība uz vairogdziedzera folikulārajām šūnām, kam seko destruktīva tireoidīta attīstība.
Amiodarona inducēta hipotireoze (AIH)
Biežāk AIH sastopama apgabalos, kur joda saturs uzturā ir pietiekams (11-31%). Vīrieši ar amiodarona inducētu hipotireozi slimo biežāk nekā sievietes (1,5:1). AIH biežāk novēro pacientiem ar autoimūnu (Hašimoto) tireoidītu.
Sievietei ar pozitīvām AvTPO un AvTg relatīvais AIH risks ir 13,5%. Ja nav autoimūnas vairogdziedzera slimības, parasti novēro spontānu remisiju.
Amiodarona inducēta tireotoksikoze (AIT)
Biežāk AIT sastopama apgabalos, kur uzturā ir nabadzīgs joda saturs (5-10%), vīrieši slimo trīs reizes biežāk nekā sievietes (3:1).
AIT var parādīties dažas nedēļas vai mēnešus pēc amiodarona terapijas sākšanas. Jāņem vērā, ka ilgā pussabrukšanas laika un izvades dēļ tā var attīstīties pat 6-9 mēnešus pēc amiodarona lietošanas pārtraukšanas.
Amiodarona inducētu tireotoksikozi iedala 2 tipos. Tabulā norādītas būtiskākās tipu atšķirības.
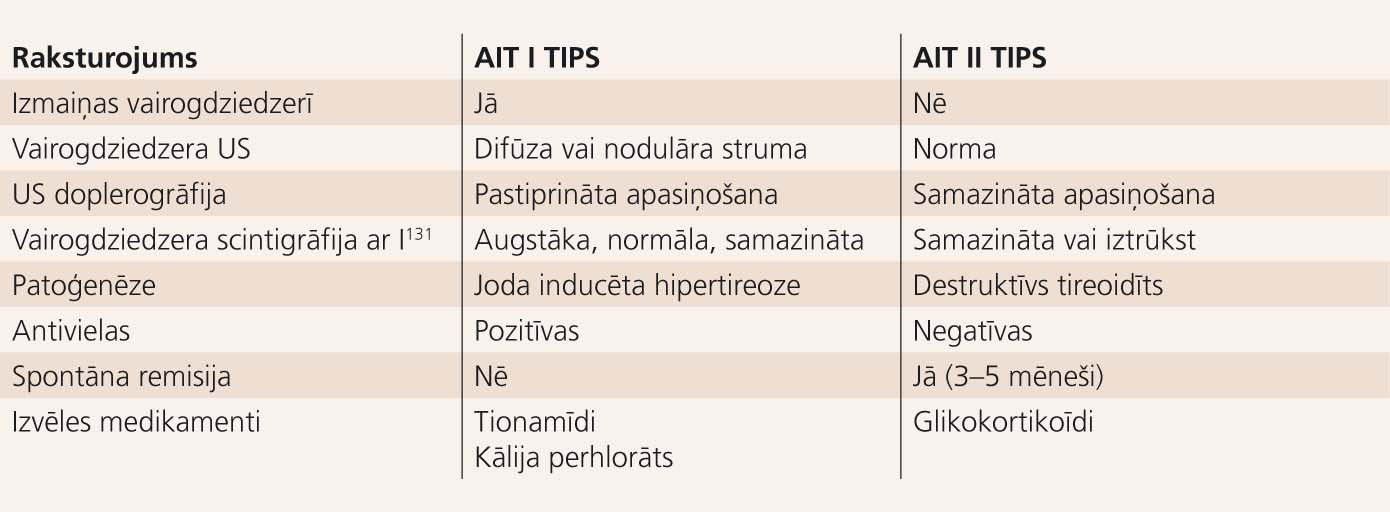

Tabula
Amiodarona inducētas tireotoksikozes būtiskākās abu tipu atšķirības
Rekomendācijas
- Pirms amiodarona terapijas sākšanas vairogdziedzera hormonu noteikšana, kā arī 1.un 3.mēnesī, tad pēc 3-6mēnešiem.
- Amiodarona pārtraukšana jāvērtē kopā ar kardiologu, izvērtējot pacienta kardiālo funkciju.
- Kombinēta ārstēšana ar antitireoīdiem medikamentiem un glikokortikoīdiem.
Ārstēšana
- AIT I tips:
- tionamīdi (metimazols 20-40 mg/d, propiltiouracils 400-600 mg/d),
- kālija perhlorāts 1 g/d;
- AIT IItips- prednizolons 40 mg/d;
- jaukts tips- tionamīdi un glikokortikoīdi.
Ķirurģiska ārstēšana indicēta gadījumos, ja pacients nereaģē uz agresīvu medikamentozo ārstēšanu.