Lai gan visbiežāk psoriāzes izpausmes ir ādā, tā asociēta arī ar sistēmisku iekaisumu un dažādām blakusslimībām (komorbiditātēm), kas saistītas ar autoimūniem procesiem. Viens no šiem procesiem ir psoriātiskais artrīts — iekaisīga, seronegatīva spondiloartropātija, kas kādā dzīves posmā attīstās 13—30 % psoriāzes pacientu.
Psoriāze — pacientu prasības pēc rezultāta pieaug
Dermatologa viedoklis
(Dr. R. Karls)
Psoriāze ir izplatīta hroniska iekaisīga ādas slimība. Tā vienlaikus ir visbiežākā autoimūnā ādas slimība, to raksturo eritematozi, papulozi elementi ar virsmas zvīņām. Tā skar 2—3 % pasaules iedzīvotāju. Latvijā šis procents noteikti ir augstāks.
Patoģenēze
Pēdējos gados izstrādātas daudzas ļoti efektīvas, mērķtiecīgas ārstēšanas metodes, jo papildinājusies izpratne par psoriāzes patoģenēzi. Medikamentu darbības imunoloģiskais modelis ir pamatīgi pārskatīts, iekļaujot jaunākos sasniegumus izpratnē par psoriāzes patoloģisko fizioloģiju. Šā brīža modelī tiek uzskatīts, ka mijiedarbība starp keratinocītiem, neitrofilajiem leikocītiem, tuklajām šūnām, T limfocītu šūnām un dendrītiskajām šūnām rada iekaisuma un proproliferatīvus procesus, ko mediē hemokīni un citokīni.
Dažādi ierosinātāji, ieskaitot nesen identificētus autoantigēnus, Toll līdzīgu receptoru agonistus, stromas limfopoetīnu, var aktivēt patogēno kaskādi, izraisot pastiprinātu izdali un proliferāciju izraisošo mediatoru, piemēram, interleikīna (IL)–17 un –23, audzēja nekrozes faktora sintēzi. TNFα, IL–23, IL–22, interferons (IFN) α un IFNγ sintēzi veic imūnajās šūnas. Starp šiem galvenajiem citokīniem ir īpaši terapeitiskie mērķi, kas pašlaik apstiprināti antipsoriātiskai terapijai.
Terapija
Vieglas gaitas psoriāzes pamatā joprojām paliek lokālā terapija. Tai izmanto gadiem ilgi pārbaudītus medikamentus: dažādas potences kortikosteroīdus, kas iestrādāti dažādās nesējvielās (losjonos, gelos, krēmos, ziedēs), D vitamīna atvasinājumus, piemēram, kalcipotriolu. Atsevišķās lokalizācijās efektivitāti un lietošanas drošumu pierādījuši kalcineirīna inhibitori, kaut arī to lietošana psoriāzes pacientiem joprojām ir ārpus indikācijām.
Vidēji smagas vai smagas psoriāzes ārstēšanā tiek izmantoti sistēmiskie medikamenti, piemēram, metotreksāts, ciklosporīns vai bioloģiskie medikamenti. Jaunākās bioloģiskās zāles ir ļoti efektīvas un labi panesamas, taču ne visi pacienti reaģē uz ārstēšanu ar bioloģiskiem līdzekļiem, tāpēc joprojām tiek meklētas jaunas ārstēšanas iespējas psoriāzei. Arī finansiālā puse bioloģisko medikamentu terapijā joprojām ir aktuāls jautājums, īpaši tik novājinātas veselības aprūpes sistēmas kontekstā, kāda tā ir Latvijā.
Psoriāze bērniem
Psoriāze skar ap 0,5 % bērnu. Psoriāze, kas sākusies bērnu vecumā, ir bieži sastopama ādas slimība, kam pēdējā laikā pievērš arvien lielāku uzmanību, īpaši tās ievērojamā medicīniskā, sociālā, finansiālā un psiholoģiskā sloga un ar to saistīto blakusslimību dēļ. Pašreizējā terapeitiskajā arsenālā ietilpst lokālā terapija, fototerapijas procedūras un sistēmiskā terapija (parastā sistēmiskā terapija un bioterapija), ar ko vairumā gadījumu pietiek, lai kontrolētu šo ādas slimību.
Turpmākā šo bērnu dinamiskā vadībā galvenā uzmanība jāpievērš terapeitiskās iedarbības saglabāšanai un recidīva novēršanai, samazinot ar ārstēšanu saistīto toksicitāti, lai uzlabotu viņu dzīves kvalitāti. Tāpēc izvēlas proaktīvu aprūpi. Šī vadības pieeja attiecas uz četriem galvenajiem priekšrakstiem un terapeitisko izglītību:
- slimības, tās patofizioloģijas un dažādu iespējamo terapeitisko metožu skaidrojums,
- tādu faktoru novēršana, kas izraisa paasinājumus vai pasliktina psoriāzes gaitu (infekcijas, stress, trauma, diēta (galvenokārt aptaukošanās samazināšana)),
- proaktīva pieeja vietējai terapijai (ādas higiēna un mīkstinošu līdzekļu lietošana, kā arī aktīvās terapijas ierobežošana, devu lietošanas intervāli un “nedēļas nogales terapija”, lai samazinātu recidīvu risku),
- proaktīva pieeja sistēmiskai terapijai (uzlabots terapeitiskais drošums, samazinātas kumulatīvās devas, samazinātas devas, dozēšanas intervālu izmantošana un nedēļas nogales terapija).
Ārstējot psoriāzi ar šādām metodēm, palīdzam ierobežot uzliesmojumu ilgumu un smagumu, vienlaikus uzlabojot dzīves kvalitāti. Vienkārši pasākumi faktiski var nodrošināt efektīvu ārstēšanu ilgtermiņā.
Ko sagaida pacients?
Epidemioloģiskie pētījumi, pacientu aptauju rezultāti Eiropā un ASV rāda, ka psoriāzes slimnieku vidējā slimības aktivitāte ir augsta un dzīves kvalitāte ir slikta pat pacientiem, kurus regulāri uzrauga dermatologs. Turklāt pie šiem datiem nākuši klāt pētījumu rezultāti, kas liecina par zemu apmierinātības līmeni ar ārstēšanu un pacientu prasības pēc efektīvākas, drošākas un praktiskākas terapijas.
Psoriāze un blakusslimības
Īpašās pacientu grupas un ārstēšanas situācijas: tuberkulozes sijājošā diagnostika pirms psoriāzes ārstēšanas un tās laikā, psoriāzes ārstēšanas izvēle cilvēkiem, kas plāno ģimenes pieaugumu, un sievietēm grūtniecības un barošanas ar krūti periodā, kā arī pacienti ar locītavu iesaisti un vakcinācijas jautājumi bioloģisko preparātu lietošanas laikā.
Īpaša uzmanība un ieteikumi pacientiem ar šādām blaknēm: hepatīts un citi aknu darbības traucējumi, HIV, ļaundabīgi audzēji, neiroloģiski un psihiski traucējumi, išēmiska sirds slimība un sastrēguma sirds mazspēja, cukura diabēts, nieru darbības traucējumi un zarnu iekaisīgās slimības.
Jaunas terapijas iespējas
Pasaulē plaši tiek lietoti, izstrādāti jauni un efektivitātes un drošuma pētījumos salīdzināti dažādi medikamenti vidējas līdz smagas gaitas psoriāzes ārstēšanai: etanercepts, infliksimabs, adalimumabs, certolizumabs, ustekinumabs, sekukinumabs, iksekizumabs, brodalumabs, guselkumabs, tildrakizumabs, risankizumabs.
Psoriātiskā artrīta pazīmes, diagnostika, ārstēšanas pamatprincipi
Reimatologa viedoklis
(Dr. med., doc. A. Mihailova)
Psoriātiskais artrīts attīstās līdz 30 % psoriāzes slimnieku. To raksturo daudzveidīgas klīniskās pazīmes, tāpēc diagnozes noteikšana un ārstēšana nereti ir novēlota. Šī ir slimība, kas jāuzlūko ar vērīgu prātu, arī terapija jāpiemēro kompleksa, nevis tāda, kas šauri vērsta tikai uz akūtāko simptomu novēršanu.
Sākotnējā pieredze šādu pacientu ārstēšanā uzrādīja labdabīgu slimības gaitu. Tomēr ilgstošāk un dziļāk izzinot psoriātisko artrītu, kļuvis skaidrs, ka slimība bieži izraisa funkciju traucējumus un pasliktina dzīves kvalitāti. Izprotot slimības mehānismu, izstrādātas efektīvas mērķtiecīgas terapijas metodes, kas aptur slimības tālāku attīstību.
Diagnozes noteikšana
Izšķir piecus klīniskos psoriātiskā artrīta (PsA) apakštipus. Oligoartikulārā apakštipa gadījumā slimība skar četras vai mazāk locītavas un parasti asimetriskā sadalījumā. Poliartikulārais apakštips ietekmē piecas vai vairāk locītavas; iesaiste var būt simetriska un atgādināt reimatoīdo artrītu. Distālais apakštips, kas ietekmē roku, pēdu vai abu roku distālās starpfalangu locītavas, parasti attīstās līdztekus citiem apakštipiem. Autonomi tas attīstās vien 5 % pacientu.
Mutilējoša, deformējoša un destruktīva artrīta apakštipam, kas saistīts ar izteiktu kaulu resorbciju vai osteolīzi, raksturīgas izteikti bojātas rokas pirkstu locītavas. Aksiālais vai spondiloartrīta apakštips galvenokārt skar mugurkaulu un sakroileālās locītavas. PsA apakštipi slimības gaitā var mainīties.
Entezīts un daktilīts ir divas raksturīgas PsA pazīmes salīdzinoši lielai pacientu daļai. Entezītu novēro 30—50 % pacientu. Biežāk iekaist plantārā fascija un Ahileja cīpsla, bet sāpes var parādīties arī ap ceļa kauliņu, iliac crest, epikondiļos un m. supraspinatus cīpslas piestiprināšanās vietā.
Daktilītu novēro 40—50 % pacientu, biežāk kājas 3. un 4. pirkstā, lai gan dažkārt skarti arī roku pirksti. Daktilīts var būt akūts (ar pietūkumu, ādas apsārtumu un sāpēm) vai hronisks (pietūkums bez iekaisuma). Daktilīts raksturīgs smagai slimības formai, līdztekus attīstoties arī poliartrītam, kaulu erozijai un veidojoties jaunam kaulam.
PsA diagnozi nosaka pēc klīniskos un radioloģiskos izmeklējumos iegūto pazīmju analīzes un atpazīšanas. Slimībai nav īpašu biomarķieru. Pacienta stāvoklis jāvērtē vismaz piecās izpausmēs: psoriāze, perifēro locītavu slimība, aksiālā slimība, entezīts un daktilīts. Strādājot ar pacientu, jāpatur prātā, ka ik atsevišķā gadījumā domēni var kombinēties dažādi.
Raksturīgi, ka gan pacienta individuālajā, gan ģimenes anamnēzē parasti ir rodamas norādes par problēmām kādā no pieciem domēniem. Iekaisuma artrīts, entezīts, daktilīts un locītavu iesaiste ir būtiski faktori diagnostikas procesā. Tomēr PsA pazīmes var izpausties arī ārpus locītavām, piemēram, ar zarnu iekaisuma slimību un uveītu.
Tā kā PsA var attīstīties gan pirms ādas bojājumu parādīšanās, gan arī tad, ja pacientam nav psoriāzes, izmeklējot būtiski pievērst uzmanību psoriātiskiem ādas bojājumiem — īpaši cirkšņos, nabas apvidū, matu līnijā, ausīs un intergluteālajā krokā. Nagu bojājumi un mugurkaula slimība — arī raksturīgas slimības pazīmes. 2006. gadā publicētie PsA klasifikācijas kritēriji (CASPAR kritēriji) definē slimību un paredzēti izmantošanai, iekļaujot pacientus klīniskajos pētījumos (tabula).
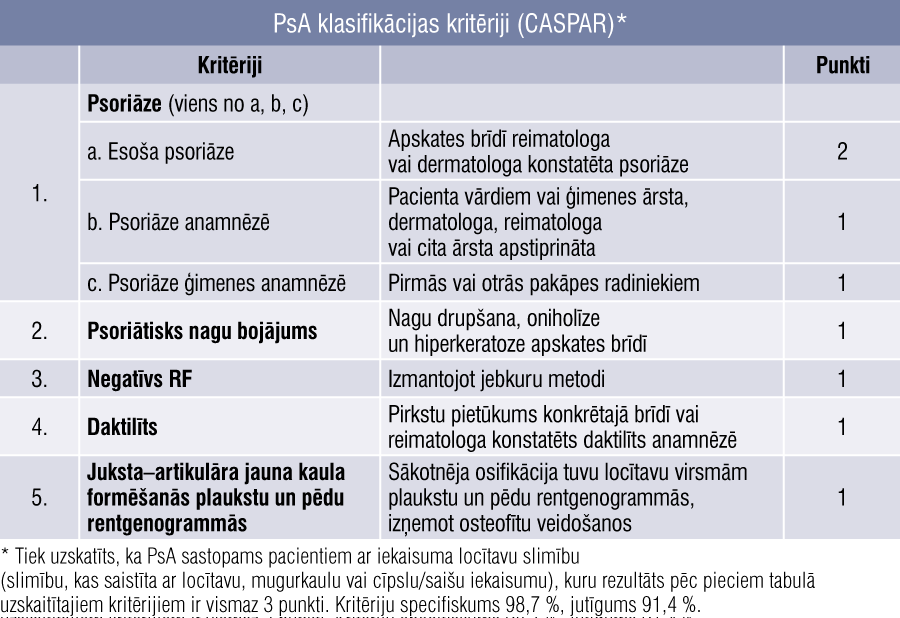

Tabula
PsA klasifikācijas kritēriji (CASPAR)*
Diferenciālā diagnoze
Izsverot diagnozi, PsA jānošķir no citām artrīta formām — reimatoīdā artrīta (RA), osteoartrīta, podagras, pseidopodagras, sistēmiskās sarkanās vilkēdes un citām spondiloartrīta formām.
Reimatoīdo artrītu raksturo proksimāla, simetriska roku un pēdu locītavu iesaiste. Vairāk nekā 50 % PsA pacientu slimība skar distālās locītavas. Raksturīgi, ka bojātas tiek visas, piemēram, viena pirksta locītavas, kamēr citi pirksti paliek neskarti. Šo pazīmi dēvē par “staru” sadalījumu. Pazīme novērojama gan klīniski, gan radioloģiski.
Sākuma stadijā PsA parasti ir oligoartikulārs un mazāk simetrisks nekā RA. Ar laiku PsA var kļūt poliartikulārs un simetrisks. PsA skartās locītavas ir mazāk sāpīgas nekā RA gadījumā. Locītavām var būt purpursarkana krāsa. Mugurkaula locītavu iesaiste slimības gaitā (sakroileālās locītavas vai mugurkaula jostas, krūšu vai kakla daļa) raksturīga vairāk nekā 40 % PsA pacientu, bet ir netipiska pacientiem ar RA.
Psoriātisko monoartrītu, īpaši, ja tas skar kāju pirkstus, vai daktilītu var nepareizi diagnosticēt kā podagru vai pseidopodagru. Urīnskābes līmeņa paaugstinājums raksturīgs visu trīs slimību gadījumā, apgrūtinot diferenciāldiagnozi, īpaši, ja locītavu šķidruma kristālu analīze ir negatīva vai to nevar veikt.
Distālo locītavu bojājumu, kas raksturīgs PsA, novēro arī osteoartrīta gadījumā. PsA gadījumā distālo locītavu pietūkums veidojas mīksto audu iekaisuma dēļ, toties osteoartrīta gadījumā pietūkums rodas no osteofītiem un ir ciets. PsA pacientiem bieži sastopamas distālās starpfalangu locītavas un nagu slimība (pitting vai oniholīze). Tās nav novērojamas osteoartrīta gadījumā.
Ankilozējošais spondilīts sākas dzīves otrās desmitgades beigās vai trešās sākumā. PsA biežāk attīstās ceturtajā dzīves desmitgadē. Tas var noritēt ne tik smagi kā ankilozējošais spondilīts, ar mazākām sāpēm, sakroileālo locītavu ankiloze šiem pacientiem veidojas reti. Asimetriskie sindesmofīti raksturīgāki PsA.
PsA var būt grūti nošķirt no reaktīvā artrīta. Abas slimības bojā locītavas un ādu. Subakūti ādas vilkēdes psoriāzei līdzīgie bojājumi var atgādināt psoriasis vulgaris, bet raksturīgi, ka pacientiem ar ādas vilkēdi nav citu PsA raksturīgo pazīmju.
PsA kā blakusslimība attīstās 30 % psoriāzes pacientu. Dermatologiem un primārās aprūpes ārstiem, kuri uzrauga psoriāzes pacientus, pastāvīgi jāpatur prātā PsA attīstības iespēja un jārūpējas par savlaicīgu slimības diagnosticēšanu, regulāri izvērtējot, vai locītavās nav parādījušas sāpes, izmainījušies pirksti (sausage digits jeb daktilīts) un neveidojas rīta stīvums.
Laboratorijas un radioloģisko izmeklējumu dati
RF un anticiklisko citrulinēto peptīdu antivielas 95 % PsA slimnieku ir negatīvi. Ja kāda testa (vai abu) rezultāts ir pozitīvs, PsA atšķiršanai no RA jāizmanto klīniskās pazīmes un radioloģiskās izmeklēšanas dati. Ap 25 % PsA pacientu ir HLAB27 pozitīvi. CRO un/vai EGĀ līmeņa paaugstināšanās serumā novērota tikai 40 % slimnieku. Izvērtējot radioloģiskos izmeklējumus, būtiski zināt, ka skrimšļa un kaula destrukcija ar patoloģiska jauna kaula veidošanos ir viena no PsA raksturīgākajām pazīmēm. Perifēro locītavu rentgenogrammās bieži redzams kaulu zudums ar ekscentriskām erozijām un locītavas spraugas sašaurinājums, kā arī jaunu kaulu veidošanās, kam raksturīgs periostīts, tūska.
Power Dopler ultrasonogrāfijā var identificēt sinovītu, pastiprinātu vaskularizāciju, tenosinovītu, entezofītus un agrīnu erozīvu slimību.
PsA ir smaga artrīta forma, lielam skaitam pacientu attīstās locītavu bojājumi un deformācijas. Kaulu erozijas pirmajos divos gados novēro 47 % pacientu, lai gan vairāk nekā puse pacientu lieto tradicionālās slimību modificējošās zāles. Turklāt smaga slimība prezentācijas laikā un paaugstināts CRO līmenis ir radiogrāfijas progresēšanas riska faktori.
Ārstēšana
PsA ārstēšana ir sarežģīta daudzveidīgo un bieži citām artrīta formām raksturīgo pazīmju dēļ, kas nereti kļūst par iemeslu novēlotai diagnozes noteikšanai. Tāpēc, pieļaujot PsA varbūtību, būtiski identificēt slimības aktivitātes katrā no raksturīgajām izpausmēm. Ārstēšanas primāro izvēli nereti nosaka simptomātika ar visaugstāko aktivitātes līmeni. Tomēr ir jāārstē viss PsA pacienta slimības izpausmju spektrs.
Galvenie uzdevumi, ārstējot PsA, ir rūpēties par pacienta dzīves kvalitātes un funkciju saglabāšanu ilgtermiņā, kontrolējot simptomus, aizkavējot strukturālos bojājumus, apturot iekaisumu. Sākotnējā ārstēšana — NSPL un glikokortikoīdu injekcijas. Pacientiem, kam šī terapija nav efektīva vai iedarbojas toksiski, kā arī perifēra artrīta gadījumā nepieciešama sistēmiska terapija ar sSMARL jeb sintētiskiem slimību modificējošiem pretreimatisma līdzekļiem (metotreksātu, leflunomīdu, sulfasalazīnu), pēc tam pacientiem, kuri nepietiekami reaģē uz sSMARL, ordinē terapiju ar anti–audzēja nekrozes faktoru (TNF).
Alternatīva anti–TNF inhibitoriem ir citas bioloģiskās zāles (piemēram, interleikīna 12/23 vai 17 inhibitori, Janus kināzes inhibitori) atsevišķiem PsA pacientiem. Terapeitiskā izvēle izriet no slimības klīniskā izklāsta, jo dažas PsA izpausmes, piemēram, entezīts, daktilīts un aksiālā slimība, nereaģē vai slikti reaģē uz sSMARL. Ādas slimības ārstēšanai ieteicama specifiska šim nolūkam paredzēta terapija un medikamenti.
Spontāna remisija PsA pacientiem ir reti. Novērošanas pētījumā, kurā piedalījās ar anti–TNF līdzekļiem ārstēti pacienti, daļēja remisija novērota tikai 23 %. Taču, ja bioloģisko zāļu lietošanu pārtrauc, recidīvu līmenis ir augsts.
Noslēgumā
Līdztekus farmakoterapijai pacients noteikti jāizglīto par to, cik izšķirīga ir iekaisuma kontrole. Dzīvesveida modifikācija — smēķēšanas atmešana, svara samazināšana, locītavu saudzēšana, fiziska aktivitāte, stresa pārvaldība — ir būtiska PsA ārstēšanā.