Lai gan par ģenēriskajām (patentbrīvajām) zālēm diskutēts bieži, pieņēmumu joprojām daudz. “Kad oriģinālajām zālēm beidzies patenta termiņš, formulu pārdod, bet līdz galam visas kārtis neatklāj. “Līdzvērtīgs medikaments” nenozīmē, ka tas ir identisks medikaments,” — tāds diezgan izplatīts viedoklis. Kas ir kas? Noskaidrosim faktus soli pa solim.
Interesanti — no vēstures
Mūsdienu izpratne par ģenērisko zāļu līdzvērtību sāka veidoties XX gadsimta 60. gados. ASV plaša spektra antibiotika hloramfenikols (Chloromycetin) bija viens no pirmajiem antibiotiku blokbasteriem, kuram 1966. gadā beidzās patents. Līdz tam, lai reģistrētu ģenēriskās zāles, ražotājiem bija jāpierāda tikai ķīmiskā ekvivalence. Kad hloramfenikola ģenēriskās zāles nonāca tirgū, vairākos pētījumos noskaidrojās, ka lētākais preparāts nešķīst ūdenī, turklāt cilvēka organismā nav iespējams noteikt aktīvo vielu. Kaut ķīmiskās ekvivalences prasības bija augstas, cilvēka organismā zāles iedarbojās atšķirīgi. ASV Pārtikas un zāļu pārvalde atsauca ģenērisko preparātu un izstrādāja prasības noteikt zāļu absorbciju cilvēka organismā, t.i., pierādīt bioloģisko ekvivalenci. [1]
Ģenērisko zāļu patēriņš aug
ASV Pārtikas un zāļu pārvalde (Food and Drug Administration — FDA) norāda: 2015. gadā beidzās patents vairākiem populāriem medikamentiem, tāpēc tuvākajos gados sagaidāms ģenērisko zāļu īpatsvara pieaugums. IMS Health aprēķini paredz, ka līdz 2017. gadam attīstītajās valstīs lielāko daļu hronisko slimību ārstēs ar ģenēriskajām zālēm, rezultātā izmaksas pieaugs tikai par 5 %. [1]
Kopumā vairāk nekā puse no visām pasaulē lietotajām zālēm ir ģenēriskie preparāti, kas izmaksu ziņā veido tikai 18 % no visa zāļu tirgus. [2] Piemēram, no visiem ASV izsniegtajiem preparātiem 84 % ir ģenēriskie medikamenti, taču naudas izteiksmē — 28 % (ģenērisko zāļu tirgus daļa dažādās valstīs — 1. attēlā). Kā uz citu valstu fona izskatās Latvija? Zāļu valsts aģentūras dati rāda, ka 2015. gadā 75 % no visiem izsniegtajiem preparātiem bija ģenēriskie medikamenti, tie veidoja 45 % no tirgus vērtības (2. attēlā — zāļu patēriņš absolūtos ciparos (dati par tikai nacionālajās procedūrās reģistrētajām zālēm)).
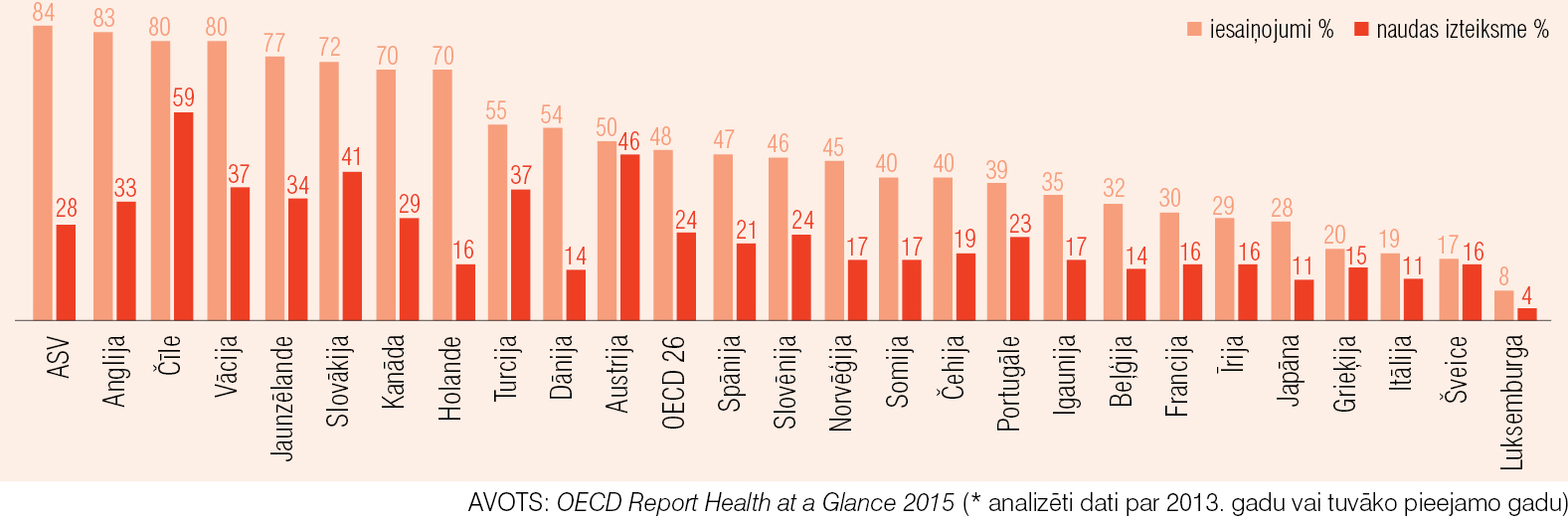

1. attēls
Ģenērisko zāļu tirgus daļa OECD valstīs (naudas izteiksmē un iesaiņojumos)*


2. attēls
Zāļu patēriņš Latvijā 2015. gadā
ZVA analīze liecina, ka Latvijā ģenēriskās zāles visvairāk lieto sirds—asinsvadu sistēmas slimību ārstēšanai, nervu sistēmas, gremošanas trakta un vielmaiņas problēmu risināšanai.
Ieguvums — ne tikai divreiz lētāk
FDA norāda, ka ģenēriskās zāles maksā par 80—85 % mazāk nekā oriģinālās. [3] ZVA aprēķini liecina, ka Latvijā šī cenu atšķirība ir vidēji divreiz mazāka, taču dažās kardiovaskulāro zāļu grupās pat deviņas reizes mazāka (3. un 4. attēls). Eksperti piebilst: ieguvums no ģenēriskajām zālēm ir plašāks nekā tikai lētums. Viens no būtiskākajiem ieguvumiem ir zāļu pieejamība, kas veicina laicīgu terapijas sākšanu un līdzestību. [1]
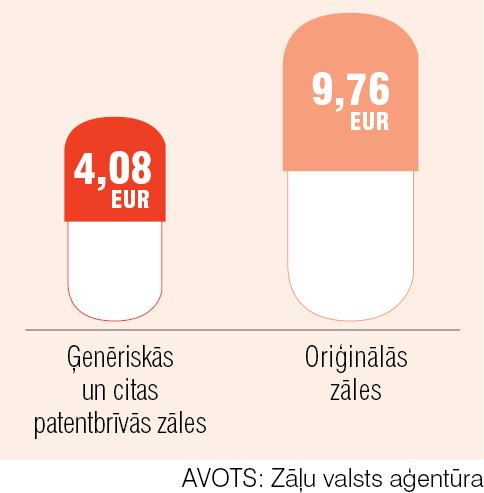

3. attēls
Zāļu iesaiņojuma vidējā cena 2015. gadā Latvijā (eiro ar PVN)
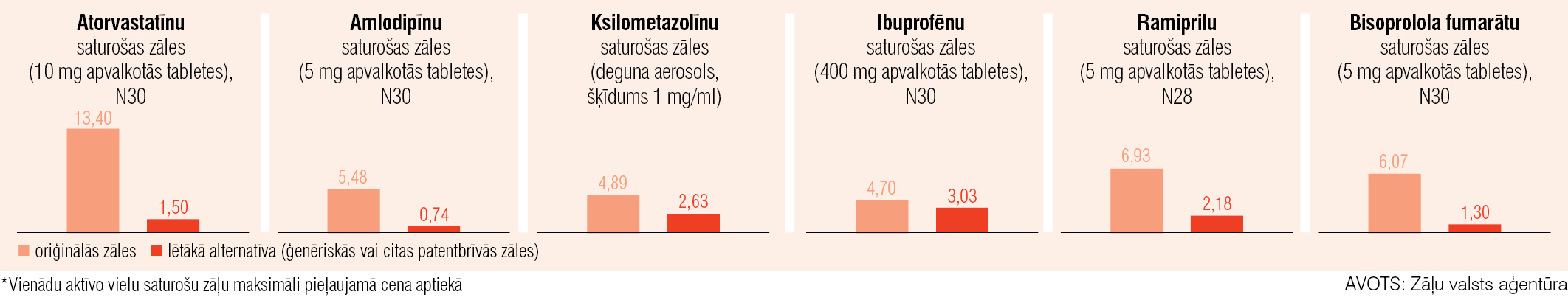

4. attēls
Zāļu cenu salīdzinājums (eiro ar PVN)*
Latvijā līdzīgi kā daudzās citās valstīs kompensējamo zāļu jomā darbojas mehānisms, kas ārstam uzliek par pienākumu terapiju sākt ar lētākajām līdzvērtīgas efektivitātes zālēm (pacientam, kas sāk lietot kompensējamās zāles, ārsta pienākums ir receptē rakstīt zāļu vispārīgo nosaukumu, bet farmaceita pienākums — izsniegt lētākās līdzvērtīgās zāles), paredzot ārstam tiesības šīs zāles nomainīt pret citām, ja konstatētas konkrētā pacienta un zāļu bioloģiskās mijiedarbes problēmas.
Nacionālais veselības dienests norādījis, ka 2012. gadā iedarbinātie pacientu un valsts izdevumu samazināšanas mehānismi par kompensējamo zāļu iegādi pozitīvi ietekmējuši zāļu kompensācijas procesu. Ik gadu aug unikālo pacientu skaits, kuriem aptiekās izsniegti valsts kompensējamie medikamenti, — kopš 2012. gada šo pacientu skaits pieaudzis par teju 88 tūkstošiem.
Rīgas Stradiņa universitātes asociētā profesore, farmakoloģe Santa Purviņa uzsvērusi, ka valsts šādi var ieekonomēt naudu sarežģītākiem un dārgākiem medikamentiem un tādējādi palīdzēt arī citām pacientu grupām (pacientiem, kam nepieciešamas monoklonālās antivielas, reimatoīdā artrīta slimniekiem u.c.). “Ja nerīkosimies taupīgi, atstāsim aiz svītras ļaudis, kam gadiem ilga gaidīšana pēc palīdzības var izrādīties dzīvības cenā. Valsts nodrošina standarta palīdzību, ko pamato pierādījumi. Kāpēc valstij būtu jāpiedāvā pilsoņiem braukt ar Ferrari? Tās uzdevums ir piedāvāt iespēju pārvietoties!” [4]
1. fakts
Ģenēriskās zāles nav identiskas oriģinālajām zālēm, bet tikpat efektīvas, drošas un kvalitatīvas
Jā, ģenēriskās zāles nav identiskas oriģinālajām zālēm, bet to savstarpējo aizvietošanu pamato fakts, ka tās ir līdzvērtīgas aspektos, kas uzskatāmi par svarīgiem. Un tie ir: efektivitāte, drošums, kvalitāte.
Pētījumi rāda, ka nav būtisku atšķirību oriģinālo un ģenērisko zāļu efektivitātē. Sistemātiskā apskatā un meta–analīzē, kur analizēja 38 pētījumus (kontrolētus, ar dalībnieku iedalījumu pēc nejaušības principa) par dažādām kardiovaskulāro zāļu grupām, secināja, ka nav pamata apšaubīt ģenērisko zāļu efektivitāti un drošumu. Pētījumā apskatīja bēta blokatorus, diurētiķus, kalcija kanālu blokatorus, antikoagulantus un statīnus, kā arī varfarīnu. [5]
Citā — epidemioloģiskā pētījumā (piedalījās 49 673 pacienti) — salīdzināja ģenēriskos metoprolola medikamentus ar oriģināliem, tie uzrādīja līdzvērtīgu ietekmi uz nopietnu kardiovaskulāro risku attīstību. [6] Ģenēriskos medikamentus bieži ražo tajās pašās rūpnīcās, kur oriģinālos. Ģenēriskie medikamenti tiek laisti tirgū pēc oriģinālo zāļu patenta termiņa beigām un satur to pašu aktīvo vielu tādā pašā devā vai koncentrācijā kā attiecīgās oriģinālās zāles. Abiem ir vienādas indikācijas un līdzvērtīga terapeitiskā efektivitāte un drošums. Taču šiem preparātiem var atšķirties izmantotās palīgvielas, zāļu forma, krāsa, smarža. Patentbrīvie medikamenti ir lētāki, jo nav jāveic preklīniskie un klīniskie pētījumi. Lai patentbrīvo medikamentu varētu izplatīt un lietot, jāpierāda tā bioekvivalence oriģinālajam preparātam. [7] Bioekvivalenci pamato zāļu biopieejamība, kas norāda aktīvās vielas absorbciju laika periodā. Biopieejamību raksturo divi parametri — maksimālā aktīvās vielas koncentrācija plazmā (Cmax) un laukums zem koncentrācijas laika periodā plazmā līknes (area under the plasma concentration time curve AUC). Šis rādītājs atspoguļo kopējo aktīvās vielas daudzumu, kas nonāk asinīs. Eiropas Medicīnas aģentūras (EMA) un FDA bioekvivalences definīcija formulē, ka ģenēriskā un oriģinālā preparāta Cmax un AUC rādītāju attiecības 90 % ticamības intervālam ir jāiekļaujas robežās no 80 % līdz 125 %. [1]
2. fakts
Uzskats, ka aktīvās vielas koncentrācija ģenēriskajām un oriģinālajām zālēm var atšķirties līdz pat 45 %, ir mīts
Šis priekšstats radies, jo mehāniski tiek izskaitļota bioekvivalences robeža, taču 90 % ticamības intervāla robeža 0,8—1,25 ir skaitlisks indekss un neatspoguļo reālās farmakokinētisko rādītāju atšķirības starp oriģinālo un ģenērisko preparātu. Lai rādītāji iekļautos šajā intervālā, biopieejamības atšķirība nedrīkst būt lielāka par 10 %. [8]
FDA izvērtēja 2070 pētījumus (veikti no 1996. gada līdz 2007. gadam), un biopieejamība ģenēriskajiem medikamentiem atšķīrās par 3,5 %. [9]
Bioekvivalences robeža attiecas ne tikai uz ģenēriskajiem medikamentiem, bet arī uz oriģinālo preparātu dažādām sērijām. FDA norāda: šāda atšķirība ir pieļaujama un ir arī starp dažādos laikos ražotiem oriģinālajiem preparātiem, turklāt tā ir līdzīga, ja salīdzina ģenēriskos—oriģinālos preparātus un oriģinālos—oriģinālos preparātus.
3. fakts
Bioekvivalences pētījumos jāpierāda biopieejamība, nevis aktīvā viela, tāpēc pētījumu statistiskā jauda ir mazāka
Arī šis ir biežs arguments: oriģinālo medikamentu pētījumos iesaistīti tūkstošiem pacientu, bet ģenērisko zāļu — mazāk par 50. Taču oriģinālo un ģenērisko zāļu pētījumu mērķis ir pavisam atšķirīgs! Biopieejamības pētījumos dalībnieku ir mazāk, jo uzdevums nav pierādīt aktīvās vielas efektivitāti — tas jau paveikts ar oriģinālo medikamentu. Biopieejamības pētījumos veselām brīvprātīgām personām nosaka medikamenta aktīvās vielas līmeni asinīs. Atsevišķos laika posmos katrs pētījuma dalībnieks saņem oriģinālo medikamentu un jauno ģenērisko medikamentu.
Ģenēriskajam medikamentam jāuzrāda tā pati aktīvās vielas koncentrācija asinīs, kāda sasniegta pēc oriģinālmedikamenta lietošanas. Starp zāļu produktu un citu tā versiju (ģenērisko) nav būtiskas atšķirības biopieejamībā (ātrumā un apjomā, kādā medikamenta aktīvā viela tiek absorbēta un kļūst pieejama tā darbības vietā), ja līdzīgā stāvoklī tiek lietota tā pati koncentrācija. Pieļaujamā starpība zāļu bioekvivalencē nerada terapeitiskās ekvivalences izmaiņas. Prof. Skutelis uzsver — biopieejamība būs atkarīga arī no cilvēka slimību buķetes. “Pētījumos iesaista relatīvi veselus cilvēkus, bet ārsta praksē parasti būs pacients, kam ir četras piecas slimības. Kādas zāles viņš lieto, kādas augu tējas dzer, kāda ir to mijiedarbība? Te arī sākas sarežģītā virtuve, kurā ārstam jābūt meistaram.”
4. fakts
Pacienti, kas lieto ģenēriskās zāles, ir līdzestīgāki
Kohortu pētījumā, salīdzinot oriģinālo un ģenērisko statīnu lietošanu cilvēkiem pēc 65 gadu vecuma, pētnieki secināja, ka ģenērisko zāļu lietotāji ir līdzestīgāki. Pacienti, kas terapiju sāka ar patentbrīvajiem statīniem, labāk ievēroja parakstīto zāļu lietošanas režīmu, par 8 % samazinājās kardiovaskulāro notikumu skaits, salīdzinot ar zīmolu statīniem. Ģenērisko zāļu grupā pacientiem uz 100 cilvēkgadiem novēroja par 1,53 klīniskiem notikumiem (mirstība vai hospitalizācija koronārās sirds slimības vai insulta dēļ) mazāk (TI no -2,69 līdz -0,19), salīdzinot ar oriģinālo preparātu lietotājiem. [10]
Foto: no DOCTUS arhīva
Pilnu raksta versiju lasiet Doctus 2016. gada augusta numurā