Autoimūna orbitopātija ir potenciāla redzi apdraudoša slimība, kam raksturīgas retrobulbāro audu iekaisīgas pārmaiņas un/vai orbītas taukaudu proliferācija, palielinot saistaudu un ekstraokulāro muskuļu tilpumu.
Līdz 90 % pacientu autoimūna orbitopātija klīniski saistīta ar autoimūnu tireotoksikozi. Apmēram 20 % pacientu autoimūna orbitopātija klīniski izpaužas pirms hipertireozes, 40 % — kopā ar tireotoksikozi, bet 10 % pacientu — autoimūna orbitopātija saistīta ar hronisku autoimūnu tireoidītu un hipotireozi.
Klīniskais gadījums
Paciente, 64 gadus veca, 31.10.2017. ar endokrinologa nosūtījumu akūtā kārtā stacionēta PSKUS ar sūdzībām par progresējošu redzes zudumu labajā acī, dubultošanos, plakstiņu tūsku, konjunktīvas iekaisumu, asarošanu, ierobežotu acs ābola kustīgumu labajā acī.
Slimības anamnēze
Pirmās sūdzības par dubultošanos kreisajā acī pacientei parādījušās 2016. gada decembrī. Ambulatori veikta magnētiskā rezonanse (MR) galvas smadzenēm, kur konstatēta viegli izteikta kreisā acs ābola proptoze, ievērojami palielināts m. rectus oculi inferior apjoms kreisajā orbītā (šķērsizmērs 0,8 × 1,5 cm). Slēdzienā radiologs šīs izmaiņas saista ar autoimūnu orbitopātiju. Pēc MR atbildes saņemšanas paciente konsultējas ar endokrinologu, kurš pacienti nosūta uz RAKUS i/v glikokortikosteroīdu pulsa terapijas kursa sākšanai autoimūnas orbitopātijas dēļ. Pacientei ambulatori noteikts arī vairogdziedzera hormonālais spektrs, kur diagnosticē hipotireozi, tāpēc sāk Euthyrox 25 µkg lietošanu no rīta, tukšā dūšā.
2017. gada sākumā (no janvāra līdz martam) paciente trīs reizes (katru reizi trīs dienu garumā) stacionēta RAKUS glikokortikosteroīdu pulsa terapijai, kur trīs mēnešu laikā i/v saņemtā Solu–Medrol deva bija 4,5 g. 2017. gada martā RAKUS veiktajās analīzēs: TSH 3,2560 mkSV/ml [], FT4 0,81 ng/dl [], AvTSHR 3,46 [].
Paciente izrakstīta ambulatori ar diagnozi:autoimūns tireoidīts, primāra hipotireoze, medikamentozi kompensēta; autoimūna abpusēja orbitopātija (OS > OD); diplopija. Rekomendē turpināt Euthyrox (Levothyroxine sodium) 25 µkg no rīta, tukšā dūšā, D3 vitamīnu — Oel Vigantol 5 pilienus 1 × dienā un bioselēnu.
Pēc izrakstīšanās no stacionāra
Pēc izrakstīšanās pacientei sūdzības par izmaiņām kreisajā acī nav bijušas, jutusies ļoti labi. 2017. gada maija beigās un jūnija sākumā parādījusies tūska labās acs augšējā plakstiņā un “it kā aizmiglojusies” redze labajā acī. Sākotnēji simptomiem nav pievērsusi uzmanību, bet pēc divām nedēļām parādījusies izteikta labās acs abu plakstiņu tūska un straujš redzes zudums.
Pacienti atkārtoti konsultē oftalmologi, kuri rekomendē Azopt pilienus un mākslīgās asaras, kā arī endokrinologa konsultāciju. No jūlija paciente atrodas regulārā endokrinologa uzraudzībā PSKUS ambulatorajā daļā, kur tiek atsākta i/v Solu–Medrol pulsa terapija 1 × nedēļā, devu rēķinot atbilstīgi pieļaujamai kopējai i/v glikokortikosteroīdu devai — 8000 mg (ieskaitot RAKUS saņemto devu 4500 mg). Terapijas fonā pacientei progresē sūdzības par asarošanu un graušanu acīs, pieaug abpusēja plakstiņu tūska, sāpes, grozot acs ābolu, īpaši — skatoties augšup, palielinās eksoftalms dx > sin un ar labo aci paciente praktiski neredz — redz tikai kontūras un pēdējās divas nedēļas pirms stacionēšanas parādās sūdzības par melniem laukiem pie skata uz augšu. Paciente joprojām turpina lietot Euthyrox 25 µkg.
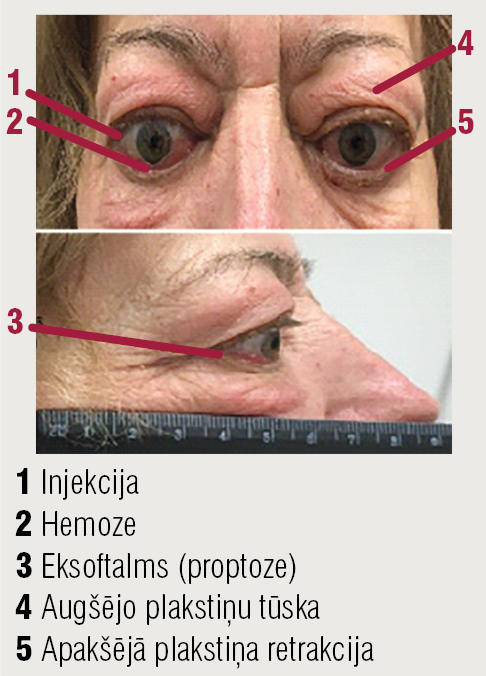

1. attēls
Autoimūnas orbitopātijas klīniskie simptomi
Atkārtota stacionēšana
Endokrinologs, izvērtējot pacientes sūdzības par progresējošu redzes zudumu un aktīvu autoimūnu orbitopātiju maksimāli pieļaujamās un saņemtās Solu–Medrol devas fonā, pacienti nosūta uz PSKUS, lai lemtu par tālāko terapijas taktiku. Stacionēšanas diagnoze: Greivsa slimība. Subklīniska hipertireoze. Aktīva autoimūna orbitopātija, smagas pakāpes dx > sin, rezistenta pret glikokortikosteroīdiem.
Slimību, dzīves un ģimenes anamnēze
Paciente strādājusi par skolotāju, šobrīd pensijā. Nesmēķē. Praktiski vesela, nopietnas slimības citās orgānu sistēmās noliedz. Ģimenes anamnēzē vairogdziedzera slimības noliedz.
Vispārējā izmeklēšana
Vispārējais stāvoklis apmierinošs, apziņa skaidra, kontakts labs. Āda silta, sausa, mēle valga, sārta, bez aplikuma. Vairogdziedzeris — gluds, mīksts, nesāpīgs, nedaudz palielināts, kakla un zemžokļa limfmezglus nepalpē. Sirdsdarbība ritmiska, 62 ×/min., TA 140/70 mmHg. Vezikulāra elpošana, frekvence 16 ×/min., SpO2 98 %. Perifēro tūsku nav.
Autoimūnas orbitopātijas klīniskās aktivitātes izvērtējums
Pacientei konstatē trīs pazīmes no septiņām (tabula):
- abpusēja augšējo plakstiņu tūska,
- hemoze,
- injekcija.
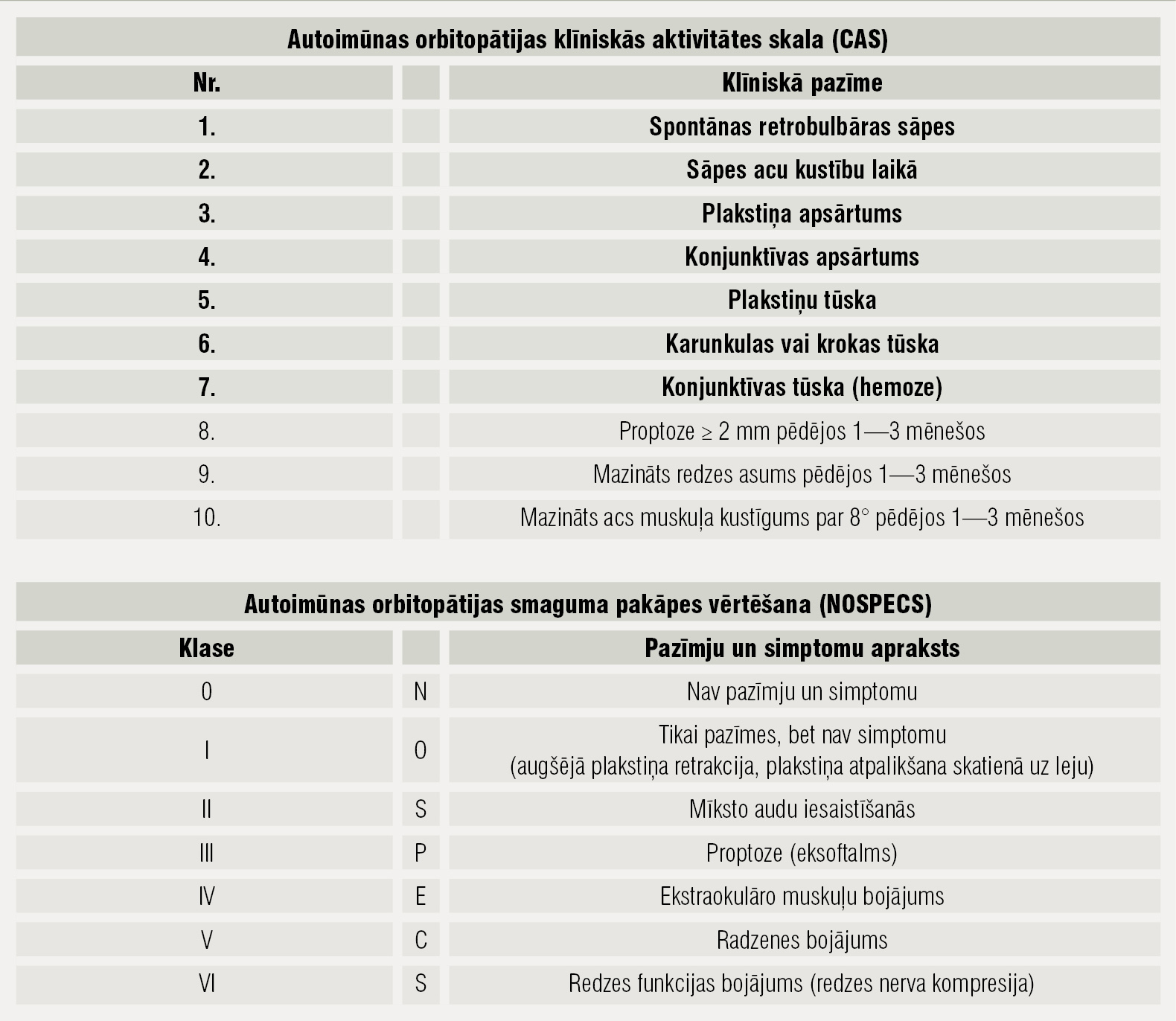

Tabula
EUGOGO kritēriji un NOSPECS klasifikācija
Autoimūnas orbitopātijas smaguma pakāpes izvērtējums
Orbitopātiju klasificē kā smagu, jo ir:
- eksoftalms (proptoze),
- abpusēja abu (augšējā un apakšējā) plakstiņa retrakcija,
- agophtalmus (nepilnīga acs aizvēršanās) dx > sin,
- pozitīvi acu simptomi — Dālrimpla, Mēbiusa, Štelvāga, Kohera un Fon Grēfes.
Izmeklējumi
31.10.2017. Pilna asinsaina, asins bioķīmija — norma, glikoze — 7,5 mmo/l (4,1—5,9 mmol/l), HbA1c — 6,7 % (4—6 %).
Hormonālais spektrs
31.10.2017. TSH — 0,05 uSV/ml (0,55—4,78), FT4 — 1,42 ng/ml (0,89—1,76), FT3 — 3,86 pg/ml (2,3—4,2).
6.11.2017. TSH — 0,12 uSV/ml (0,55—4,78), FT4 — 1,20 ng/ml (0,89—1,76), FT3 — 4,3 pg/ml (2,3—4,2).
Imunoloģija
6.11.2017. AvTPO — 10,91 SV/ml (0—5,6) un AvTSHR — 18 V/l (0—0,4).
Datortomogrāfija orbītām natīvā
2.11.2017. Deguna starpsiena ar septu pa kreisi, blakusdobumi bez patoloģiska satura. Abpusēji simetriski samērā izteikta proptoze (2. attēls), abpusēji palielināti acs kustību muskuļi, palielinājums skar visus muskuļus, izteiktāk palielināti m. rectus medialis inferior un superior, mazāk palielināti augšējie slīpie muskuļi. Maksimālais muskuļu Ø līdz 9 mm. Redzes nervi izstiepti. Orbītas galotnēs, iespējams, konkrementi. Nav redzami taukaudi ap redzes nervu proksimālo daļu. Acs ābola mugurējā kontūra bez deformācijas, redzes nervu distālā daļa apjomā lielāka nekā parasti. Paplašināti redzes nervu apvalki un likvors.
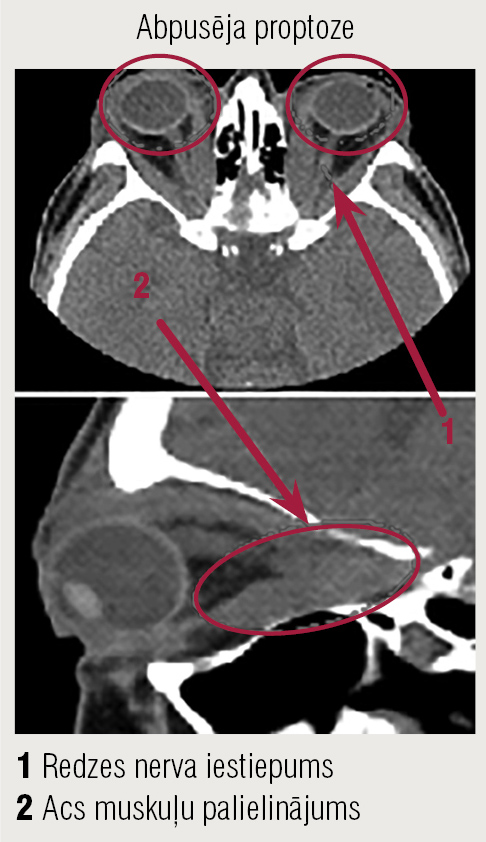

2. attēls
Datortomogrāfija orbītām natīvā
Secinājums: tipiska endokrīna abpusēja oftalmopātija ar simetrisku proptozi, visu acu kustību muskuļu palielinājumu, redzes nervu iestiepumu, iespējams, paplašinātiem apvalkiem un likvoru tāsdistālajās daļās.
Turpmākā taktika
Izvērtējot pacientes sūdzības un objektīvo atradi, lūgta otorinolaringologa konsultācija, lai lemtu par orbītas dekompresiju, lai gan ir aktīva autoimūna orbitopātija.
Oftalmologa konsultācija 5.11.2017. Slēdziens: aktīva autoimūna orbitopātija, smagas pakāpes, rezistenta pret glikokortikosteroīdiem. Keratopātija. Kreisās acs sekundārā glaukoma. Rekomendācijas: pacientei nepieciešama orbītas dekompresijas operācija. Turpināt iepriekš izrakstītos acu pilienus un mākslīgās asaras.
Otorinolaringologa konsultācija
6.11.2017.Objektīvi izmeklējot: abpusējs eksoftalms ar konjunktivītu. Deguna starpsienas deviācija. Citu patoloģiju ORL orgānos neatrod. Diagnoze: autoimūns tireoidīts, abpusēja orbitopātija. Deguna starpsienas deviācija. Rekomendācija: progresējoša redzes zuduma un n. opticus iestiepuma dēļ orbītu dekompresijas operāciju plānot neatliekamā kārtā (8.11.2017.).
Izrakstīšanās no nodaļas
Pacienti no endokrinoloģijas nodaļas izraksta ar klīnisko diagnozi: Greivsa slimība — difūza toksiska struma. Hipertireoze. Aktīva autoimūna orbitopātija, smagas pakāpes, rezistenta pret glikokortikosteroīdiem. Keratopātija. Kreisās acs sekundārā glaukoma. Glikozes panesības traucējumi glikokortikosteroīdu terapijas fonā.
PSKUS ORL nodaļa
7.—15.11.2017. Operācijas dēļ paciente pārvesta uz ORL nodaļu.
8.11.2017. — abu orbītu dekompresijas operācija. Speciālisti veic deguna starpsienas septoplastiku, FESS — abpusēji maksilotomiju, sfenoetmoidotomiju, endonazālu orbītu mediālās sienas dekompresiju un labās orbītas laterālās sienas dekompresiju.
Pēc orbītas dekompresijas operācijas (3. attēls) jau tās pašas dienas vakarā paciente atzīmē, ka beidzot redz medicīnisko personālu, nevis tikai neskaidras kontūras. Neesot arī melno plankumu, skatoties uz augšu.
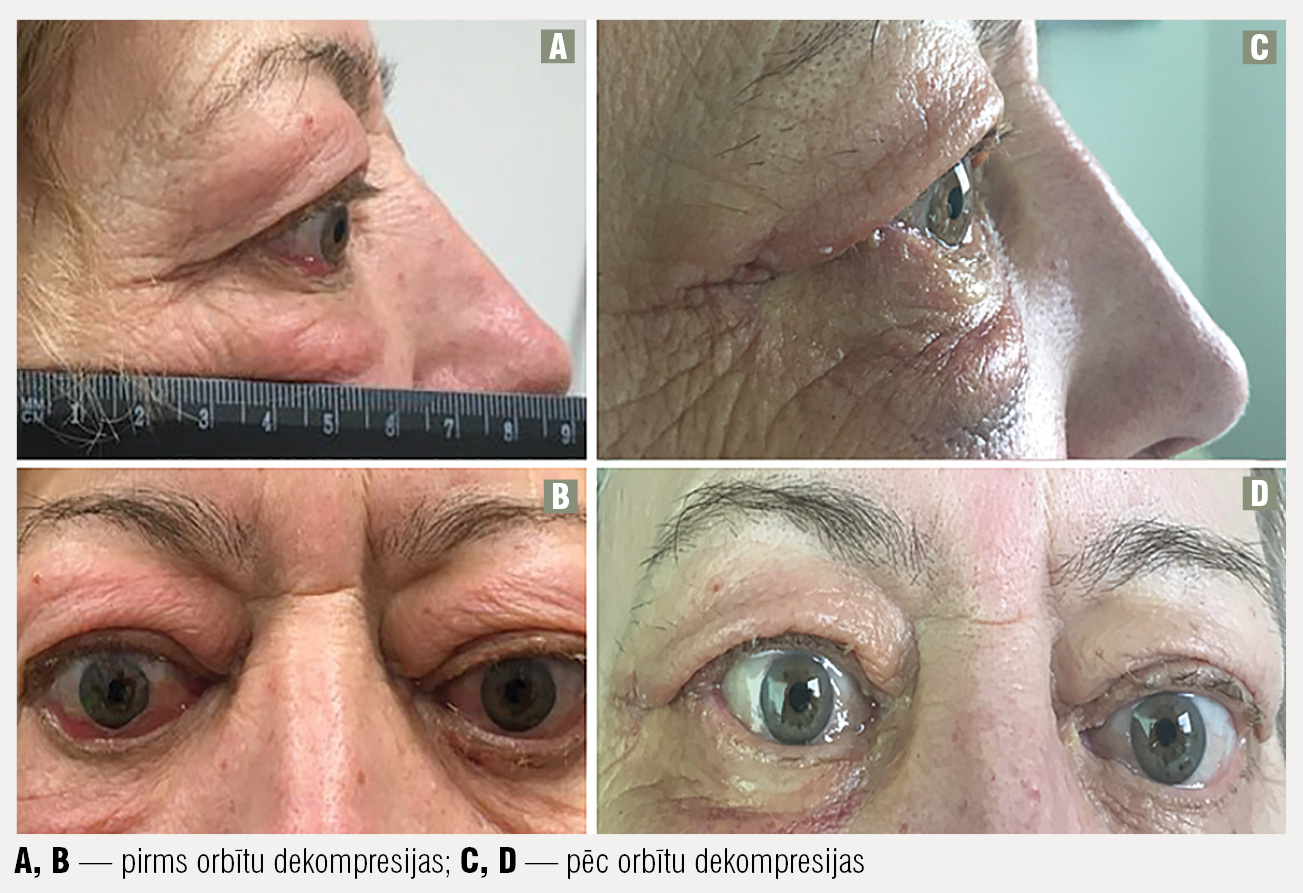

3. attēls
Pirms un pēc orbītas dekompresijas operācijas
Izrakstīšanās diagnoze
15.11.2017. Pacienti izraksta ambulatori ar klīnisko diagnozi: Greivsa slimība — difūza toksiska struma. Hipertireoze. Autoimūna orbitopātija, smagas pakāpes, rezistenta pret glikokortikosteroīdiem. Keratopātija. Kreisās acs sekundāra glaukoma. Deguna starpsienas septoplastika, FESS (abpusēji maksilotomija, sfenoetmoidotomija, endonazāla orbītu mediālās sienas dekompresija (08.11.17.). Glikozes panesības traucējumi.
Rekomendācijas:
- ģimenes ārsta, endokrinologa un oftalmologa uzraudzība;
- diētā ierobežot ātri asimilējamus ogļhidrātus (paciente informēta par produktiem ar augstu glikēmisko indeksu);
- acis sargāt no vēja, putekļiem, spilgtā gaismā nēsāt melnas saulesbrilles;
- izvairīties no smagumu celšanas, acs piepūles — maksimāli ierobežot televīzijas skatīšanos, lasīšanu;
- deguna dobuma kopšana ar Humer, ar deguna eļļu Rhinopanteina;
- tab. Dolmen (Dexketoprofenum) 25 mg × 2 p/o sāpju gadījumā;
- pēc trim nedēļām ambulatori noteikt TSH, FT4, FT3, Av pret TSHR, tad vizīte pie endokrinologa terapijas korekcijai;
- 12.12.2017. atkārtota apskate un ORL konsultācija PSKUS ORL nodaļā;
- sākt T. Thyrozoli 2,5 mg 1 × dienā.
Teorijas pārskats
Autoimūnas orbitopātijas izplatība vispārējā populācijā: ♀ : ♂ = 16 : 3 uz 100 000 iedzīvotājiem gadā. Visbiežāk autoimūna orbitopātija sievietēm attīstās 40—44 gadu vecumā un 60—64 gadu vecumā, vīriešiem 45—49 gadu vecumā un 65—69 gadu vecumā.
Etioloģija
Autoimūnas orbitopātijas etioloģiskie faktori var būt koriģējami un nekoriģējami.
Nekoriģējamie faktori:
- ģenētiskie faktori — autoimūna tireotoksikoze un hronisks autoimūns tireoidīts pirmās un otrās pakāpes radiniekiem; pētījumos pierādīta korelācija starp autoimūnu tireotoksikozi un orbitopātiju, ko izraisa patoģenēzē iesaistītie iekaisuma citokīni un interleikīni (IL–12, IL–6, IL–8, TNF), CTLA–4 (citotoksiskā T limfocīta antigēna 4) gēnu polimorfisms, kas saistīts ar autoimūnu tireotoksikozi;
- dzimums — biežāk slimo sievietes, turklāt autoimūna orbitopātija norit smagāk.
Koriģējamie faktori:
- smēķēšana — varbūtības attiecība autoimūnas orbitopātijas attīstībai: 7,7 smēķētājiem pret 4,3 nesmēķētājiem, turklāt smēķētājiem tā norit klīniski smagāk, smaguma pakāpe saistīta ar izsmēķēto cigarešu skaitu dienā. Smēķēšanai ir toksiska ietekme uz orbītas audu vaskularizāciju un imunoloģiskām pārmaiņām, kas izraisa saistaudu tilpuma palielināšanos orbītā, bet ne ekstraokulāros muskuļos. Pētījumos in vitro pierādīts, ka smēķēšana veicina glikozaminoglikānu (GAG) veidošanos un adipoģenēzi.
- stress;
- radioaktīvā joda lietošana risku autoimūnas orbitopātijas attīstībai palielina par 15—39 %.
Patoģenēze
Autoimūna orbitopātija — autoimūnas vairogdziedzera pārmaiņas pavadošs autoimūns process orbītas saistaudos, taukaudos un ekstraokulāros muskuļos. Orbītas audiem un vairogdziedzerim ir kopīgi antigēni — TSH (vairogdziedzeri stimulējošā hormona) receptori (šajā gadījumā), bet orbītas audos atrasti arī citi antigēni: tireoperoksidāze (TPO), IGF–1 receptori, muskuļu proteīni — D1, flavoproteīns, kalciju saistošais proteīns — kalsekvestrīns u.c.
Autoreaktīvie T limfocīti pazīst vairogdziedzera un orbītas audu kopīgos antigēnus. T limfocīti infiltrējas orbītas audos, asaru dziedzera audos, ekstraokulāros muskuļos. MHC II klases molekulas prezentē sadalītā TSH receptora peptīdus CD4+ T limfocītiem (helperiem) — veidojas Ag—Av komplekss, kam seko CD8+ T limfocītu un B limfocītu aktivācija un autoantivielu veidošanās. Procesa rezultātā izdalās citokīni: T helperi 1 (IL–2, gamma IFN, TNF alfa) un T helperi 2 (IL–4, IL–5, IL–10). Makrofāgi, fibroblasti, adipocīti arī veicina citokīnu sintēzi un sekrēciju: IL–1, IL–6, IL–16, augšanas faktoru TNF bēta.
Citokīni veicina fibroblastu proliferāciju, kuri arī sintezē un sekretē skābos GAG, kas retrookulārajai telpai piesaista šķidrumu, radot tūsku periorbitālajos audos, proptozi un ekstraokulāro muskuļu palielināšanos, nodrošina preadipocītu diferencēšanos par adipocītiem ar sekojošu to masas palielināšanos.
Orbītas fibroblasti var diferencēties arī par miofibroblastiem vai lipofibroblastiem.
Klīniskās pazīmes
Galvenās orbitopātijas pazīmes (4. attēls):
- acs plakstiņu retrakcija,
- mīksto audu pārmaiņas,
- proptoze jeb eksoftalms,
- n. opticus neiropātija/radzenes pārmaiņas,
- šķielēšana/diplopija.
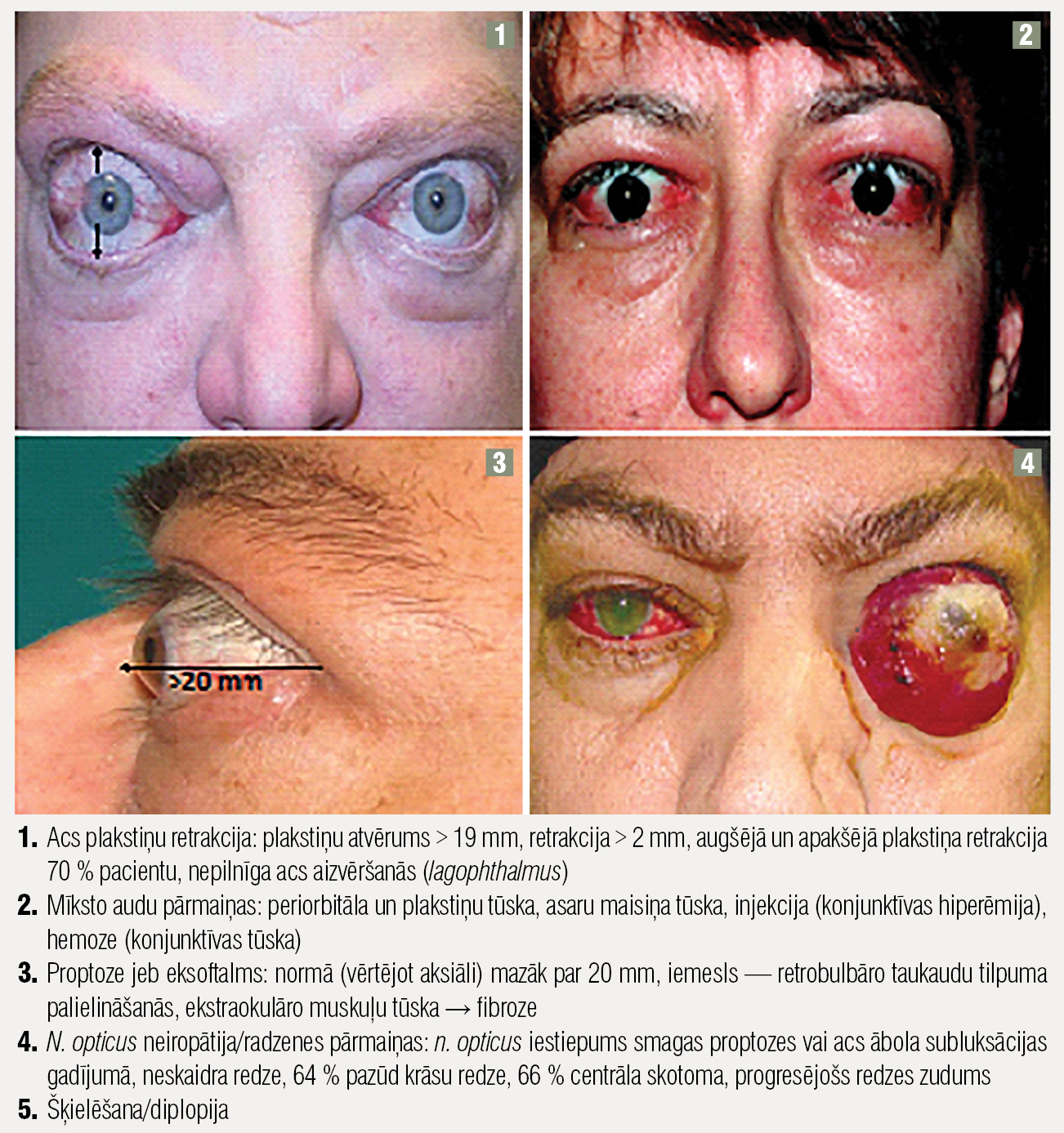

4. attēls
Klīniskās izpausmes
Autoimūnas orbitopātijas klīniskās pazīmes iedala divās fāzēs: aktīvajā, kas pēc noteikta laika pāriet neaktīvajā. Aktīvā fāze — plakstiņu tūska un apsārtums, konjunktīvas tūska un hiperēmija, eksoftalms, dubultošanās, radzenes čūla, redzes zudums n. opticus kompresijas dēļ. Neaktīvā fāze — neatgriezeniskas izmaiņas, kas izpaužas ar neatgriezenisku eksoftalmu, plakstiņu restrikciju, persistējošu restriktīvu šķielēšanu.
Mīksto audu izvērtējums ir ļoti būtisks, taču jāņem vērā, ka tā ir subjektīva metode. Lai izvērtējums, nosakot slimības aktivitāti, būtu maksimāli precīzs, izstrādātas īpašas izvērtējuma skalas. 1999. gadā tika nodibināta asociācija EUGOGO (European Group of Graves Orbitopathy), kas apvienoja astoņu Eiropas valstu ekspertus no dažādiem centriem, lai izveidotu vienotus ieteikumus Greivsa orbitopātijas diagnostikai un terapijas stratēģijai.
EUGOGO iesaka izmantot septiņus kritērijus: katra klīniskā pazīme atbilst vienam punktam, šos punktus izmeklēšanas gaitā summē. Pēc klīniskās aktivitātes novērtēšanas jāizvērtē orbitopātijas smaguma pakāpe — to veic oftalmologs. Ar šo skalu var izvērtēt arī terapijas efektivitāti. Mazinoties procesa aktivitātei, mazinās arī orbitopātijas klīniskā smaguma pakāpe. Orbitopātijas smaguma pakāpes izvērtēšanai izmanto NOSPECS klasifikāciju — tā ir populārākā klasifikācija, ko izveidojusi Amerikas Vairogdziedzera asociācija un ko sāka izmantot 1969. gadā (tabula).
Svarīgi atcerēties, ka orbitopātijas aktivitāte nav sinonīms orbitopātijas smaguma pakāpei.
Diagnostika
Analīzes: TSH, brīvais T3, brīvais T4, AvTPO, AvTSHR, slimības aktivitātes skala. Oftalmologa konsultācija: orbitopātijas smaguma pakāpes noteikšana, datorizētā redzes lauku perimetrija, ehobiometrija. Lai precizētu ekstraokulāro muskuļu palielinājumu, tūsku, orbītas taukaudu daudzumu, redzes nerva kompresiju vai iestiepumu, veic DT vai MR.
Svarīga arī ORL konsultācija: ja redzes nerva kompresija vai redzes nerva iestiepums — jāplāno orbītas dekompresijas operācija.
Ārstēšana
Ārstēšanas plānu pēc slimības klīniskās aktivitātes un smaguma pakāpes individuāli pielāgo katram pacientam.
Viens no galvenajiem priekšnosacījumiem — smēķēšanas atmešana. Ļoti būtiska ir arī acu kopšana, aizsardzība: mākslīgās asaras, rehidratējošas ziedes radzenes aizsardzībai, acu aizklāšana gulēšanas laikā, saulesbrilles ar UV filtriem spilgtā gaismā, sargāt acis no vēja, putekļiem, bet vidēji smagas/smagas orbitopātijas gadījumā — izvairīties no fiziskas slodzes un smagumu celšanas, pastiprinātas acu noslogošanas (TV, dators, adīšana, lasīšana).
Jānodrošina normāls vairogdziedzera hormonālais spektrs. Aktīvas autoimūnas orbitopātijas ārstēšana ar imūnsupresīvu terapiju — glikokortikosteroīdiem intravenozi lielās devās, taču, ja attīstās rezistence pret glikokortikosteroīdiem, var apsvērt terapiju ar citiem imūnsupresantiem: ciklosporīnu A, ciklofosfamīdu kombinācijā ar lielām glikokortikosteroīdu devām (p/o), bet jāatzīmē, ka efektivitāte nav pierādīta pārliecinoši, turklāt šiem medikamentiem ir daudz blakusparādību.
No jaunākām terapijas metodēm rezistences pret glikokortikosteroīdiem sakarā jāmin rituksimabs — monoklonālā antiviela, kas samazina AvTSHR, B limfocītu darbību retroorbitālos audos, un somatostatīna analogi, kaut gan ir pretrunīgi ziņojumi par oktreotīda sekmīgu izmantošanu, turklāt oktreotīds neietekmē proptozi, dubultošanos, plakstiņu retrakciju.
Neaktīvās fāzes laikā apsver rekonstruktīvu rehabilitējošu ķirurģisko ārstēšanu — orbītas dekompresiju, šķielēšanas korekciju, plakstiņu rekonstrukciju. Orbītas dekompresiju parasti veic tikai stabilas orbitopātijas gadījumā, vienīgais izņēmums — ja ir progresējošs redzes zudums un terapija ar glikokortikosteroīdiem ir neefektīva.