Klīniskā gadījuma demonstrācijā paciente ar hroniska C vīrushepatīta infekciju, kas netika savlaicīgi ārstēta: paciente uz stacionāru devās novēloti, viņai bija tipiskas aknu cirozes komplikācijas – sepse un asiņošana no barības vada vēnām.
Klīniskā gadījuma demonstrācija
(dr. S. Lugovska)
Sūdzības un anamnēzes dati
Paciente, 53 gadus veca, hospitalizēta š. g. 22. septembrī ar neatliekamo medicīnisko palīdzību (NMP), nosūtīšanas diagnoze: hepatīts? Aknu ciroze?
No anamnēzes zināms, ka 2009. gadā pacientei veikta osteoplastiska trepanācija intracerebrālas hemorāģijas dēļ, pēc tās parādījās epilepsija, bet pēc dažiem mēnešiem tajā pašā gadā tika diagnosticēta hroniska C vīrushepatīta infekcija. Šī hepatīta dēļ paciente detalizēti netika izmeklēta. Kursu veidā viņa periodiski lietoja karsilu.
Apmēram nedēļu pirms hospitalizācijas paciente saslimusi akūti, bijusi febrila ķermeņa temperatūra līdz 39 °C, to pavadījis drudzis, parādījušās sāpes mugurā, izteiktāk nieru rajonā. Visu nedēļu paciente novērojusi elpas trūkumu. Mājās lietojusi paracetamolu pa 1 tabletei 3-4 reizes dienā, turpinājusi lietot pretepilepsijas zāles. Visu šo nedēļu paciente ārstējusies pati. Sūdzībām pieaugot, īpaši sāpēm mugurā, un saglabājoties augstai ķermeņa temperatūrai, viņa ar NMP tiek hospitalizēta.
Objektīvā atrade
Iestājoties stacionārā, stāvoklis smags. Āda bāla, ir zemādas asins izplūdumi (uz sejas, ķermeņa). Asins izplūdumi parādījušies pirms divām nedēļām pēc epilepsijas lēkmes, kad viņa mājās bija nokritusi. Pacientei ir paaugstināta temperatūra 38 °C, diezgan izteikta aknu smaka no mutes, sāpes visā ķermenī, turklāt tik spēcīgas, ka viņa praktiski ir guloša, ar grūtībām spēj pagriezties. Visu nedēļu pirms hospitalizācijas viņa mājās praktiski nav staigājusi.
Hemodinamika stabila - sirdsdarbība ir 88 ×/min., TA 120/80 mm/Hg. Virs plaušām vezikulāra elpošana. Vēders palielināts apjomā, ir ascīts, hepatosplenomegālija. Uz apakšstilbiem palpatori ir pastozitāte.
Laboratoriskā un instrumentālā atrade
Asinsaina: Leik. 5,7 10ˆ9/l; Er. 4,0 10ˆ12/l; Hg 115 g/l; Tr. 78 10ˆ9/l.
Asins bioķīmija: AlAT 49 u/l; AsAT 98 u/l; GGT 34 U/l; kreat. 44 µmol/l; K 3,8 mmol/l; CRO 75,6 mg/l.
Koagulogramma: APTL 37,1 s; protrombīna indekss 62,9%; INR 1,2; D-dimēri 2,22 mg/l.
Urīna analīze: brūns; dzidrs, olb. 0,75 g/l; bilirub. 17 µmol/l; er. 30 µl.
RTG thoracis: fibrotiskas pārmaiņas plaušās.
Vēdera dobuma US: liesa 18,4 × 6,35 cm, gluda, homogēna. Difūzs aknu parenhīmas bojājums. Hepatosplenomegālija.
Darba diagnozes
Hroniska C vīrushepatīta infekcija. Aknu ciroze.
Sepse?
Epidurīts? Spondilodiscīts?
Terapija
Oxacillini 2 g × 4 i/v; Ciprofloxacini 400 mg × 2 i/v; Propranololi 10 mg × 2 p/o; Verospironi 50 mg × 2 p/o; Omeprazoli 20 mg × 2 p/o; Lactulose.
Tālākie izmeklējumi
Urīna uzsējums: negatīvs.
Slēptās asinis: negatīvs.
Asins uzsējums: MS. St. Aureus.
Lai izslēgtu septisku endokardītu, veikta EhoKG: papildstruktūras uz vārstuļu virām pārliecinoši neredz.
Pacienti konsultē neirologs, diagnozes precizēšanai rekomendēts MRI izmeklējums muguras krūšu un jostas daļai. Slēdziens: Th6-Th8 skriemeļu ķermeņu kompresijas lūzumi - subakūti. Iespējama izteikti plāna epidurāla hematoma vai iniciāla flegmona Th7-Th11.
Krūškurvja DT: izteikts varikozs tīklojums ap barības vadu. Nav datu par PATE.
Vēdera dobuma DT: abpusējs akūts pielonefrīts. Aknu ciroze. Portāla hipertensija. Splenomegālija. Ascīts.
Slimības gaita
Laboratorisko rādītāju izmaiņas skat. 1. tabulā. Tā kā pacientei pieaug CRO, tiek koriģēta antibakteriālā terapija un sākts piperacilīns/tazobaktāms 4,5 g 3 × d i/v.
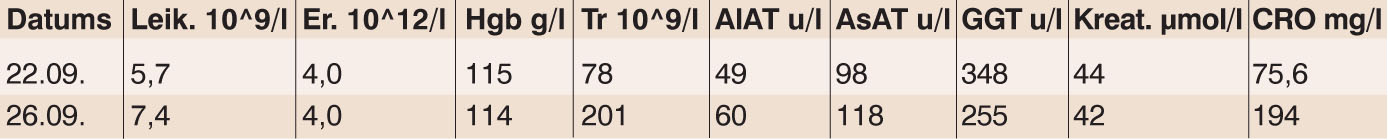

1. tabula
Laboratorijas rādītāju izmaiņas dinamikā
Paciente no 26. līdz 29. septembrim jūtas ievērojami labāk, sāpes mugurā mazinās, viņa staigā, samazinās ascīts, normalizējas ķermeņa temperatūra. 29. septembrī pievienojas masīva vemšana ar asinīm, recekļiem. Ir hipotensija. Operāciju zālē tiek veikta neatliekama ezofagogastroduodenoskopija, kur redz masīvu asiņošanu no gremošanas trakta augšdaļas, visticamāk, no barības vada vai kardijas varikoza vēnu mezgla. Izmeklējuma laikā pacientei apstājas sirdsdarbība, paciente tiek reanimēta. Pēc stāvokļa stabilizācijas ievada Blekmora zondi. Novērošanai un terapijai pacienti pārved uz reanimācijas nodaļu. Arī tālākajā gaitā pacientei ir nestabila hemodinamika, atkārtoti tiek veikti reanimācijas pasākumi. 29.09.13. pacientei iestājas exitus letalis.
Klīniskā diagnoze
Hroniska C vīrushepatīta infekcija
Aknu ciroze
Aknu encefalopātija
Portāla hipertensija
Splenomegālija
Ascīts
Barības vada vēnu varikoze
Masīva asiņošana gremošanas trakta augšdaļā, visticamāk, no barības vada vai kardijas varikoza vēnu mezgla (29.09.13.)
Kardiopulmonāla reanimācija (29.09.13.)
Sepse
Abpusējs akūts pielonefrīts
Th6-Th8 skriemeļu ķermeņu kompresijas lūzumi - subakūti. Iespējama izteikti plāna epidurāla hematoma vai iniciāla flegmona Th7-Th11
Stāvoklis pēc osteoplastiskas trepanācijas 2009. gadā
Simptomātiska epilepsija
Diskusija
Prof. V. Pīrāgs: Piekrītu, ka pacientes stacionēšana bija novēlota, bet varbūt mums būtu izdevies viņu stabilizēt kādu laiku. Vai tikai hroniska C vīrushepatīta infekcija bija iemesls aknu cirozei? Varbūt bija vēl toksiski, medikamentozi bojājumi, jo viņai bija epilepsija?
Dr. S. Lugovska: Epilepsija viņai parādījās pēcoperācijas periodā pēc galvaskausa operācijas.
Prof. V. Pīrāgs: Vai pacientei bija alkohola lietošana anamnēzē?
Dr. S. Lugovska: Paciente to noliedza, bet es to pilnībā neizslēdzu.
Prof. U. Dumpis: Mēs pilnībā nevaram izslēgt alkohola lietošanu, lai gan to noliedza, jautājot dažādos veidos. Par to varētu liecināt arī tas, ka AsAT rādītājs bija augstāks par AlAT, arī GGT bija paaugstināts. Turklāt paciente bija lietojusi viņai toksisku paracetamola devu un pilnībā nebija izslēgta arī nimesulīda lietošana. Iespējams, tas bija kombinēts - toksisks un medikamentozs aknu pasliktinājums. Tas ir raksturīgi, ka cirozes pacientiem ir tendence uz sepsi, bet sepse un asiņošana veicina encefalopātijas pastiprināšanos, arī pacienta nāvi. Veidojas apburtais loks.
Paciente bija konsultējusies arī Latvijas Infektoloģijas centrā (LIC), bet nebija dziļāk izmeklēta. Mums nebija informācijas ne par vīrusu genotipu, ne arī aknu biopsiju. Pacientei iestāšanās brīdī stacionārā bija aknu smaka no mutes, encefalopātijas pazīmes, anamnēzes vākšana šādos apstākļos, iespējams, nebija pilnīga.
Prof. I. Folkmane: Vai Latvijā pirms C vīrushepatīta terapijas identificē genotipu?
Dr. P. Aldiņš: Vīrusa genotipu nosaka mūsu molekulārās ģenētikas laboratorijā, kā arī Latvijas Infektoloģijas centrā.
Prof. I. Folkmane: Man ir iespaids, ka mēs esam ļoti kūtri aknu biopsijas veikšanā. Aknu fibrozei tas ir viens no galvenajiem faktoriem pirms terapijas. Īsti nav skaidrs, kurš veic aknu biopsiju - hepatologs, gastroenterologs, radiologs?
Dr. P. Aldiņš: Latvijā veic aknu biopsijas. Arī vadlīnijās iestrādāts, ka aknu biopsija ir viens no rādītājiem, kam noteikti jābūt pirms C hepatīta terapijas. Biopsiju mūsu slimnīcā veic radiologi US kontrolē. Mērķtiecīgi un precīzi. Ja pacientam ir hipokoagulācija, kas neļauj veikt parastu transkutānu aknu biopsiju, tiek veikta transjugulārā aknu biopsija, arī to pie mums veic.
Prof. U. Dumpis: Arī CC, CT, TT pacienta genotipu, kas paredz ārstēšanas iznākumu, mēs varam noteikt Biomedicīnas centrā.
Prof. V. Pīrāgs: Vai ir aplēses, cik pacientiem potenciāli būtu vajadzīga šī terapija? Ja jau tagad tik daudz zinām par molekulāro genotipēšanu, vai varam noteikt devas efektivitāti ar kaut kādiem īsajiem testiem, lai atdalītu responderus no ne-responderiem, negaidot 48 nedēļas?
Dr. P. Aldiņš: Par rekomendācijām Latvijā. Pirmo terapijas efektivitāti vērtē pēc 12 nedēļām, nosakot vīrusa slodzi. Terapiju turpina, ja vīrusa slodze ir zem noteikšanas sliekšņa jeb samazinājusies par divām kārtām. Eiropā rekomendācijās pacientiem, ko ārstē trīskārši, vīrusu slodzi nosaka pēc četrām terapijas nedēļām. Ja šiem pacientiem pēc četrām terapijas nedēļām vīrusa slodze samazinājusies par divām kārtām, ir arī vislielākās cerības pilnīgi izārstēties. Savukārt tiem, kam ceturtajā nedēļā nav dinamikas, terapiju nevajadzētu turpināt. Pēc Latvijas vadlīnijām pirmo terapijas efektivitāti joprojām izvērtē pēc 12. nedēļas.
Man nav precīzu datu, cik cilvēku Latvijā būtu jāārstē. LIC gadā ārstē 400-600 pacientu. Bērnu klīniskajā universitātes slimnīcā - maz. Mēs arī ārstējam salīdzinoši maz. Tātad kopā Latvijā gadā reāli ārstē ap 600-700 pacientu.
Varētu būt, ka vajadzība pēc terapijas ir vairāk nekā 1000 cilvēkiem gadā. Tie būtu pirmreizēji ārstētie pacienti. Cik neefektīvi ārstēto pacientu vajadzētu ārstēt jau ar citu veidu zālēm? Šobrīd tādu datu nav. Aptuveni diviem trim tūkstošiem cilvēku būtu vajadzīga terapija ar jaunajām zālēm. Bet tie ir tikai statistikas dati un nav pamatoti.
Vakcīnas pret vīrushepatītu C joprojām nav. Efektīva terapija ir daudz tuvāka kā vakcīna, galvenā cerība ir radīt iespējami labākas zāles, ar kurām izārstēt. Radīt vakcīnu šobrīd izskatās pārāk sarežģīti.
Prof. U. Dumpis: Vismaz 2% Latvijas iedzīvotāju varētu būt C hepatīts. Protams, liela daļa no tiem nav ārstējama dažādu iemeslu pēc. Daļai varētu būt nepieciešami jaunie medikamenti, kas maksās 20-30 tūkstošus latu par ārstēšanas kursu. Diezin vai tās būs lētākas, vismaz pirmajos gados. Tas tiešām ir milzīgs finansiāls slogs. Kādi ir risinājumi? Galvenais - pārtraukt inficēšanu, transmisiju. Protams, ārstēšana ir viens no veidiem, kā pārtraukt transmisiju, samazināt inficēto cilvēku skaitu, bet ir arī citi risinājumi, piemēram, māsām mainīt cimdus pēc manipulācijas ar katru pacientu, sekot līdzi, kas notiek tetovēšanas salonos, i/v narkomāniem. Katrs jauns pacients, kas inficējas, rada milzīgus izdevumus valstij. Diemžēl profilaktiskajam darbam (C hepatīta gadījumā) Latvijā praktiski nav nekādu līdzekļu.
Gribēju uzsvērt, ka C hepatīta pacienti, kas nevar ārstēties vai negrib ārstēties, nedrīkst lietot alkoholu vispār, nevienu glāzi. Jo jebkura alkohola deva pasliktina aknu stāvokli. Savukārt kafija samazina cirozes attīstības risku.
Prof. V. Pīrāgs: Domāju, ka šī uzstāšanās rāda potenciālu, kāds ir mūsu infektologiem. Varbūt tieši jums jābūt tiem, kas veido jauno hepatoloģiju arī mūsu slimnīcā. Ne mazāk svarīgi ir būt arī starptautiskajā apritē. Ja jums būtu iespēja piekļūt klīniskiem pētījumiem, kas šobrīd ļoti intensīvi notiek, tas būtu būtiski gan mūsu pacientiem, gan visai globālajai pētniecībai.
"Jaunais" C vīrushepatīts
(dr. P. Aldiņš)
Šajā medicīnas jomā mēs esam ļoti lielu jaunumu priekšā, un mans mērķis ir informēt par jaunajām nostādnēm un tuvās nākotnes vīziju C vīrushepatīta ārstēšanas jomā.
Problēmas aktualitāte ir zināma - pasaulē tiek lēsts ap 170 miljoniem C vīrushepatīta pacientu. Cik Latvijā? Dati ir pretrunīgi: no 40 000 līdz 100 000 pacientu. Precīzāku datu nav. Skaidrs, ka arī Latvijā šādu pacientu ir ļoti daudz.
Hroniska C vīrushepatīta terapijas indikācijas
- Visiem iepriekš neārstētiem pacientiem, kam ir kompensēta slimība (AII).
- Neatliekami sākama terapija pacientiem ar izteiktu aknu fibrozi (Metavir F3-F4) (BII).
- Bez lielas kavēšanās terapija sākama pacientiem ar mērenu aknu fibrozi (Metavir F2) (BII).
- Individuālas indikācijas pacientiem ar vieglu slimības norisi (CII). [1]
Hroniska C vīrushepatīta terapija
Hroniska C vīrushepatīta terapiju, terapijas efektivitāti skat. 2. tabulā.


2. tabula
Hroniska C vīrushepatīta terapijas efektivitāte
Faktori, kas ietekmē hroniska C vīrushepatīta terapijas efektivitāti
Genotips
Pasaulē ir seši genotipi. 1. genotips ir visizplatītākais (~75%), viens no grūtāk ārstējamajiem genotipiem. Paradoksāli, ka bieži vien tieši 1. genotips saistās ar inficēšanos sadzīvē vai medicīniskā ceļā. Narkotiku lietotājiem biežāk ir 3. genotips, kas ilgu laiku šķita vieglāk ārstējams, šobrīd uzskati mainās - visvairāk pacientu mirst no 3. genotipa, jo šis vīruss veicina steatohepatīta attīstību, faktiski attīstās jauktas etioloģijas ciroze, kad iznākums ir nāve. Alkohols, iespējams, izraisa daudz postošāku turpinājumu nekā citiem genotipiem.
Pacienta un terapijas attiecības
- Iepriekš neārstēts pacients.
- Iepriekš ārstēts pacients:
o slimības recidīvs (HCV RNS vīrusa slodze atjaunojusies pēc terapijas) - šiem pacientiem ar mūsdienu jaunajām zālēm ir vislielākās cerības izārstēties,
o daļēji efektīva iepriekšējā terapija (HCV RNS vīrusa slodze mazinājusies, bet nav izzudusi vai atjaunojusies jau iepriekšējās terapijas laikā) - šos pacientus ārstēt ir grūtāk,
o absolūti neefektīva iepriekšējā terapija (HCV RNS vīrusa slodze terapijas laikā bez dinamikas) - šiem pacientiem grūti paredzēt labu terapijas iznākumu.
Interleikīna 28B gēna polimorfisms
Ja baltās rases pārstāvjiem ir CC gēna polimorfisms, cerības izārstēties salīdzinoši labas, ja nav CC polimorfisma, izārstēšanās cerības ievērojami vājākas. [2]
Fibroze
Jo izteiktākas morfoloģiskās izmaiņas aknās, jo cerības izārstēties mazinās. [3]
Trombocītu skaits un albumīna līmenis asinīs
Pavisam nopietns jaunums konstatēts franču pētījumā: pacientiem, kas saņēmuši modernos trīskāršās terapijas līdzekļus un kam ir mazs trombocītu skaits un zems albumīna līmenis asinīs, zāļu blakņu risks un nāves risks no šiem blakusefektiem ir 44%.
Dzīvībai bīstamu medikamentozās terapijas blakņu (SAE) un nāves risku HCV trīskāršās terapijas saņēmējiem skat. 3. tabulā. [4]


3. tabula
Dzīvībai bīstamu medikamentozās terapijas blakņu un nāves risks HCV trīskāršās terapijas pacientiem
Rase
Rase (baltajai rasei izārstēšanās izredzes labākas), vecums (sliktāki rezultāti vecākiem cilvēkiem), ĶMI (sliktāki rezultāti ar lielāku ĶMI), blakus slimības, ārstēšanas izmaksas (Latvijā tiek kompensēti 75% ārstēšanas izmaksu), motivācija.
Hroniska C vīrushepatīta terapija nākotnē
Medikamentu grupas ir dažādas. Sofosbuviram 2014. gada sākumā paredzēta reģistrācija ASV, pēc tam arī Eiropā. Zināms, ka Latvija ir to valstu sarakstā, kur šis preparāts jau sākotnēji tiks piedāvāts. Arī asunaprevirs, sovaprevirs 2014. gadā, iespējams, parādīsies tirgū.
Šobrīd noris dažādi pētījumi ar šiem medikamentiem. Ir liela cerība, ka daļu no tiem jau no 2014. gada sākuma varētu izmantot terapijā, turklāt shēmās bez interferona. Tas nozīmē, ka terapija daudziem cilvēkiem būs tikai perorāla, bez interferona nopietnajām blaknēm, no kurām cieš ļoti daudz pacientu. Terapijas kursi varētu būt īsāki. Ja šobrīd lielākoties runājam par 48 nedēļām, tad nākotnē terapijas ilgums varētu būt 24 nedēļas, varbūt pat 18 vai 12 nedēļas. Dažiem genotipiem, piemēram, 2. genotipam, 8-12 nedēļas ilgs ārstēšanas kurss drīz varētu būt realitāte.
Hroniska C vīrushepatīta terapijas nākotne Latvijā
Šobrīd pegilētais interferons un ribavirīns ir ar 75% kompensāciju no valsts puses. Terapija ar telaprevīru, boceprevīru šobrīd būtībā ir par naudu (Ls 18 000). Mūsu mērķis - 100% valsts zāļu kompensācija. Bet pats svarīgākais, manuprāt, ir speciālistu izstrādātas ārstēšanas rekomendācijas pacientiem Latvijā, ņemto vērā pacientu grupas, vīrusu paveidus.