Zem HOPS atrasts Mounier–Kuhn sindroms. Jautājums – vai ziņa, ka tas ir Mounier–Kuhn sindroms, kaut ko maina ārstēšanā? Visticamāk, nemaina, bet tas radikāli maina mūsu domāšanu – to, ka mēs visu neredzam vienādi un starp pamatkrāsām sākam redzēt starptoņus. Ko tas dod? Tas dod iespēju ģimenes ģenētiskai konsultēšanai, lai secinātu, ka tas nav vienīgais gadījums ģimenē. Pacienta radinieki nedrīkstētu smēķēt.
Klīniskā gadījuma demonstrācija
(Dr. Zaiga Kravale)
Sūdzības un slimības anamnēze
Pacients, 57 gadus vecs, II grupas invalīds, akūtā kārtā stacionēts Paula Stradiņa Klīniskajā universitātes slimnīcā.
Slimības anamnēze
Pacientam sūdzības par paaugstinātu temperatūru līdz 38ºC divas dienas, izteiktu elpas trūkumu, vairākas nedēļas mokošs klepus ar grūti atkrēpojamām krēpām. Citas slimības anamnēzē:
- kopš bērnības bieži bronhīti;
- progresējošs elpas trūkums slodzes laikā kopš 1990. gada;
- hroniskas obstruktīvas plaušu slimības diagnoze kopš 2000. gada;
- recidivējošas pneimonijas;
- atkārtoti stacionēts Paula Stradiņa Klīniskās universitātes slimnīcas 14. nodaļā (apm. 20 reizes), iepriekšējā reize pirms šīs stacionēšanas – 2011. gada martā;
- smēķē 30 paciņgadus;
- kaitīgos apstākļos neesot strādājis;
- alerģiskas reakcijas anamnēzē noliedz.
Pastāvīgi lietotie medikamenti: tiotropija bromīds 18 μg rītā, ipratropija bromīds/fenoterola hidromromīds 3–4 reizes dienā, teofilīna kapsulas 350 mg 3 reizes dienā (beidzamās dienas), epizodiski amoksicilīns/klavulānskābe.
Izmeklēšana
Objektīvā atrade
Vispārējais stāvoklis vidēji smags. Apziņa skaidra. Pacients kahektisks. Āda tīra, turgors normāls, perifēras tūskas neatrod. Palielinātus perifēros limfmezglus nepalpē. Elpo 18 reizes minūtē, virs plaušām auskultē difūzi novājinātu vezikulāru elpošanu. Virs labās plaušas vidusdaivas auskultē maigu krepitāciju. SpO2 92%. Sirdsdarbība ritmiska 88 reizes minūtē, asinsspiediens 138/70 mmHg. Vēders zem krūšu kaula līmeņa, palpējot mīksts, nesāpīgs. Aknu apakšējā mala labā ribu loka līmenī. Liesu nepalpē. Nieru rajons apklauvējot nesāpīgs.

1A
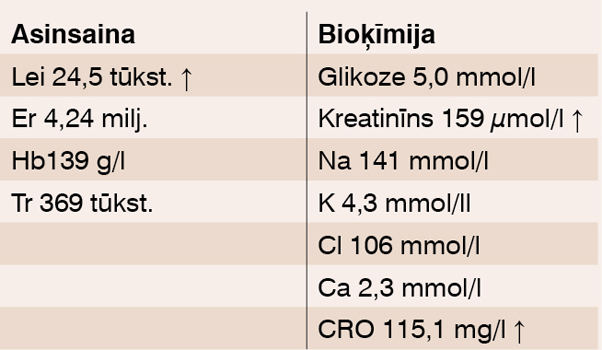
Laboratorie rezultāti
Tālākie izmeklējumi
Laboratorās atrades skat 1. tabulā, koagulogrammu skat. 2. tabulā.


5
Koagulogramma
EKG: sinusa tahikardija 110 ×`, PQ 0,14`, QRS 0,08`, QT 0,3`. Sirds elektriskā ass vertikāla. Labā ātrija un labā ventrikula hipertrofijas pazīmes.
Rentgenogramma krūškurvim: izteikta emfizēma, pneimofibroze, lb. vidusdaivas pneimonija (skat. 1. attēlu).
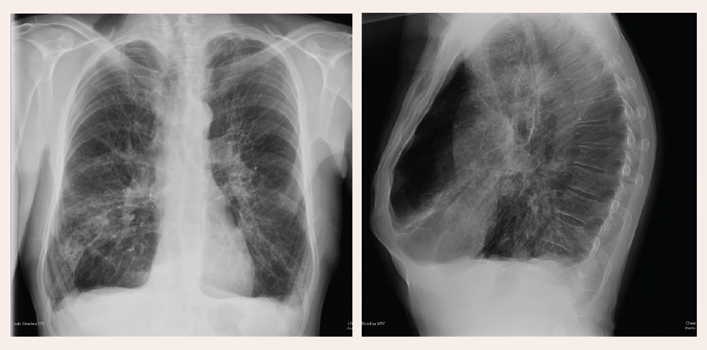

1. attēls
Izteikta emfizēma, pneimofibroze, lb. vidusdaivas pneimonija
Bronhodilatācijas tests: smagas pakāpes obstruktīva tipa nereversibla ventilācijas funkcijas nepietiekamība (skat. 2. attēlu).
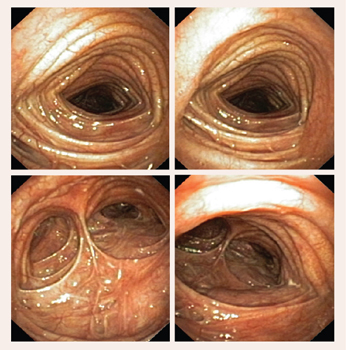

2. attēls
Izteikta trahejas un galveno bronhu dilatācija, atrofiska gļotāda
Sanācijas bronhoskopija – veikta divas reizes. Dinamikā CRO mazinās (skat. 3. tabulu).


3. tabula
CRO dinamika
Mikrobioloģija no bronhu skalojuma: izaug Streptococcus pneumoniae. Jutīgs uz:
- penicilīnu;
- eritromicīnu;
- ofloksacīnu;
- klindamicīnu;
- TMP/SMX (trimetoprimu/sulfametoksozolu);
- vankomicīnu.
Terapijā saņēma
- Ceftriaksonu 1 g × 1 i/v;
- klaritromicīnu 500 mg × 2 p/o;
- acetilcisteīnu 600 mg × 1 p/o;
- teofilīnu 350 mg p/o vakarā;
- paracetamolu 500 mg × 2 p/o;
- eifilīnu 15 mg × 1 i/v;
- diazepamu 5 mg uz nakti;
- inhalācijas ar ipratropija bromīdu/fenoterola hidrobromīdu un ambroksola hidrohlorīdu 2 reizes dienā.
Tiek mainīta antibakteriālā terapija uz ciprofoksacīnu 400 mg × 2 i/v un TMP/SMX 960 mg p/o.
Klīniskā diagnoze
Labās plaušas vidusdaivas pneimonija. Traheobronhomegālija. Smagas pakāpes HOPS.
Rekomendācijas
- Atmest smēķēšanu.
- Vakcinācija ar Pneumo23 un pretgripas vakcīna. Lietot:
o TMP/SMX 960 mg × 2 p/o vēl 2 nedēļas,
o ciprofloksacīnu 500 mg × 2 p/o vēl 2 nedēļas,
o acetilcisteīnu 600 mg × 1,
o tiotropija bromīdu 18 μg × 1,
o indakaterolu 150 μg × 1,
o ipratropija bromīdu/fenoterola hidrobromīdu – 2 inhalācijas pēc vajadzības.
- Bronhu sanācijas veikšanai pacientu rekomendē stacionēt Pulmonoloģijas un alergoloģijas centra dienas stacionārā.
Atkārtota stacionēšana
2011. gada 18.–23. decembrī pacients atkārtoti stacionēts 14. nodaļā. Sūdzības par elpas trūkumu, paaugstinātu temperatūru līdz 38,3ºC, klepu ar grūti atkrēpojamām krēpām. Antibakteriālajā terapijā lietojis tikai TMP/SMX, nav lietojis ciprofloksacīnu.
Izmeklējumi
Laboratorie izmeklējumi: CRO – 74,1 mg/l un Lei – 14,5 tūkst. Terapijā nozīmē ciprofloksacīnu 500 mg × 2 p/o, un uz terapijas fona iekaisuma marķieri mazinās: CRO – 16,5 mg/l un Lei – 5,9 tūkst. Pacientam tiek veiktas trīs bronhu sanācijas. Bronhos daudz strutaina sekrēta.
Datortomogrāfija plaušām: traheja ir izteikti paplašināta, deformēta visā tās garumā. Tāpat arī galvenie un subsegmentārie bronhi izteikti deformēti un paplašināti. Vēro arī bronhektāzes (skat. 3. attēlu). Slēdziens – HOPS aina, ar bullozu emfizēmu, hronisku deformējošu bronhītu, bronhektāzēm, īpaši skartas abas augšdaivas. Izteikta trahejas un abu galveno bronhu deformācija.
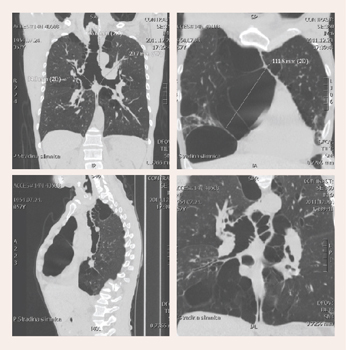

3. attēls
Datortomogrāfija plaušām
Gāzu difūzijas tests: normāla plaušu difūzijas kapacitāte.
Ķermeņa pletismogrāfija: plaušu emfizēma. Palielināts plaušu kopējais tilpums (+ 46%) un atlieku tilpums (+ 202%). Pacientu pēc datortomogrāfijas un ķermeņa pletismogrāfijas konsultē torakālais ķirurgs. Iesaka plaušu perfūzijas scintigrāfiju, apsvērt tilpuma redukcijas operāciju (skat. 4. attēlu).
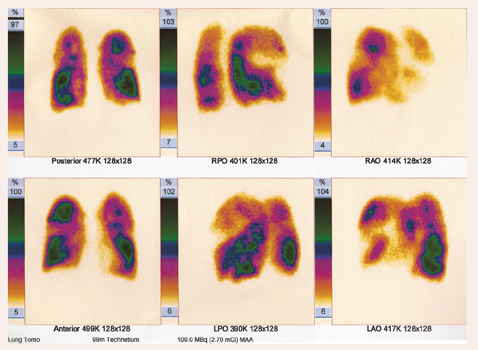

4. attēls
Pacientam ir izteikti preparāta krāšanās defekti, galvenokārt abās augšdaivās, labajā vidusdaivā, vairāk lejasdaivās
Klīniskā diagnoze
Mounier–Kuhn sindroms. Smagas pakāpes HOPS.
Rekomendācijas
o amoksicilīnu 500 mg × 2 p/o vēl 1 mēnesi,
o acetilcisteīnu 600 mg × 1 p/o ilgstoši,
o tiotropija bromīdu 18 mg pa 1 inhalācijai rītos,
o indakaterolu 300 μg pa 1 inhalācijai rītos;
- plānot tilpuma redukcijas operāciju slimības remisijas periodā.
Diskusija
Prof. V. Pīrāgs: Cik reizes jūs viņam ieteicāt atmest smēķēšanu?
Dr. Z. Kravale: Katru reizi.
Prof. V. Pīrāgs: Cik reizes piedāvājāt vakcinēties?
Dr. Z. Kravale: Katru stacionēšanas reizi. Galvenā problēma – sasniegt stabilu slimības remisiju, lai varētu veikt vakcināciju. Pacients apgalvo, ka esot samazinājis izsmēķēto cigarešu skaitu līdz dažām cigaretēm dienā.
Doc. V. Šiliņš: Šīs abas ir nopietnas problēmas. Īpaši par vakcināciju gribētu teikt – tā ir gan ārstu, gan pacientu problēma Latvijā. Mēs visiem spēkiem mēģinām par to runāt un aktualizēt, taču diemžēl vakcinācija tiek pieņemta ar ļoti lielām grūtībām.
Prof. V. Pīrāgs: Par sindroma ģenētiku. Es saprotu, ka ir kaut kāds defekts tieši elastībā.
Dr. E. Krustiņš: Grūti pateikt. Vairākums publikāciju pēdējos gados atsaucas uz 1962. gada rakstu. Nekādu pētījumu par šo jautājumu nav.
Prof. V. Pīrāgs: Būtu ļoti interesanti, ja varētu paņemt bioptātu un genotipēt. Tagad ir iespējas veikt genotipēšanu. Tas gan ir dārgi. Iespējams, šis sindroms tādās mazākās klīniskās izpausmēs ir biežāk, nekā mēs domājam.
Doc. V. Šiliņš: Šim pacientam ir iedzimta patoloģija, kas vairāk vai mazāk kaut kādā veidā ietekmē šo cilvēku un viņa hroniskās slimības smagumu, kā arī viņa ekonomisko stāvokli. Šā iemesla pēc daudzos gadījumos cilvēki arī vairāk smēķē. Ir zināms, šādiem pacientiem ir problēmas ar kaitīgiem faktoriem. Pacientam, kam sākumā ir tikai lielo gaisa ceļu patoloģija, 30 gadu laikā pievienojusies arī mazo gaisa ceļu patoloģija. Smēķēšana jau pamatā ietekmē mazos gaisa ceļus. Šeit parādās šī kombinētā situācija. Visi redzējāt, ka vēsturiski ir bijis periods, kad problēmu konstatē patanatomiski. Tad seko periods, kad mēs sākam klīniski analizēt pacientu. Savukārt šodien ir iespējama datortomogrāfiska izmeklēšana. Tādējādi mēs patiesībā šo patoloģiju varam konstatēt diezgan vienkārši un pacientam palīdzēt. Mums ir iespējas pacientu stabilizēt. Runājot par konkrēto gadījumu, iespēju robežās centīsimies šo histopatoloģisko preparātu izmeklēt un veikt genotipēšanu.
Prof. V. Pīrāgs: Šajā gadījumā jāpateicas rezidentu entuziasmam, ka esam atklājuši Mounier–Kuhn sindromu, kas slēpjas zem HOPS. Vēlos norādīt, ka mūsu klīnika kļūs spožāka, ja mēs šos retos gadījumus arī publicēsim, mēģināsim ģenētiski analizēt. Mums ir ļoti lielas iespējas Latvijā, citās Baltijas valstīs. To vajag izmantot, domāju, varētu iznākt spīdoša publikācija starptautiskā žurnālā.
Mounier–Kuhn sindroms
(Dr. Eduards Krustiņš)
Mounier–Kuhn sindromu autopsijā pirmo reizi apraksts 1897. gadā, savukārt klīnisko sindromu publicēja 1932. gadā. [1] 1962. gadā Katzq izveido pārskatu par šo slimību, kā arī ievieš nosaukumu Mounier–Kuhn sindroms. [2] Pacientu vecums var būt no 18 mēnešiem līdz 79 gadiem, vairākums vecāki par 30 gadiem. Sastopamība varētu būt 1:500–1:600. Analizējot 5324 DT uzņēmumus, sindroms tika atrasts 8 vīriešiem. [3] Mounier–Kuhn sindroms ir autosomāli recesīvi pārmantojams. Visbiežāk slimo vīrieši. Slimības pamatā ir garenisko elastīgo šķiedru atrofija, plānāka kļūst arī mucosa muscularis. Ir aprakstīta saistība ar dažādiem iedzimtiem sindromiem, piemēram, Ehler–Danlos, Marfan, Brachman de Lange, Kenny–Caffey.
Iedalījums
- 1. tips – simetriska, vienmērīga trahejas un bronhu paplašināšanās;
- 2. tips – divertikuļu un bronhektāžu parādīšanās uz vienmērīgi dilatētas trahejas un bronhu fona;
- 3. tips – tāpat kā 2. tipam, bet, slimībai progresējot, tiek skarti arvien sīkāki bronhi.
Klīnika
Sūdzības ir par klepu, elpas trūkumu, biežām elpceļu infekcijām. Ir aprakstīta arī asins spļaušana, spontāns pneimotorakss. Nereti pacientiem ilgstoši jau ir HOPS diagnoze.
Diagnostika
Diagnostikas standarts ir datortomogrāfija, kur konstatē palielinātu traheju un/vai galvenos bronhus. Tipiski, ka 3.–4. pakāpes bronhu līmenī dilatācija izzūd. Kritērijs – 3 SD (standartnovirzes) virs cilvēku vidējā elpceļu diametra:
- trahejas diametrs 2 cm virs aortas loka > 3 cm;
- labā bronha diametrs > 2,4 cm;
- kreisā bronha diametrs > 2,3 cm.
Vēl aprakstīts, ka endobronhiālā flourescences mikroskopijā samazinātā elastīgo šķiedru skaita dēļ redzams fluorescences intensitātes samazinājums. [4] Pacientiem ar šo sindromu jāievēro īpaša piesardzība pie intubācijas:
- uzpūsta manžete var nenoslēgt traheju – vai arī nepieciešams daudz gaisa;
- endotraheālā intubācija var radīt izteiktu trahejas stenozi – rekomendē neizmantot intubācijas cauruli ar manžeti.
Terapija
Terapija – visbiežāk simptomātiska: fizioterapija bronhu drenāžai un antibiotikas infekcijas uzliesmojumu gadījumā. Mēģināta plaušu transplantācija, bet rezultāti ilgtermiņā slikti. Ar dažādām sekmēm trahejā un bronhos likti stenti elpceļu diskinēzijas mazināšanai. Perspektīvā pētījumā 35 pacientiem (tikai četriem bija Mounier–Kuhn sindroms) bronhoplastija sniedza labus ilgtermiņa rezultātus. [5] Savukārt pacientam arī ar Marfāna sindromu aprakstīta pat 28 mm bronhu stenta ievietošana. Ilgtermiņa prognoze variabla. Ir labi rezultāti, bet vairākumā gadījumu pacientiem pat ar regulāru fizioterapiju bronhu drenāžai un novērošanu saglabājas vai pat progresē apakšējā respiratorā trakta infekcijas un bieži arī elpošanas mazspēja.