Vēža slimnieki jebkurā audzēja stadijā var just sāpes, tomēr stipras vai izteiktas tās biežāk ir progresējošu un ielaistu vēžu gadījumā III—IV stadijā, kad sāpes ir pat 80 %, vidēji 50—80 % gadījumu, kad terapijā jālieto opioīdi. Sāpju sindroms var saglabāties arī pēc speciālās terapijas, respektīvi, pārciestām operācijām, apstarošanas vai ķīmijterapijas.
Onkoloģiskiem pacientiem papildus var būt citas ar sāpēm saistītas slimības (artrīti, artrozes, neiroloģiskas slimības, diabētiska neiropātija utt.), tad sāpju sastopamības statistika tikai palielinās. Sāpes ir biežākais stacionēšanas iemesls paliatīvās aprūpes nodaļā, un tās ir sastopamas 40—80 % gadījumu.
Pacienti nodaļā tiek stacionēti pēc konsultācijas poliklīnikā vai arī pārvesti ar neatliekamo medicīnisko palīdzību, respektīvi, ar indikācijām “mērenas/stipras sāpes”, ko grūti kupēt ambulatoros apstākļos. Jāpiezīmē, ka runa ir par mērenām/stiprām/neciešamām sāpēm, 5—9 punkti pēc ciparu skalas, vidēji 7. Paliatīvās aprūpes nodaļā 15—30 % gadījumu pacienti iestājas terminālās stadijās, kad sāpes var būt ļoti spēcīgas un, slimniekam mirstot, var strauji pieaugt dienu—nedēļu laikā.
Būtiski ir noteikt sāpju cēloņus, mehānismus, izzināt iepriekš lietotos medikamentus un metodes, to efektivitāti.
Pretsāpju terapijas pamatprincipi
Pretsāpju terapija sastāv no divām būtiskām daļām — bāzes sāpju un izlaušanās sāpju kupēšanas. Pacientiem ar mērenām/stiprām sāpēm vispirms tiek titrēta bāzes sāpju (BS) terapija ar garas darbības opioīdiem, piemēram, tramadolu SR, morfīnu SR, kas darbojas 12 stundas, vai TDS jeb transdermālām fentanila sistēmām, jeb plāksteriem, kuru darbības ilgums ir 72 stundas.
Par bāzes sāpēm uzskata pastāvīgas vai ilgstošas sāpes vismaz 12 stundas diennaktī. [1; 2] Ārstējot hroniskas BS, opioīdu devas titrē (palielina) pakāpeniski, ievērojot zāļu darbības ilgumu, intervālu nesaīsinot, bet vajadzības gadījumā palielinot nākamo devu. Terapijā papildus lieto adjuvantus (antiemētiķus, laksatīvus, sedatīvus, antidepresantus, steroīdus u.c.), kā arī aktīvi novērš medikamentu izraisītas blaknes.
Izlaušanās sāpju raksturojums
Tikai tad, kad ir notitrēta vai pielāgota bāzes sāpju terapija, var runāt par izlaušanās sāpēm (IS). Pēc definīcijas par izlaušanās sāpēm uzskata pārejošu sāpju uzliesmojumu stabili noteiktas opioīdu bāzes terapijas fonā. [3] Par izlaušanās sāpēm neuzskata, ja ir:
- neskaidra sāpju/slimības diagnoze un nediagnosticēts, mainīgs sāpju mehānisms,
- sāpju epizodes bez bāzes sāpju terapijas,
- sākot bāzes sāpju opioīdu titrēšanu,
- nepietiekama, nestabila BS terapija, piemēram, sakarā ar audzēja progresu,
- “pseidopierašanas” sindroms, ja ir nepietiekama bāzes sāpju medikamenta deva,
- “astes sāpes”, BS medikamentiem beidzot darboties. [4]
- Izlaušanās sāpju etioloģija:
- audzēja izsauktas izlaušanās sāpes, piemēram, metastāzes skeletā, orgānos, to cauraugšana,
- netieši inducētas audzēja sāpes — tūskas, skarta nervu sistēma, izraisīts iekaisums u.c.,
- sāpes specifiskas terapijas rezultātā — pēc manipulācijām, operācijām, apstarošanas un ķīmijterapijas,
- blakusslimību izsauktas sāpes — diabēts, neiromuskulāras slimības, kaulu un locītavu slimības. [5]
Onkoloģijā izlaušanās sāpes attīstās 24—95 % vēža pacientu, [6] vidēji 3—4 reizes dienā, ilgums vidēji līdz 30 minūtēm 74 % gadījumu. Visbiežāk IS ir somatiskas (45 %), viscerālas (29 %), neiropātiskas (9 %) un jauktas (16 %). IS etioloģija visbiežāk atšķiras no BS izcelsmes. [7]
Izlaušanās sāpju iedalījums:
- spontānas — izsaucējfaktors lielākoties nav nosakāms. IS var būt jebkurā ķermeņa vietā. Maksimālais sāpju līmenis tiek sasniegts vidēji desmit minūtēs. Epizodes ilgums vidēji līdz 60 minūtēm,
- momentsāpes — vidēji maksimumu sāpes sasniedz piecās minūtēs; epizode ilgst vidēji 45 minūtes,
- prognozējamas — faktori, kas var izsaukt sāpes, piemēram, klepus, meteorisms, noteikts ķermeņa stāvoklis vai tā maiņa,
- neprognozējamas — kritiens, neierastas kustības, trauksme u.c.,
- manipulāciju rezultātā: veicot dažādas procedūras, punkcijas, pārsienot brūci, kustinot bojāto ekstremitāti u.c. [7; 8]
Ārstēšanas iespējas
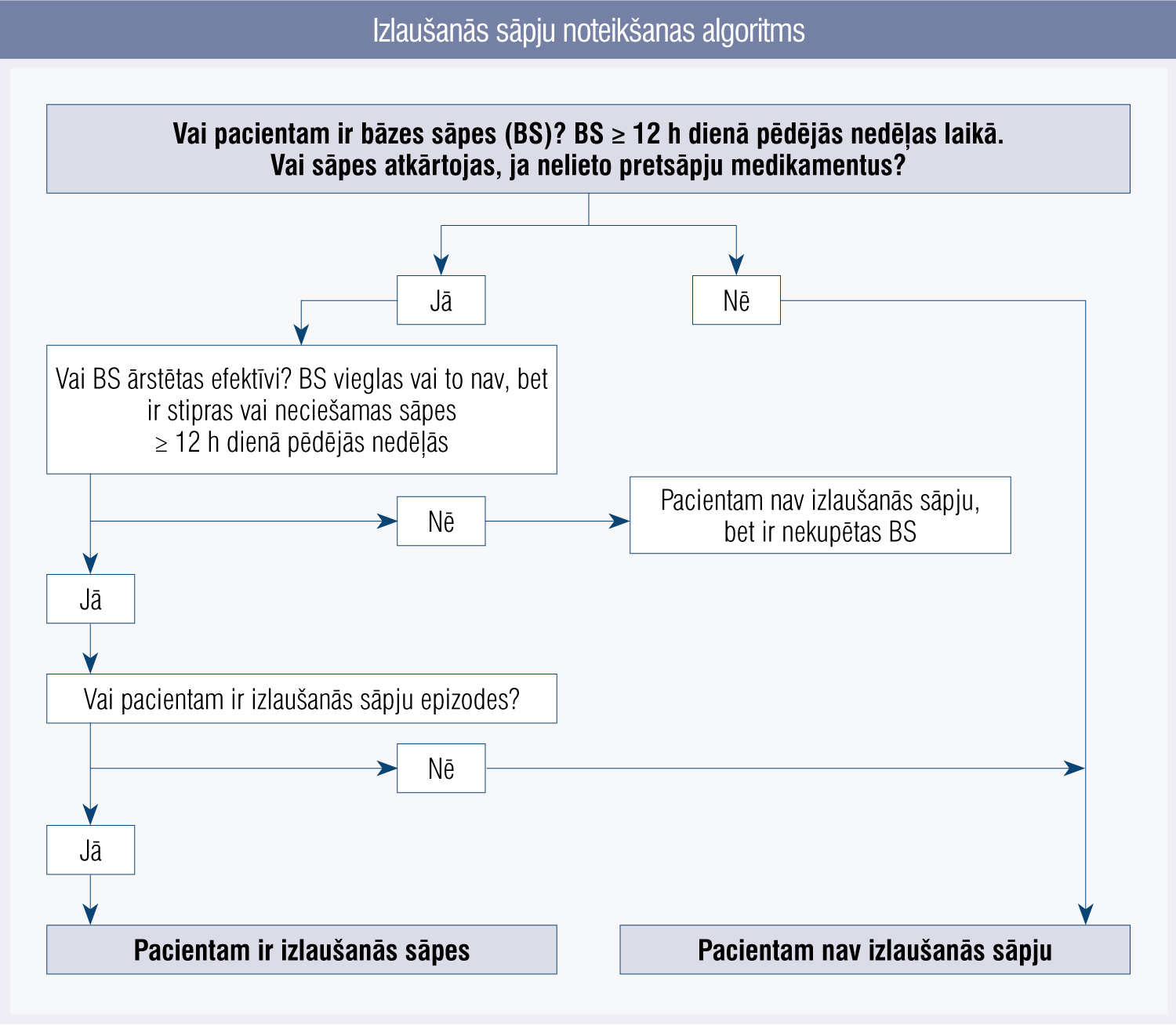

1. attēls
Izlaušanās sāpju noteikšanas algoritms
Izlaušanās sāpes, spontānas sāpes un momentsāpes var kupēt ar ātras darbības NSPL, vājajiem un stiprajiem opioīdiem. Izteiktas IS kupē ar stiprajiem opioīdiem p/o, i/m, i/v. Parenterāla opioīdu ievade ir invazīva un onkoloģijā, paliatīvajā aprūpē (PA) maz piemērota ambulatorajā praksē. Perorālās morfīna ātras darbības tabletes vai šķīdumi Latvijā nav pieejami un to efekts IS gadījumā ir novēlots, ar pagarinātu papildu opioīdu toksicitāti pacientam. [9]
Izlaušanās sāpes visērtāk ir kupēt ar vaiga gļotādas vai zemmēles fentanila tabletēm, kas ātri, ērti un neinvazīvi lietojamas PA un onkoloģijas praksē. Sevišķi svarīgi tas ir ģimenes ārstiem, jo nav nepieciešamas injekcijas, piemēram, izteiktas kaheksijas (barības vada, rīkles u.c. lokalizācijas vēžu), ģeneralizētas tūskas gadījumā. Kā noteikt, vai pacientam ir izlaušanās sāpes? Algoritms apkopots 1. attēlā. [8; 10; 11]
Vaiga un zemmēles gļotādas fentanila tablešu devas
Tablešu devas: 100 µg, 200 µg, 400 µg, 600 µg, 800 µg. Devas titrēšanu sāk ar mazāko devu 100 µg. Biežākās devas klīniskajā praksē ir 200 µg un 400 µg. Pirms tabletes ievietošanas aiz vaiga vai zem mēles, muti vēlams paskalot ar neitrālu ūdeni, lai uzlabotu tabletes uzsūkšanos, jo mutes gļotāda bieži ir sausa (“sausās mutes sindroms”). Otro tableti lieto tad, ja pēc 15—30 minūtēm pretsāpju efekts neiestājas. Devas lielums papildu devai ir nākamais tabletes stiprums, piemēram, ja IS sāk kupēt ar 100 µg, papildu deva būs 100 µg jeb kopā vienas epizodes mazināšanai 200 µg. Nākamo IS epizodi kupē ar 200 µg, bet, ja nepieciešams, tad papildu deva būs 200 µg. Tātad kopā IS epizodei būs nepieciešami 400 µg.
Vienas IS epizodes kupēšanai lieto ne vairāk kā divas tabletes diennaktī, t.i., ≤ 4 fentanila devas, nepieciešamības gadījumā IS devas titrējot jeb kāpinot līdz 8 tabletēm diennaktī. Ja deva ir 800 µg, tad papildu devu nelieto. Ja IS epizodes diennaktī ir > 4, tad pārskata bāzes terapiju, nepieciešamības gadījumā palielinot BS medikamentu devu. Abos gadījumos gan BS, gan IS terapijā devas pielāgo (titrē).
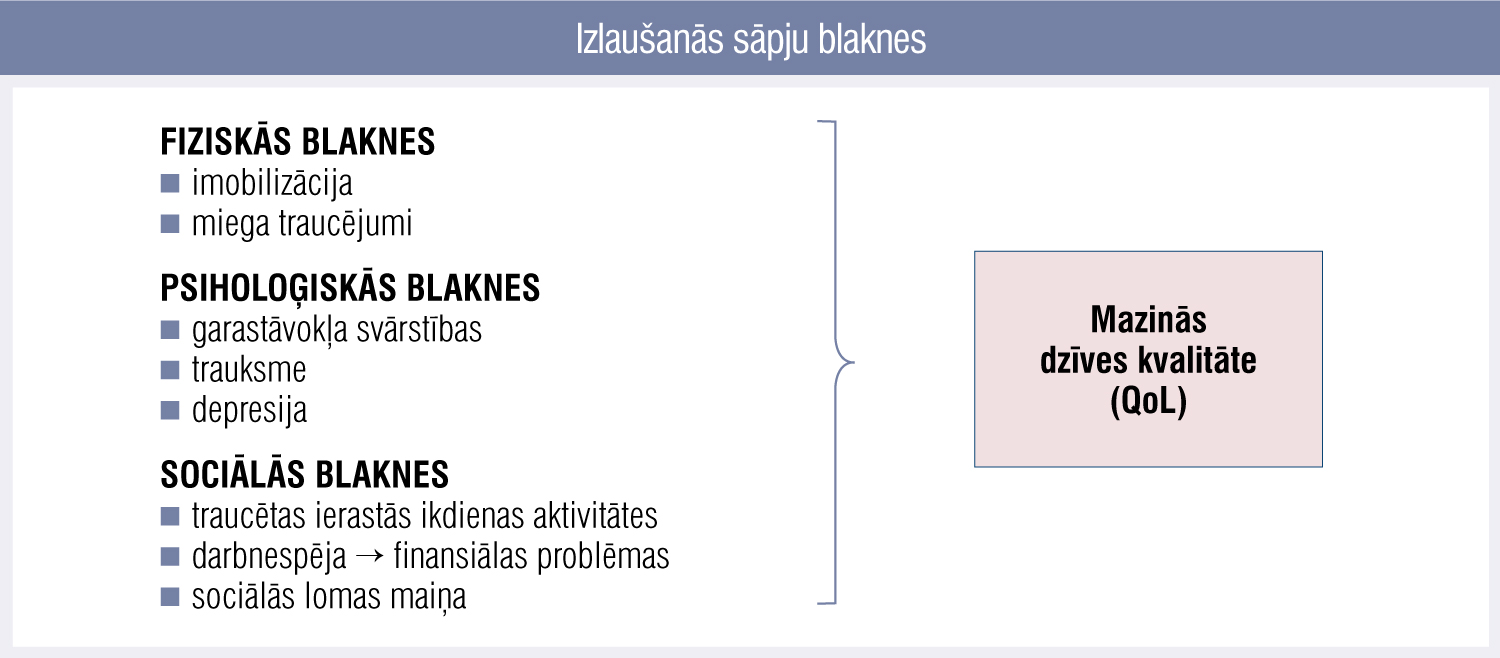

2. attēls
Izlaušanās sāpju blaknes
Izlaušanās sāpes — terapijas vadlīnijas
- IS novērtējums, pacientam ciešot sāpes.
- IS specifisks novērtējums.
- Individuāla IS kupēšana.
- Apsvērt sāpju iemesla ārstēšanas iespējas.
- Novērst/ārstēt sāpes veicinošos faktorus.
- BS analgētisko shēmu modifikācijas iespējas diennakts režīmā.
- IS epizožu ārstēšanā opioīdi ir izvēles medikamenti — perorāli lietojamie opioīdi nav optimālākie IS kupēšanas līdzekļi.
- Opioīda devu IS gadījumā nosaka, individuāli titrējot.
- IS ārstēšanā var noderēt NSPL.
- Ieteicama nefarmakoloģisku metožu izmantošana IS terapijā.
- Lietderīga invazīvo metožu izmantošana IS gadījumos.
- Pacientus ar IS vienmēr atkārtoti specifiski izvērtēt. [12]
Nekupētas IS var būtiski ietekmēt onkoloģisko pacientu dzīves kvalitāti fiziskā, psiholoģiskā, sociālā un garīgā jeb eksistenciālā plānā (2. attēls).