Hronisku nieru slimību diagnosticē pēc šiem kritērijiem — glomerulu filtrācijas ātruma (GFĀ) samazināšanās < 60 ml min./1,73 m² > 3 mēnešus (ar vai bez nieru bojājuma pazīmēm) un/vai nieru bojājuma pazīmes > 3 mēnešus.
Tās var būt: albuminūrija ≥ 30 mg/diennaktī (mikroalbuminūrija), izmaiņas urīna sedimentā (proteinūrija, eritrocitūrija), nieru vizualizācijas metodēs (ultrasonogrāfijā, datortomogrāfijā u.c.), biopsijā pierādīta nieru patoloģija vai izmaiņas asins analīzēs (piemēram, elektrolītu izmaiņas tubulāras disfunkcijas dēļ). [3]
Tātad pacientam ar normālu GFĀ un zināmu strukturālu nieru patoloģiju, piemēram, autosomāli dominantu nieru policistozi, ir HNS 1. stadija. Savukārt pacientam ar samazinātu GFĀ, kas saglabājas > 60 ml/min./1,73 m², bet kuram nav nekādu citu nieru bojājuma pazīmju, HNS diagnozes nebūs.
Ģimenes ārsta vai internista praksē HNS var diagnosticēt, nosakot kreatinīnu serumā un pēc tā aprēķinot GFĀ, kā arī, veicot urīna analīzi, īpašu uzmanību pievēršot mikroalbuminūrijas noteikšanai (ar mikroalbuminūrijas strēmeli, albumīna/kreatinīna attiecību urīnā vai 24 h albuminūrijas noteikšanu) riska grupās: pacientiem ar cukura diabētu, arteriālu hipertensiju un aptaukošanos.
Pēdējā laikā arvien vairāk tiek runāts par kardio—renāli—metaboliskām slimībām (CaReMe conditions), kas norāda uz šo orgānu sistēmu savstarpējo ietekmi.
Pacientiem ar jau diagnosticētu HNS vismaz reizi gadā jāatkārto seruma kreatinīna un albuminūrijas mērījums. Ja GFĀ samazinās zem 60 ml/min./1,73 m², reizi gadā jānosaka hemoglobīna līmenis, bet pacientam ar GFĀ < 30 ml/min./1,73 m² tas jānosaka vismaz divreiz gadā. [3] Jāatceras arī par gadījumiem, kad seruma kreatinīns nebūs precīzs marķieris GFĀ aprēķināšanai, — pacientiem ar samazinātu muskuļu masu, kaheksiju, aptaukošanos, amputētām ekstremitātēm. Tad var noteikt cistatīna C līmeni serumā un pēc tā aprēķināt GFĀ.
HNS iedala piecās stadijās pēc GFĀ (tabula). Svarīgs ir trešās HNS stadijas sadalījums apakšstadijās a un b. GFĀ samazinoties zem 45 ml/min./1,73 m², palielinās HNS izraisītu komplikāciju klīniskās izpausmes. Ja agrīnu HNS uzraudzību var nodrošināt ģimenes ārsts un internists, pacients ar HNS 3.b stadiju ir jānosūta regulārai ambulatorai novērošanai pie nefrologa. Lielākā daļa HNS pacientu nesasniedz terminālu nieru mazspēju (HNS 5. stadiju). Biežākais HNS pacientu nāves iemesls ir kardiovaskulāri notikumi. [3]
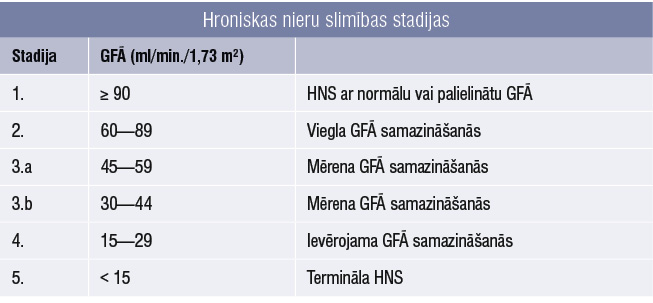

Tabula
Hroniskas nieru slimības stadijas
HNS gaita un nieru funkciju samazināšanās ātrums ir atkarīgs no HNS iemesla, tomēr ir universāli ieteikumi, kas piemērojami visiem HNS pacientiem. HNS progresēšanas faktori, kurus nevaram ietekmēt, ir melnā rase, lielāks vecums, vīriešu dzimums. Savukārt virkne HNS progresēšanas riska faktoru ir ietekmējami, un šeit nozīme ir ārstu rekomendācijām (no vienas puses) un pacientu motivācijai šīs rekomendācijas īstenot (no otras puses). Daudzas rekomendācijas sakrīt ar sirds slimību gadījumā izteiktajām, jo HNS un kardiovaskulārais risks iet roku rokā.
Rekomendācijas HNS pacientam
Arteriāla hipertensija (AH)
AH var būt gan HNS cēlonis, gan tās sekas. 2021. gada KDIGO vadlīnijas rekomendē sistoliskā asinsspiediena (AS) mērķi < 120 mmHg visiem pacientiem ar HNS, kas var to tolerēt, uzsvaru liekot uz pareizu asinsspiediena mērīšanu. [4]
Šīs rekomendācijas pamatā ir pētījuma SPRINT rezultāti, un tā uzsver kardioprotektīvu iedarbību un, iespējams, labvēlīgu ietekmi uz kognitīvo funkciju pacientiem ar HNS, sasniedzot šādu SAS mērķi. Tomēr 2021. gada Eiropas Kardioloģijas biedrības vadlīnijas iesaka mazāk striktus mērķus: sistoliskais AS < 140 mmHg līdz 130 mmHg, ja pacients tolerē, un diastoliskais AS < 80 mmHg. [5]
Arteriālās hipertensijas kontrolei KDIGO vadlīnijas rekomendē arī samazināt sāls lietošanu uzturā < 5 g dienā (atbilst < 2 g nātrija dienā) un veltīt 150 minūtes nedēļā vidējas intensitātes fiziskām aktivitātēm.
Fiziskās aktivitātes var sākt, dienā veltot 10—15 minūtes ātrai pastaigai, peldēšanai, riteņbraukšanai vai kādam sporta veidam, laiku pakāpeniski palielinot līdz 30—60 minūtēm dienā.
Olbaltumvielu daudzums uzturā
Pacientiem ar GFĀ < 30 ml/min./1,73 m² rekomendē olbaltumvielu lietošanu uzturā samazināt līdz 0,8 g/kg/dienā. Visiem pacientiem ar HNS progresēšanas risku iesaka izvairīties no izteikti palielināta olbaltumvielu satura uzturā (> 1,3 g/kg/dienā). [3] Jāatceras, ka pārāk strikta olbaltumvielu ierobežošana var veicināt malnutrīcijas attīstību.
Smēķēšana
Paralēli pārējiem smēķēšanas nelabvēlīgajiem efektiem tā ir saistīta gan ar palielinātu HNS sastopamību, gan ar HNS progresēšanu, gan palielinātu visu cēloņu mirstību. [6; 7] Visiem smēķējošiem HNS pacientiem jārekomendē smēķēšanas atmešana.
Aptaukošanās
Aptaukošanās izraisa plašas metaboliskas izmaiņas organismā. Taukaudi darbojas kā endokrīns orgāns, veicinot iekaisuma, oksidatīvā stresa, insulīnrezistences attīstību un renīna—angiotensīna—aldosterona sistēmas aktivāciju.
Aptaukošanās palielina risku arī HNS biežāko izraisītāju — cukura diabēta un AH — attīstībai, kā arī kopējo kardiovaskulāro notikumu risku. Interesanti, ka HNS cēlonis var būt arī aptaukošanās per se bez pavadoša cukura diabēta un AH.
Ar aptaukošanos saistītas glomerulopātijas (obesity-related glomerulopathy) pamatā ir taukaudu daudzuma palielināšanās nieres sinusā, glomerulārās hipertensijas un hiperfiltrācijas attīstība, kuras rezultātā nieru kamoliņi pieaug izmēros (glomerulomegālija), bet vēlāk tos aizvieto rētaudi — attīstās glomeruloskleroze. Aptaukošanās saistīta arī ar lielāku risku nierakmeņu slimības un nieru audzēju attīstībai. [8; 9]
Hiperlipidēmija
Pacientiem ar HNS ir augsts aterosklerozes un aterosklerotiskas kardiovaskulāras slimības risks. Ja pacientam ar HNS ir dislipidēmija, Eiropas Kardioloģijas biedrība rekomendē statīnu vai statīnu/ezetimiba kombinācijas lietošanu HNS 3.—5. stadijā pacientiem, kuriem nav sākta nieru aizstājterapija.
Nav skaidrs, vai ir ieguvums no šīs terapijas, kad jau sākta dialīze. Vadlīnijas rekomendē turpināt sākto hipolipidemizējošo terapiju arī dialīzē, bet, ja tā nebija sākta, to neparakstīt. [5]
Hiperglikēmija
KDIGO 2020. gada vadlīnijas bez jau minētajiem ieteikumiem rekomendē glikēmijas kontroli ar metformīnu un SGLT2 inhibitoru visiem pacientiem ar 2. tipa cukura diabētu, HNS un GFĀ > 30 ml/min./1,73 m². Tiem pacientiem, kuriem neizdodas sasniegt mērķa glikēmiju ar šo terapiju, rekomendē pievienot glikagonam līdzīgā peptīda–1 receptora agonistu. [10]
Proteinūrija
Proteinūrija ir neatkarīgs HNS progresēšanas un kardiovaskulārā riska faktors. Tā ne tikai norāda uz jau notikušu nieru bojājumu, bet arī pati par sevi veicina ātrāku nieru funkcijas zudumu, bojājot nieru kanāliņus un veicinot intersticiālu fibrozi. Proteinūrijas samazināšana ievērojami ietekmē HNS prognozi. Šeit izceļamas divas nefroprotektīvu medikamentu grupas, kas var aizkavēt HNS progresēšanu.
- Renīna—angiotensīna—aldosterona sistēmas blokāde ar AKE inhibitoriem vai angiotensīna II receptoru blokatoriem (ARB) — tie ne tikai pazemina sistēmisko asinsspiedienu, mazinot AH izraisīto nieru bojājumu, bet arī paplašina nieru kamoliņu eferento arteriolu, tādā veidā samazinot intraglomerulāro spiedienu un proteinūriju. 2021. gada KDIGO vadlīnijas rekomendē AKE inhibitoru vai ARB sākšanu visiem pacientiem ar paaugstinātu asinsspiedienu, HNS un mēreni vai ievērojami palielinātu albuminūriju. Joprojām netiek rekomendēta AKE inhibitoru un ARB vienlaicīga lietošana. [4]
- SGLT2 inhibitori — pēc vairākiem neseniem pētījumiem kļuvis skaidrs, ka ieguvumi no šīs zāļu grupas lietošanas ir daudz plašāki par glikēmijas kontroli pacientiem ar cukura diabētu. Tie samazina HNS progresēšanas, terminālas nieru mazspējas, kardiovaskulāras nāves un ar HNS asociētas nāves risku pacientiem ar un bez cukura diabēta. SGLT2 inhibitoru nefroprotektīvā darbība izpaužas caur pastiprinātu nātrijurēzi un ietekmi uz tubuloglomerulāro atgriezenisko saiti. Rezultātā notiek kamoliņa aferentās arteriolas vazokonstrikcija, samazinās intraglomerulārais spiediens un hiperfiltrācija, tātad arī proteinūrija. SGLT2 inhibitoriem piemīt antioksidatīva darbība. Šobrīd SGLT2 inhibitori indicēti pacientiem ar sirds mazspēju, 2. tipa cukura diabētu, diabētisku nefropātiju un HNS ar albuminūriju, kas nav saistīta ar cukura diabētu, ja GFĀ > 25 ml/min./1,73 m². [11] Pētījumā EMPA–KIDNEY iekļauti pacienti ar HNS bez albuminūrijas, un tā rezultāti viesīs skaidrību par SGLT2 inhibitoru lietošanu arī šajā HNS pacientu apakšgrupā.
Jāņem vērā, ka abu šo grupu medikamenti var izraisīt pārejošu GFĀ mazināšanos pēc terapijas sākšanas (atbilstoši darbības mehānismam, kas pazemina intraglomerulāro spiedienu). Ja GFĀ mazināšanās nepārsniedz 20 %, medikamenta lietošanu var turpināt, kontrolējot kreatinīna līmeni serumā.
Medikamentu lietošanas principi pacientiem ar HNS
- Būtiski atcerēties, ka medikamentu devas HNS pacientiem ir jāpielāgo pacienta aktuālajam GFĀ, turklāt daļa medikamentu mērenas vai smagas pakāpes HNS stadijā ir pat kontrindicēti.
- Pacientiem ar HNS pirms bezrecepšu medikamentu un olbaltumvielu saturošu uztura bagātinātāju lietošanas iesaka konsultēties ar ārstu. Šeit īpaši svarīgi pieminēt nesteroīdo pretiekaisuma līdzekļu (NSPL) lietošanu, ko pacienti mēdz turpināt ilgstoši, nezinot par to iespējamo nefrotoksisko iedarbību un alternatīvām pretsāpju terapijas iespējām. Jāatceras, ka visi NSPL ir potenciāli nefrotoksiski!
- Ja GFĀ < 30 ml/min./1,73 m², jāatceļ metformīns.
- Iespējamas nefrotoksiskas iedarbības dēļ pacientiem ar HNS neiesaka lietot augu valsts izcelsmes līdzekļus bez skaidrām indikācijām.
- Akūtas slimības gadījumā, ja iespējama akūtas nieru mazspējas attīstība, iesaka iespēju robežās uz laiku atcelt potenciāli nefrotoksiskos medikamentus — AKE inhibitorus un ARB, aldosterona antagonistus, urīndzenošos līdzekļus, NSPL, metformīnu, litiju un digoksīnu. [3]
Diētas īpatnības pacientiem ar HNS
Līdzīgi kā visiem, kas rūpējas par savu veselību, HNS pacientiem iesaka pilnvērtīgu, sabalansētu, dažādu uzturu, piemēram, Vidusjūras diētu. Tomēr, mazinoties nieru funkcijai, izteiktāki kļūst HNS metaboliskie traucējumi: nātrija un ūdens pārslodze, hiperkaliēmija, hiperfosfatēmija, metaboliska acidoze.
Pacientiem ar GFĀ < 30 ml/min./1,73 m², lai izvairītos no hiperkaliēmijas, iesaka mazāk lietot kāliju saturošus produktus: žāvētus augļus un riekstus, augļus ar kauliņiem, avokado, kartupeļus, banānus, šokolādi. Ieteicams nepārsniegt > 1000 mg kalcija dienā no visiem kalcija avotiem — uztura (piena produktiem, zaļumiem, zivīm), uztura bagātinātājiem, medikamentiem. Lai gan vēlākām HNS stadijām raksturīga hipokalcēmija, tomēr pastiprināta kalcija lietošana nav vēlama, jo var veicināt asinsvadu pārkaļķošanos. Fosforu saturošus produktus vajadzētu lietot tādā daudzumā, lai fosfora līmenis serumā saglabātos normas robežās. Fosforu satur zivis, piena produkti, zirņi un pupiņas, gaļa un pilngraudu produkti. [12; 13]
Iedvesmai ieviest regulāru HNS skrīningu riska grupu pacientiem un HNS ārstēšanas rekomendācijas savā praksē un ikdienā var izmantot Eiropas Nieru slimību asociācijas (ERA) iniciatīvu StrongKidneys.
ERA izstrādātais plakāts ar padomiem nieru veselības saglabāšanai meklējams šeit: https://www.era-online.org/en/strongkidneys/materials/resources/
Kliedējam mītus!
“Man ar nierēm viss kārtībā, jo man nieres nesāp”
Visbiežāk hroniskas nieru slimības izpausme nebūs sāpes vai diskomforts nieru rajonā! HNS klīniskās izpausmes ir tās komplikāciju — anēmijas, kaulu—minerālvielmaiņas traucējumu, AH, urēmiskas intoksikācijas — izpausmes. Bieži vien šie klīniskie simptomi ir nespecifiski un pacients tos var nesaistīt ar HNS. Tie var būt dažādi domāšanas traucējumi, trauksme un depresija, nemierīgo kāju sindroms, samazināta apetīte, gastrīts, kuņģa čūla, ātrāka nogurdināmība, sausa un niezoša āda, samazināts libido, kaulu lūzumi un daudzi citi. [14]
“Man ir sāpes mugurā, tātad sāp nieres un man ir nieru mazspēja”
HNS jeb nieru mazspēja parasti neizraisa sāpes nieru apvidū. Sāpes nierēs rodas, ja tiek iestiepta nieres kapsula, piemēram, akūta pielonefrīta gadījumā. Sāpes nieru apvidū var būt arī dažu pārmantotu nieru slimību gadījumā, piemēram, autosomāli dominantas nieru policistozes pacientiem. Bet visbiežāk sāpes nieru apvidū ir saistītas ar muskuļu vai mugurkaula patoloģiju.
“Man nav urinācijas traucējumu vai urīna daudzums nav samazināta apjoma, tātad man nav nieru slimības”
Progresējot HNS, protams, lielākoties raksturīga urīna apjoma samazināšanās (īpaši HNS 4. un 5. stadijā), bet daļai pacientu diurēze ir saglabāta, toties pilnvērtīgi neizvadās vielas (metabolisma galaprodukti, toksīni). Tātad par HNS esību nevar spriest pēc diurēzes apjoma, bet gan pēc GFĀ.
“Ja nav HNS simptomu, pie nefrologa nav jānosūta”
Sākot ar HNS 3.b stadiju, pacientiem jābūt nefrologa uzraudzībā, pat ja nav simptomu. Nefrologs izvērtēs un nepieciešamības gadījumā koriģēs iespējamās HNS komplikācijas (renāla anēmija, sekundāra hiperparatireoze) un, ja būs ievērojami samazināts GFĀ, informēs un sagatavos pacientu nieru aizstājterapijai. KDIGO 2012. gada vadlīnijas rekomendē sūtīt pie nefrologa arī pacientus ar nozīmīgu proteinūriju (albumīna/kreatinīna attiecība > 300 mg/g), HNS un rezistentu hipertensiju, kā arī progresējošu HNS. [3]
“Lai atslogotu “nieru darbu”, ir jāuzņem maz šķidruma”
Izņemot HNS 4.—5. stadiju, kad pastiprināta šķidruma uzņemšana var veicināt tūskas un šķidruma pārslodzi, HNS 1.—3. stadijas slimniekiem nav strikti jāierobežo šķidruma uzņemšana. Samazināta šķidruma uzņemšana, īpaši karstā laikā, fiziski darbojoties, vai citkārt, kad palielinās šķidruma zudums organismā, var izraisīt dehidratāciju un akūtu prerenālu nieru mazspēju. Pacientam ar HNS akūtas nieru mazspējas risks šādos apstākļos ir lielāks nekā cilvēkam ar normālu nieru darbību.
“Samazināts GFĀ vienmēr liecinās par patoloģiju”
No 40 gadu vecuma GFĀ dabiski līdz ar vecumu gadā mazinās par ~ 1 ml/min., piemēram, 70 gadus vecam pacientam GFĀ 60 ml/min./1,73 m² atbilst fizioloģiskai vecuma normai. [3; 15] Jāatceras, ka nelielas GFĀ svārstības ir bieža parādība un ne vienmēr norāda uz HNS progresēšanu.